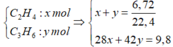Những câu hỏi liên quan
Dẫn V (lít) khí etilen (đktc) qua đúng dịch brom dư , sau khi phản ứng thấy đúng dịch brom mất màu và tạo thành 9,4 gam đibrometan A. Viết phương trình hoá học B.tính giá trị của V C.tính khối lượng dung dịch brom 8% đã tham gia phản ứng
a, PT: \(C_2H_4+Br_2\rightarrow C_2H_4Br_2\)
b, Ta có: \(n_{C_2H_4Br_2}=\dfrac{9,4}{188}=0,05\left(mol\right)\)
Theo PT: \(n_{C_2H_4}=n_{C_2H_4Br_2}=0,08\left(mol\right)\)
\(\Rightarrow V_{C_2H_4}=0,08.22,4=1,792\left(l\right)\)
c, Theo PT: \(n_{Br_2}=n_{C_2H_4Br_2}=0,08\left(mol\right)\)
\(\Rightarrow m_{Br_2}=0,08.160=12,8\left(g\right)\)
\(\Rightarrow m_{ddBr_2}=\dfrac{12,8}{8\%}=160\left(g\right)\)
Đúng 2
Bình luận (0)
Cho 3,36 lít hỗn hợp gồm etan và etilen (ở đktc) đi chậm qua dung dịch brom dư. Sau khi phản ứng thấy khối lượng bình brom tăng thêm 2,8 gam. Số mol etan và etilen trong hỗn hợp lần lượt là:
A. 0,05 và 0,1
B. 0,1 và 0,05.
C. 0,12 và 0,03
D. 0,03 và 0,12.
- Gọi số mol etan là x ; số mol etilen là y. Ta có hệ phương trình :
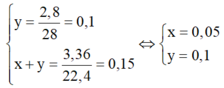
- Chọn đáp án A.
Đúng 0
Bình luận (0)
Dẫn từ từ 6,72 lit (đktc) hỗn hợp X gồm etilen và propilen và dung dịch brom, dung dịch brom bị nhạt màu, và không có khí thoát ra. Khối lượng dung dịch sau phản ứng tăng 9,8 gam. Thành phần phần trăm theo thể tích của etilen trong X là A. 50,00% B. 66,67% C. 57,14% D. 28,57%
Đọc tiếp
Dẫn từ từ 6,72 lit (đktc) hỗn hợp X gồm etilen và propilen và dung dịch brom, dung dịch brom bị nhạt màu, và không có khí thoát ra. Khối lượng dung dịch sau phản ứng tăng 9,8 gam. Thành phần phần trăm theo thể tích của etilen trong X là
A. 50,00%
B. 66,67%
C. 57,14%
D. 28,57%
Cho 3,36 lít hỗn hợp etan và etilen (đktc) đi chậm qua dung dịch brom dư. Sau phản ứng thu khối lượng brom đã phản ứng là 16 gam. Số mol etan và etilen trong hỗn hợp lần lượt là
A. 0,05 và 0,1
B. 0,12 và 0,03
C. 0,03 và 0,12
D. 0,1 và 0,05
Chọn đáp án A
etan không phản ứng với Br2, etilen phản ứng với Br2 theo tỉ lệ 1 : 1
CH2=CH2 + Br2 → CH2Br-CH2Br.
![]()
![]()
![]()
Vậy đáp án đúng cần chọn là A.
Đúng 0
Bình luận (0)
Cho 3,36 lít hỗn hợp etan và etilen (đktc) đi chậm qua dung dịch brom dư. Sau phản ứng thu khối lượng brom đã phản ứng là 16 gam. Số mol etan và etilen trong hỗn hợp lần lượt là A. 0,05 và 0,1 B. 0,12 và 0,03 C. 0,03 và 0,12 D. 0,1 và 0,05
Đọc tiếp
Cho 3,36 lít hỗn hợp etan và etilen (đktc) đi chậm qua dung dịch brom dư. Sau phản ứng thu khối lượng brom đã phản ứng là 16 gam. Số mol etan và etilen trong hỗn hợp lần lượt là
A. 0,05 và 0,1
B. 0,12 và 0,03
C. 0,03 và 0,12
D. 0,1 và 0,05
Dẫn từ từ 4,48 lít hỗn hợp khí etilen và etan (đktc) vào dung dịch brom thấy dung dịch bị nhạt màu và 1,12 lít khí thoát ra. Khối lượng dung dịch brom sau phản ứng m gam. Tính m?
\(V_{C_2H_6} = 1,12\ lít \Rightarrow n_{C_2H_4} = \dfrac{4,48-1,12}{22,4} = 0,15(mol)\\ C_2H_4 + Br_2 \to C_2H_4Br_2\\ m_{tăng}= m_{C_2H_4} = 0,15.28 = 4,2\ gam\)
Đúng 2
Bình luận (0)
Cho 3,36 lít hỗn hợp etan và etilen (đktc) đi chậm qua qua dung dịch brom dư. Sau phản ứng khối lượng bình brom tăng thêm 2,8 gam. Số mol etan và etilen trong hỗn hợp lần lượt là A. 0,05 và 0,1 B. 0,1 và 0,05 C. 0,12 và 0,03 D. 0,03 và 0,12
Đọc tiếp
Cho 3,36 lít hỗn hợp etan và etilen (đktc) đi chậm qua qua dung dịch brom dư. Sau phản ứng khối lượng bình brom tăng thêm 2,8 gam. Số mol etan và etilen trong hỗn hợp lần lượt là
A. 0,05 và 0,1
B. 0,1 và 0,05
C. 0,12 và 0,03
D. 0,03 và 0,12
Đáp án : A
Khối lượng bình brom tăng = khối lượng etilen
=> Khối lượng etilen = 2.8g
-> n etilen = 2.8/28 = 0.1
=> nl etan = 0.15 - 0.1 = 0.05
Đúng 0
Bình luận (0)
Cho 3,36 lít hỗn hợp etan và etilen (đktc) đi chậm qua qua dung dịch brom dư. Sau phản ứng khối lượng bình brom tăng thêm 2,8 gam. Số mol etan và etilen trong hỗn hợp lần lượt là A. 0,05 và 0,1. B. 0,1 và 0,05. C. 0,12 và 0,03. D. 0,03 và 0,12.
Đọc tiếp
Cho 3,36 lít hỗn hợp etan và etilen (đktc) đi chậm qua qua dung dịch brom dư. Sau phản ứng khối lượng bình brom tăng thêm 2,8 gam. Số mol etan và etilen trong hỗn hợp lần lượt là
A. 0,05 và 0,1.
B. 0,1 và 0,05.
C. 0,12 và 0,03.
D. 0,03 và 0,12.
Đáp án A
0,15 mol C2H6 và C2H4 + bình brom dư → mbình tăng = 2,8 gam.
→ mbình tăng = mC2H4 = 2,8 gam → nC2H4 = 2,8 : 28 = 0,1 mol.
nC2H6 = 0,15 - 0,1 = 0,05 mol
Đúng 0
Bình luận (0)
Cho 3,36 lít hỗn hợp etan và etilen (đktc) đi chậm qua qua dung dịch brom dư. Sau phản ứng khối lượng bình brom tăng thêm 2,8 gam. Số mol etan và etilen trong hỗn hợp lần lượt là: A. 0,05 và 0,1 mol. B. 0,1 và 0,05 mol. C. 0,12 và 0,03 mol. D. 0,03 và 0,12 mol.
Đọc tiếp
Cho 3,36 lít hỗn hợp etan và etilen (đktc) đi chậm qua qua dung dịch brom dư. Sau phản ứng khối lượng bình brom tăng thêm 2,8 gam. Số mol etan và etilen trong hỗn hợp lần lượt là:
A. 0,05 và 0,1 mol.
B. 0,1 và 0,05 mol.
C. 0,12 và 0,03 mol.
D. 0,03 và 0,12 mol.