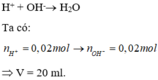Trung hòa 3,65g HCl vào dung dịch NaOH 0,5M .thể tích dung dịch NaOH cần dùng là A 50ml B 100ml C 150ml D 200ml

Những câu hỏi liên quan
Trung hòa 3,65g HCl vào dung dịch NaOH 0,5M .thể tích dung dịch NaOH cần dùng là A 50ml __B 100ml__C 150ml__D 200ml
D.200ml
\(NaOH + HCl \rightarrow NaCl + H_2O\)
\(n_{HCl}= \dfrac{3,65}{36,5}= 0,1 mol\)
Theo PTHH:
\(n_{NaOH}= n_{HCl}= 0,1 mol\)
\(\Rightarrow V_{NaOH}= \dfrac{0,1}{0,5}= 0,2 l = 200 ml\)
Đúng 2
Bình luận (0)
Thể tích dung dịch HCl 2M cần dùng để trung hoà vừa hết 200ml dung dịch hỗn hợp gồm NaOH 0,8M và KOH 0,5M là
130
100
120
200
Số mol OH- là 0,2.(0,8+0,5)=0,26 (mol).
Thể tích dung dịch HCl cần dùng là V=0,26/2=0,13 (lít)=130 (ml).
Đúng 1
Bình luận (0)
\(n_{NaOH}=0,8.0,2=0,16\left(mol\right)\\ n_{KOH}=0,2.0,5=0,1\left(mol\right)\)
PTHH:
KOH + HCl -> KCl + H2O
0,1 ---> 0,1
NaOH + HCl -> NaCl + H2O
0,16 ---> 0,16
\(\Rightarrow V_{ddHCl}=\dfrac{0,1+0,16}{2}=0,13\left(l\right)=130\left(ml\right)\)
Đúng 1
Bình luận (0)
1) để trung hòa 10mL dung dịch HCL nồng độ x M cần 50mL dung dịch NaOH 0,5M. Xác định giá trị của x 2) để chuẩn độ 10mL dung dịch HCL cần 20mL dung dịch NaOH 0,1M. Xác định nồng độ của dung dịch HCL trên
1) Để trung hòa HCl, số mol HCl phải bằng số mol NaOH. Vì vậy, ta có:
n(HCl) = n(NaOH)
x * 10 = 0,5 * 50
x = (0,5 * 50) / 10
x = 2,5 triệu
Vậy, nồng độ của dung dịch HCl là 2.5 M.
2) Ta có:
n(HCl) = n(NaOH)
n(HCl) = 0,1 * 20/10
Vậy, nồng độ của dung dịch HCl là 0.2 M.
Đúng 0
Bình luận (0)
\(1)n_{NaOH}=0,05.0,5=0,025mol\\ NaOH+HCl\rightarrow NaCl+H_2O\\ \Rightarrow n_{NaOH}=n_{HCl}=0,025mol\)
\(C_M\) \(_{HCl}=\dfrac{0,025}{0,01}=2,5M\)
\(2)n_{NaOH}=0,1.0,02=0,002mol\\ HCl+NaOH\rightarrow NaCl+H_2O\\ n_{NaOH}=n_{HCl}=0,002mol\)
\(C_M\) \(_{HCl}=\dfrac{0,002}{0,01}=0,2M\)
Đúng 0
Bình luận (0)
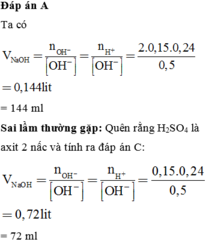
Thể tích dung dịch NaOH 0,5M cần dùng để trung hòa 240ml dung dịch H2SO4 0,15M là
A. 144 ml.
B. 120ml.
C. 72ml.
D. 80ml.
Dung dịch NaOH 40% để trung hòa 200ml dung dịch H3PO4 o,5M.
Tính thể tích dung dịch NaOH cần dùng trên, biết khối lượng riêng của Bazơ này là 1,2g/ml
\(n_{H_3PO_4}=0.2\cdot0.5=0.1\left(mol\right)\)
\(3NaOH+H_3PO_4\rightarrow Na_3PO_4+3H_2O\)
\(0.3..............0.1\)
\(m_{dd_{NaOH}}=\dfrac{0.3\cdot40}{40\%}=30\left(g\right)\)
\(V_{dd_{NaOH}}=\dfrac{30}{1.2}=25\left(ml\right)\)
Đúng 4
Bình luận (0)
PTHH: \(3NaOH+H_3PO_4\rightarrow Na_3PO_4+3H_2O\)
Ta có: \(n_{H_3PO_4}=0,5\cdot0,2=0,1\left(mol\right)\) \(\Rightarrow n_{NaOH}=0,3\left(mol\right)\)
\(\Rightarrow m_{ddNaOH}=\dfrac{0,3\cdot40}{40\%}=30\left(g\right)\) \(\Rightarrow V_{ddNaOH}=\dfrac{30}{1,2}=25\left(ml\right)\)
Đúng 1
Bình luận (0)
3NaOH+H3PO4->Na3PO4+3H2O
Số mol h3po4=0,2.0,5=0,1mol
=> n(NaOH)=0,1.3=0,3mol
mNaOH=0,3.40=12g
mddNaOH=12.100/40=30g
V=m/d=30/1,2=25ml
Đúng 1
Bình luận (0)
Xem thêm câu trả lời
Cho 10 ml dung dịch X chứa HCl 1M và H 2 SO 4 0,5M. thể tích dung dịch NaOH 1M cần để trung hòa dung dịch X là
A. 10 ml.
B. 15 ml.
C. 20 ml.
D. 25 ml.
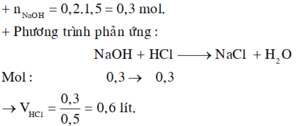
Để trung hoà 200 ml dung dịch NaOH 1,5M thì thể tích dung dịch HCl 0,5M cần dùng là bao nhiêu?
A. 0,5 lít.
B. 0,4 lít
C. 0,3 lít
D. 0,6 lít
Để trung hoà 200 ml dung dịch NaOH 1,5M thì thể tích dung dịch HCl 0,5M cần dùng là bao nhiêu?
A. 0,5 lít
B. 0,4 lít
C. 0,3 lít
D. 0,6 lít
Đáp án D
nNaOH = 0,2.1,5=0,3 (mol)
NaOH + HCl → NaCl + H2O
0,3 → 0,3 (mol)
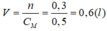
Đúng 0
Bình luận (0)
Câu 1: Để trung hòa 200ml dung dịch NaOH 0,5M cần dùng vừa đủ a gam dung dịch CH3COOH 5%. Giá trị của a là *
A. 200
B. 120
C. 60
D. 240
\(n_{NaOH}=0.2\cdot0.5=0.1\left(mol\right)\)
\(CH_3COOH+NaOH\rightarrow CH_3COONa+H_2O\)
\(0.1.......................0.1\)
\(m_{dd_{CH_3COOH}}=\dfrac{0.1\cdot60\cdot100}{5}=120\left(g\right)\)
=> B
Đúng 3
Bình luận (1)
$CH_3COOH + NaOH \to CH_3COONa + H_2O$
n CH3COOH = n NaOH = 0,2.0,5 = 0,1(mol)
=> m dd CH3COOH = 0,1.60/5% = 120(gam)
Đáp án B
Đúng 2
Bình luận (0)
Ta có: nNaOH = 0,2.0,5 = 0,1 (mol)
PT: \(NaOH+CH_3COOH\rightarrow CH_3COONa+H_2O\)
_____0,1_______0,1 (mol)
⇒ mCH3COOH = 0,1.60 = 6 (g)
\(\Rightarrow m_{ddCH_3COOH}=\dfrac{6}{5\%}=120\left(g\right)\)
⇒ Đáp án: B
Bạn tham khảo nhé!
Đúng 0
Bình luận (0)
Xem thêm câu trả lời