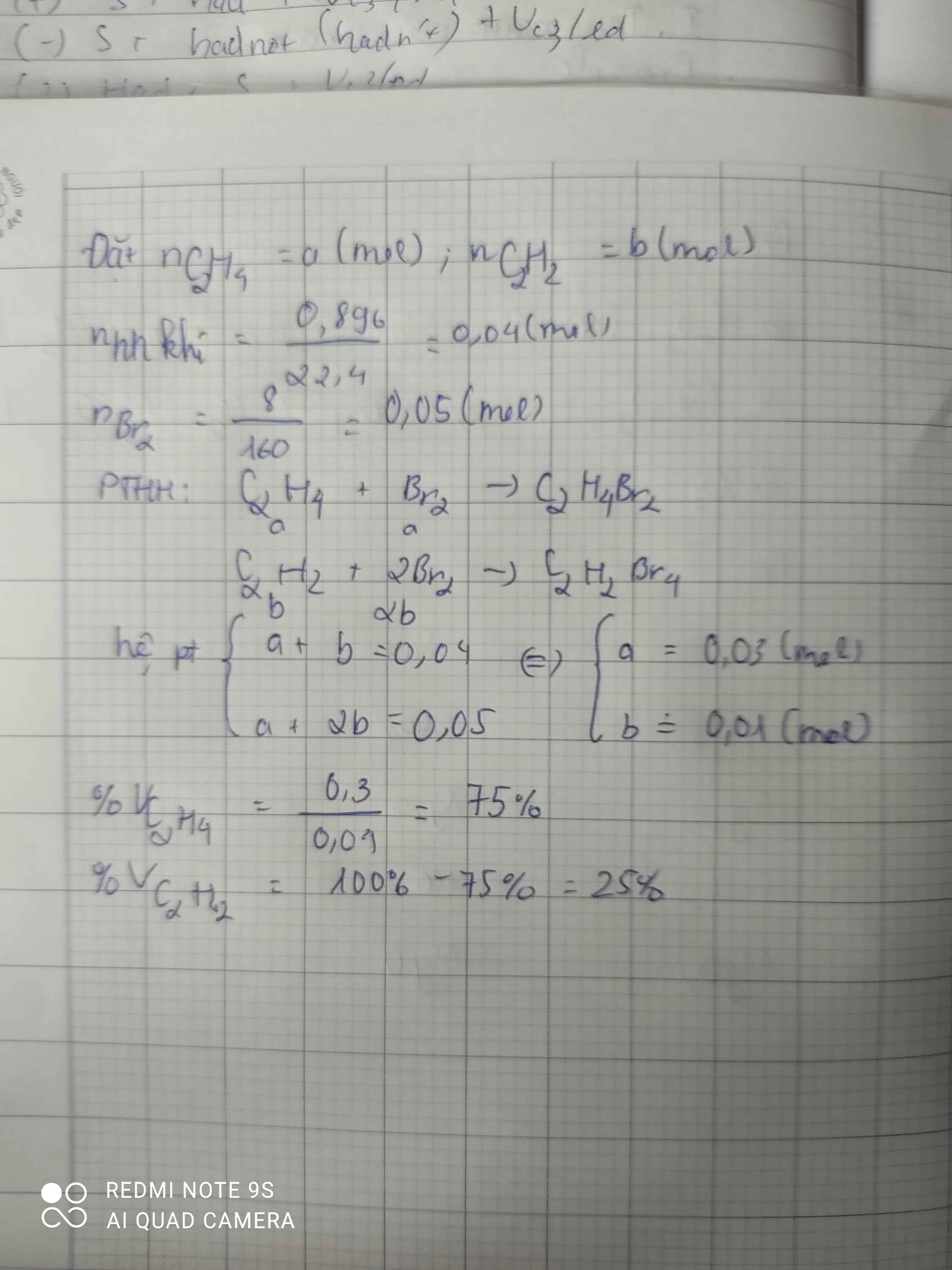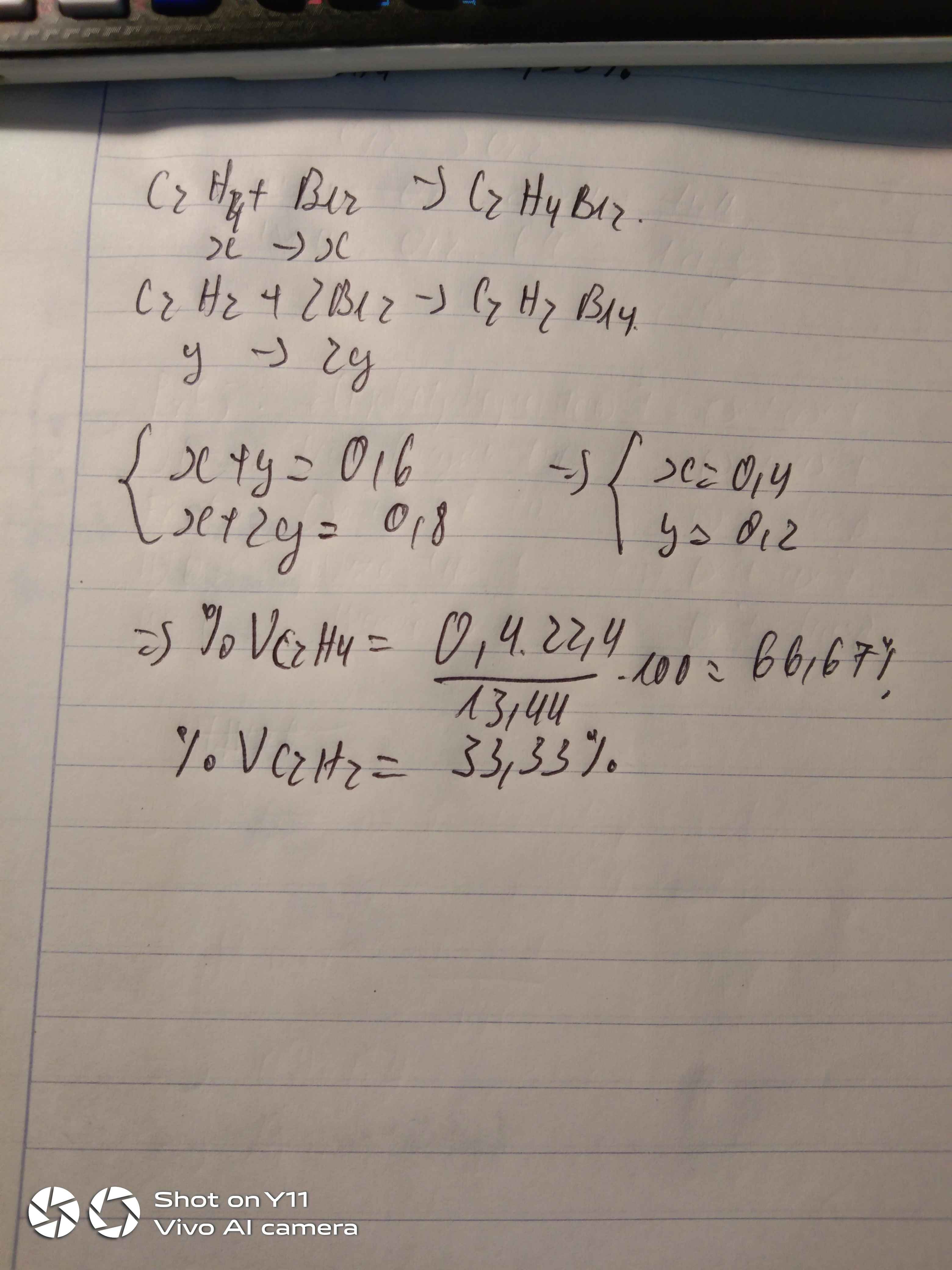Những câu hỏi liên quan
Cho 0,896lit hh gồm C2H4 và C2H2 phản ứng hoàn toàn với dd Br2, thấy có 8g Br2 tham gia. Tính: a/ %(V) mỗi khí trong hh các khí đo ở đkc b/ Khối lượng sản phẩm thu được
Ta có Cùng điều kiện -> Quy số lít về số mol.n(hh ban đầu) = 20 mol; n(hh sau) = 16 lít
=> H2 phản ứng mất 4 lít => C2H2 có 2 lít và CH4 có 8 lít
Đúng 1
Bình luận (0)
a.\(n_{hh}=\dfrac{V_{hh}}{22,4}=\dfrac{0,896}{22,4}=0,04mol\)
\(n_{Br_2}=\dfrac{m_{Br_2}}{M_{Br_2}}=\dfrac{8}{160}=0,05mol\)
Gọi \(n_{C_2H_2}\) là x => \(V_{C_2H_2}=22,4x\)
\(n_{C_2H_4}\) là y => \(V_{C_2H_4}=22,4y\)
\(C_2H_2+2Br_2\rightarrow C_2H_2Br_4\)
x 2x x ( mol )
\(C_2H_4+Br_2\rightarrow C_2H_4Br_2\)
y y y ( mol )
Ta có hpt:
\(\left\{{}\begin{matrix}22,4x+22,4y=0,896\\2x+y=0,05\end{matrix}\right.\) \(\Leftrightarrow\left\{{}\begin{matrix}x=0,01\\y=0,03\end{matrix}\right.\)
\(\Rightarrow\left\{{}\begin{matrix}V_{C_2H_2}=0,01.22,4=0,224\\V_{C_2H_4}=0,03.22,4=0,672\end{matrix}\right.\)
\(\%V_{C_2H_2}=\dfrac{0,224}{0,896}.100=25\%\)
\(\%V_{C_2H_4}=100-25=75\%\)
b.\(m_{Sp}=0,01.186+0,03.346+0,03.188=16,02g\)
( Em cảm ơn anh Kudo Sinichi rất nhiều ạ!! )
Đúng 1
Bình luận (1)
Xem thêm câu trả lời
Cho 8,96 lít một anken X ( đktc) lội quá dd brom dư . Sau pư thấy khối lượng bình brom tăng thêm 22,4g . Khi cho 11,2g X tác dụng với 250ml dd Br2 2M thì thu đc dd Y. Để lm mất màu hoàn toàn dd Y cần dùng hết V lít X(đktc). Giá trị V là?
Xem chi tiết
CT : CnH2n
nX = 8.96/22.4 = 0.4 (mol)
m tăng = mX = 22.4 (g)
MX = 22.40.4 56 (g/mol)
=> 14n = 56
=> n = 4
CT : C4H8
TN2 :
nC4H8 = 11.2/56 = 0.2 (mol)
nBr2 = 0.25*2 = 0.3 (mol)
C4H8 + Br2 => C4H8Br2
dd Y : Br2 dư , C4H8Br2
nC4H8(ct) = 0.3 - 0.2 = 0.1 (mol)
VX = 2.24 (l)
Đúng 1
Bình luận (0)
14. Cho 8,96 lít 1 Anken X(đktc) lội qua dd brom dư. Sau pư thấy khối lượng bình brom tăng thêm 22,4g . Khi cho 11,2g X tác dụng với 250ml dd Br2 2M thì thu đc dd Y. Để làm mất màu hoàn toàn dd Y cần dùng hết V lít X(đktc) . Giá trị V là ?
Xem chi tiết
Theo gt ta có: $n_{X}=0,4(mol);m_{X}=22,4(g)$
Suy ra X có CTPT là $C_4H_8$
Ta có: $n_{X}=0,2(mol);n_{Br_2}=0,5(mol)$
$C_4H_8+Br_2\rightarrow C_4H_8Br_2$
Do đó sau phản ứng dung dịch còn 0,3mol $Br_2$
Để làm mất màu hoàn toàn cần sử dụng 6,72(l) X
Đúng 2
Bình luận (0)
Sục hoàn toàn 6.7 lít hổn hợp X gồm metan vad axetilen vào dd Br2 2M thấy mất màu vừa hết 100ml dd Br2
A) viết pthh
B) tính % thể tích mỗi khí trong X
Xem chi tiết
\(n_{Br_2}=n_{C_2H_4}=0.1\cdot2=0.2\left(mol\right)\)
\(n_{hh}=\dfrac{6.72}{22.4}=0.3\left(mol\right)\)
\(\Rightarrow n_{CH_4}=0.3-0.2=0.1\left(mol\right)\)
\(C_2H_4+Br_2\rightarrow C_2H_4Br_2\)
\(\%CH_4=\dfrac{0.1}{0.3}\cdot100\%=33.33\%\)
\(\%C_2H_4=66.67\%\)
Đúng 1
Bình luận (0)
đun nòn 0,11 mol hh khí T gồm CH4, C2H4, H2 (xúc tác Ni)sau 1 thời gian thu được 0,1 mol hh khí Q có tỉ khối so với H2 bằng 7,7
Cho Q lội qua dd Br2 dư thì có 4,8g Br2 tham gia pứ
Tính % thể tích H2 trong hh Q
\(m_Q=\left(7,7.2\right).0,1=1,54\left(g\right)\)
=> mT = 1,54 (g)
Gọi \(\left\{{}\begin{matrix}n_{CH_4}=a\left(mol\right)\\n_{C_2H_4}=b\left(mol\right)\\n_{H_2}=c\left(mol\right)\end{matrix}\right.\)
=> \(\left\{{}\begin{matrix}a+b+c=0,11\left(1\right)\\16a+28b+2c=1,54\left(2\right)\end{matrix}\right.\)
ngiảm = nH2(pư) = 0,11 - 0,1 = 0,01 (mol)
\(n_{Br_2}=\dfrac{4,8}{160}=0,03\left(mol\right)\)
Bảo toàn liên kết: b = 0,01 + 0,03 = 0,04 (mol) (3)
(1)(2)(3) => a = 0,02 (mol); b = 0,04 (mol); c = 0,05 (mol)
=> nH2(Q) = 0,05 - 0,01 = 0,04 (mol)
=> \(\%V_{H_2}=\dfrac{0,04}{0,1}.100\%=40\%\)
Đúng 2
Bình luận (0)
đốt cháy hoàn toàn 3,36 lít hh ch4 và c2h4 trong không khí , cần dùng 8,96 lít oxi a. tính thể tích mỗi hh b.khối lượng mỗi khí trong hỗn hợp c. nếu dẫn toàn bộ hh khí qua dd br2 1M . Tính Thể Tích dd br2 phản ứng
a, Ta có \(n_{CH_4}+n_{C_2H_4}=\dfrac{3,36}{22,4}=0,15\left(mol\right)\left(1\right)\)
PT: \(CH_4+2O_2\underrightarrow{t^o}CO_2+2H_2O\)
\(C_2H_4+3O_2\underrightarrow{t^o}2CO_2+2H_2O\)
Theo PT: \(n_{O_2}=2n_{CH_4}+3n_{C_2H_4}=\dfrac{8,96}{22,4}=0,4\left(mol\right)\left(2\right)\)
Từ (1) và (2) \(\Rightarrow\left\{{}\begin{matrix}n_{CH_4}=0,05\left(mol\right)\\n_{C_2H_4}=0,1\left(mol\right)\end{matrix}\right.\)
\(\Rightarrow\left\{{}\begin{matrix}V_{CH_4}=0,05.22,4=1,12\left(l\right)\\V_{C_2H_4}=0,1.22,4=2,24\left(l\right)\end{matrix}\right.\)
b, \(m_{CH_4}=0,05.16=0,8\left(g\right)\)
c, \(C_2H_4+Br_2\rightarrow C_2H_4Br_2\)
Theo PT: \(n_{Br_2}=n_{C_2H_4}=0,1\left(mol\right)\Rightarrow V_{ddBr_2}=\dfrac{0,1}{1}=0,1\left(l\right)\)
\(m_{C_2H_4}=0,1.28=2,8\left(g\right)\)
Đúng 1
Bình luận (0)
Biết 0,1 mol hiđrocacbon X làm mất màu tối đa 100ml dd Br2 0,1M . Vậy X là
Biết 0,1 mol hiđrocacbon Y làm mất màu tối đa 200ml dd Br2 1M. Vậy Y là
Khi cho 0,1 lít khí axetilen tác dụng với dd Br2 thì làm mất màu vừa đủ 100ml dd Br2. Vậy nếu cho 0,1 lít khí etilen tác dụng với dd Br2 thì sẽ làm mất màu bao nhiêu ml
Trộn 200ml ancol etylic 20° với 300ml ancol etylic 45° thì được ancol bao nhiêu độ
Nhỏ vài giọt dd iot vào ống nghiệm đựng hồ tinh bột thấy xuất hiện màu
A. Đỏ b. Vàng nhạt c. Xan...
Đọc tiếp
Biết 0,1 mol hiđrocacbon X làm mất màu tối đa 100ml dd Br2 0,1M . Vậy X là Biết 0,1 mol hiđrocacbon Y làm mất màu tối đa 200ml dd Br2 1M. Vậy Y là Khi cho 0,1 lít khí axetilen tác dụng với dd Br2 thì làm mất màu vừa đủ 100ml dd Br2. Vậy nếu cho 0,1 lít khí etilen tác dụng với dd Br2 thì sẽ làm mất màu bao nhiêu ml Trộn 200ml ancol etylic 20° với 300ml ancol etylic 45° thì được ancol bao nhiêu độ Nhỏ vài giọt dd iot vào ống nghiệm đựng hồ tinh bột thấy xuất hiện màu A. Đỏ b. Vàng nhạt c. Xanh d. Tím
Biết 0,1 mol hiđrocacbon X làm mất màu tối đa 100ml dd Br2 0,1M . Vậy X là
Biết 0,1 mol hiđrocacbon Y làm mất màu tối đa 200ml dd Br2 1M. Vậy Y là
Khi cho 0,1 lít khí axetilen tác dụng với dd Br2 thì làm mất màu vừa đủ 100ml dd Br2. Vậy nếu cho 0,1 lít khí etilen tác dụng với dd Br2 thì sẽ làm mất màu bao nhiêu ml
Trộn 200ml ancol etylic 20° với 300ml ancol etylic 45° thì được ancol bao nhiêu độ
Nhỏ vài giọt dd iot vào ống nghiệm đựng hồ tinh bột thấy xuất hiện màu
A. Đỏ b. Vàng nhạt c. Xan...
Đọc tiếp
Biết 0,1 mol hiđrocacbon X làm mất màu tối đa 100ml dd Br2 0,1M . Vậy X là Biết 0,1 mol hiđrocacbon Y làm mất màu tối đa 200ml dd Br2 1M. Vậy Y là Khi cho 0,1 lít khí axetilen tác dụng với dd Br2 thì làm mất màu vừa đủ 100ml dd Br2. Vậy nếu cho 0,1 lít khí etilen tác dụng với dd Br2 thì sẽ làm mất màu bao nhiêu ml Trộn 200ml ancol etylic 20° với 300ml ancol etylic 45° thì được ancol bao nhiêu độ Nhỏ vài giọt dd iot vào ống nghiệm đựng hồ tinh bột thấy xuất hiện màu A. Đỏ b. Vàng nhạt c. Xanh d. Tím
Dẫn 13,44 lit khí C2H4 và C2H2 qua 800ml dd Br2 1M. Thấy Br2 mất màu hoàn toàn không có khí bay ra sau phản ứng. Tính %V mỗi khí
Gọi số mol C2H4, C2H2 là a, b (mol)
=> a + b = \(\dfrac{13,44}{22,4}=0,6\) (1)
nBr2 = 0,8.1 = 0,8 (mol)
PTHH: C2H4 + Br2 --> C2H4Br2
a----->a
C2H2 + 2Br2 --> C2H2Br4
b----->2b
=> a + 2b = 0,8 (2)
(1)(2) => a = 0,4 (mol); b = 0,2 (mol)
=> \(\left\{{}\begin{matrix}\%V_{C_2H_4}=\dfrac{0,4}{0,6}.100\%=66,67\%\\\%V_{C_2H_2}=\dfrac{0,2}{0,6}.100\%=33,33\%\end{matrix}\right.\)
Đúng 4
Bình luận (0)