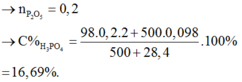Hoà tan 14,2 gam điphotpho pentaoxit vào 180 gam nước.a) Tính khối lượng axit photphoric thu được.b) Tính nồng độ % của dung dịch axit photphoric.

Những câu hỏi liên quan
Hoà tan 28,4 gam điphotpho pentaoxit trong 500 gam dung dịch axit photphoric có nồng độ 9,8%. Nồng độ % của dung dịch axit photphoric thu được là A. 17,04% B. 17,64% C. 16,69% D. 18,02%
Đọc tiếp
Hoà tan 28,4 gam điphotpho pentaoxit trong 500 gam dung dịch axit photphoric có nồng độ 9,8%. Nồng độ % của dung dịch axit photphoric thu được là
A. 17,04%
B. 17,64%
C. 16,69%
D. 18,02%
Hoà tan 28,4 gam điphotpho pentaoxit trong 500 gam dung dịch axit photphoric có nồng độ 9,8%. Nồng độ % của dung dịch axit photphoric thu được là A. 17,04% B. 17,64% C. 16,69% D. 18,02%
Đọc tiếp
Hoà tan 28,4 gam điphotpho pentaoxit trong 500 gam dung dịch axit photphoric có nồng độ 9,8%. Nồng độ % của dung dịch axit photphoric thu được là
A. 17,04%
B. 17,64%
C. 16,69%
D. 18,02%
Đáp án C
→ n P 2 O 6 = 0 , 2 → C % H 3 P O 4 = 98 . 0 , 2 . 2 + 500 . 0 , 098 500 + 28 , 4 . 100 % = 16 , 69 %
Đúng 0
Bình luận (0)
Hoà tan 28,4 gam điphotpho pentaoxit trong 500 gam dung dịch axit photphoric có nồng độ 9,8%. Nồng độ % của dung dịch axit photphoric thu được là A. 17,04% B. 17,64% C. 16,69% D. 18,02%
Đọc tiếp
Hoà tan 28,4 gam điphotpho pentaoxit trong 500 gam dung dịch axit photphoric có nồng độ 9,8%. Nồng độ % của dung dịch axit photphoric thu được là
A. 17,04%
B. 17,64%
C. 16,69%
D. 18,02%
Đáp án C.
→ n P 2 O 5 = 0 , 2 → C % H 3 P O 4 = 16 , 69 %
Đúng 0
Bình luận (0)
Bài 5: Cho 28,4 gam điphotpho pentaoxit tác dụng với 216 gam nước.
a) Viết phương trình hóa học của phản ứng.
b) Tính khối lượng axit photphoric thu được.
c) Dung dịch sau phản ứng làm đổi màu giấy quỳ tím như thế nào?
\(n_{P_2O_5}=\dfrac{28,4}{142}=0,2mol\)
\(n_{H_2O}=\dfrac{216}{18}=12mol\)
\(P_2O_5+3H_2O\rightarrow2H_3PO_4\)
0,2 < 12 ( mol )
0,2 0,4 ( mol )
\(m_{H_3PO_4}=0,4.98=39,2g\)
Dung dịch sau phản ứng làm quỳ tím hóa xanh
Đúng 3
Bình luận (1)
Cho 2,13 gam điphotpho pentaoxit tác dụng hoàn toàn với nước người ta thu được 250 gam dung dịch axit photphoric. Tính nồng độ phần trăm của dung dịch axit thu được.
Please help me !!!
nP2O5 = 0,015 mol
P2O5 + 3H2O \(\rightarrow\) 2H3PO4
\(\Rightarrow\) C% = \(\dfrac{0,03.98.100\%}{250}\) = 1,176%
Đúng 0
Bình luận (0)
nP2O5 = \(\dfrac{2,13}{142}\)=0,015 mol
P2O5 + 3H2O -> 2H3PO4
0,015 ->0,03
=>mH3PO4 = 0,03 . 98 = 2,94 g
C% = \(\dfrac{2,94}{2,13+250}\) .100% = 1,166%
Đúng 0
Bình luận (0)
Hòa tan 28,4 gam photpho (V) oxit trong 500gam dung dịch axit photphoric có nồng độ 9,8%. C% của dung dịch axit photphoric thu được là: A. 17,04% B. 17,64% C. 16,69% D. 18,02%
Đọc tiếp
Hòa tan 28,4 gam photpho (V) oxit trong 500gam dung dịch axit photphoric có nồng độ 9,8%. C% của dung dịch axit photphoric thu được là:
A. 17,04%
B. 17,64%
C. 16,69%
D. 18,02%
Hoà tan 28,4 gam photpho (V) oxit trong 500 gam dung dịch axit photphoric có nồng độ 9,8%. Nồng độ % của dung dịch axit phốtphoric thu được là
Xem chi tiết
mk chỉ hd kiểu này nha
n P2O5=0.2m ; nH3PO4= 0.5 m (500/98*9.8%)
hòa tan P2O5 vào nc có pư: P2O5 + 3 H2O ----> 2H3PO4
___> tổng n H3PO4 = 0.5+0.4= 0.9m ====>88.2g
có mdd sau pư = m p205 + m h3po4 = 28.4 + 88.2 = 116.6g
=> C% h3po4 = (tự giải tiếp nha lười nghĩ :)))))
1 like nha mn
à nhầm chỗ m dd sau pư nha
phải là 28.4+500= 528.4 g chứ :)))
Cho 5,68 gam P 2 O 5 vào cốc chứa 2,7 gam H 2 O thu được dung dịch axit photphoric H 3 P O 4 . Tính khối lượng axit tạo thành.
1. hoà tan 4,6 gam natri vào nước, tính thể tích khí thoát ra đktc. tính khối lượng bazo tạo thành
2. hoà tan 14,2 gam điphotpho penta oxit(P²O⁵) vào nước. tính khối lượng axit tạo thành
Xem chi tiết
\(1\\ 2Na + 2H_2O \to 2NaOH + H_2\\ n_{H_2} = \dfrac{1}{2}n_{Na} = \dfrac{1}{2}.\dfrac{4,6}{23} = 0,1(mol)\\ \Rightarrow V_{H_2} = 0,1.22,4 = 2,24(lít)\\ 2\\ P_2O_5 + 3H_2O \to 2H_3PO_4\\ n_{H_3PO_4} = 2.n_{P_2O_5} = 2.\dfrac{14,2}{142} = 0,2(mol)\\ \Rightarrow m_{H_3PO_4} = 0,2.98 = 19,6\ gam\)
Đúng 3
Bình luận (1)
Câu 1:
PTHH: \(Na+H_2O\rightarrow NaOH+\dfrac{1}{2}H_2\uparrow\)
Ta có: \(n_{Na}=\dfrac{4,6}{23}=0,2\left(mol\right)\)
\(\Rightarrow\left\{{}\begin{matrix}n_{H_2}=0,1\left(mol\right)\\n_{NaOH}=0,2\left(mol\right)\end{matrix}\right.\) \(\Rightarrow\left\{{}\begin{matrix}V_{H_2}=0,1\cdot22,4=2,24\left(l\right)\\m_{NaOH}=0,2\cdot40=8\left(g\right)\end{matrix}\right.\)
Câu 2:
PTHH: \(P_2O_5+3H_2O\rightarrow2H_3PO_4\)
Ta có: \(n_{P_2O_5}=\dfrac{14,2}{142}=0,1\left(mol\right)\)
\(\Rightarrow n_{H_3PO_4}=0,2\left(mol\right)\) \(\Rightarrow m_{H_3PO_4}=0,2\cdot98=19,6\left(g\right)\)
Đúng 1
Bình luận (0)