tính thể tích , khối lượng , phân tử khối cảu các hỗn hợp : a) 5,6g N2 và 0,5 mol SO2 b) 4,8g O3 và 2,24 lít CO2 ở điều kiện tiêu chuẩn

Những câu hỏi liên quan
Bài 5 : Tính khối lượng của các hỗn hợp sau
d) Hỗn hợp Y gồm 3,36 lít SO2 và 13,44 lít CH4 ở đktc
Bài 6 : Tính thể tích của các hỗn hợp khí sau ở điều kiện tiêu chuẩn
a) 0,15 mol CO2, 0,2 mol NO2, 0,02 mol SO2 và 0,03 mol N2
Bài 5:
\(m_{Y}=m_{SO_2}+m_{CH_4}=\dfrac{3,36}{22,4}.64+\dfrac{13,44}{22,4}.16=19,2(g)\)
Bài 6:
\(V_{CO_2}=0,15.22,4=3,36(l)\\ V_{NO_2}=0,2.22,4=4,48(l)\\ V_{SO_2}=0,02.22,4=0,448(l)\\ V_{N_2}=0,03.22,4=0,672(l)\)
Đúng 0
Bình luận (0)
Cho hỗn hợp khí ở điều kiện tiêu chuẩn gồm: 11,2 lít khí CO2 và 0,6.1023 phân tử khí SO2
a/Tính số mol của các khí có trong hỗn hợp.
b/Tính khối lượng hỗn hợp.
hỗn hợp A gồm chứa 0,2 mol SO2 , 0,6.10^23 phân tử CL2 , 1,2.10^23 phân tử N2
hỏi:
a, tính khối lượng của chat A?
b, tính khối lượng mol của chất A?
c, tính thể tích của A ở điều kiện thường và điều kiện tiêu chuẩn?
mSO2= 0,2.(32+16.2)= 8,8(g)
nCl2= \(\frac{0,6.10^{23}}{6.10^{23}}\)=0,1 mol
mCl2= 0,1. 35,5.2 = 7,1(g)
nN2= \(\frac{1,2.10^{23}}{6.10^{23}}\)=0,2 mol
mN2= 0,2.14.2= 5,6 (g)
=> mA= 8,8+7,1+5,6=21,5 (g)
Đúng 1
Bình luận (0)
b) nA= 0,2+0,1+0,2= 0,5 mol
MA= \(\frac{21,5}{0,5}\)= 43
Đúng 1
Bình luận (0)
ở đkt, VA= 0,5.24= 12 (l)
ở đktc, VA= 0,5.22.4= 11,2 (l)
Đúng 1
Bình luận (0)
Hãy tìm thể tích của những lượng khí sau ở điều kiện tiêu chuẩn :
a)0,4 mol phân tử CO2
b) Hỗn hợp khí gồm có : 0,25 mol N2 và 0,5 mol O2
c) 0,5 mol phân tử H2S
\(a,V_{CO_2}=0,4.22,4=8,96(l)\\ b,V_{hh}=22,4.(0,25+0,5)=16,8(l)\\ c,V_{H_2S}=0,5.22,4=11,2(l)\)
Đúng 1
Bình luận (0)
Hỗn hợp khí X chứa CO2, H2 và khí A ở điều kiện tiêu chuẩn. Trong X, thành phần % về thể tích của
CO2 là 20%, của H2 là 50%, thành phần % về khối lượng của CO2 là 45,36%. Tính khối lượng mol phân tử của
chất A
Câu 5: Thể tích của hỗn hợp khí X gồm: 0,1 mol CO2; 0,2 mol H2 và 0,7 mol O2 ở điều kiện tiêu chuẩn là:A. 15,68 lít. B. 3,36 lít. C. 22,4 lít. D. 6,72 lít.Câu 6: Lượng chất có chứa N (6.1023) nguyên tử hoặc phân tử chất đó được gọi là:A. mol. B. khối lượng mol. C. thể tích mol D. tỉ khối.Câu 7: Cho sơ đồ phản ưng: Fe2O3 + HCl 4 FeCl3 + H2O. Để hòa tan hoàn toàn 8 gam sắt (III) oxit Fe2O3 cần dùng bao nhiêu gam axit clohiđric.A. 3,65 g. B. 4,475. C. 10,65. D. 10,95.Câu 8: Nguyên tử khối của cacbo...
Đọc tiếp
Câu 5: Thể tích của hỗn hợp khí X gồm: 0,1 mol CO2; 0,2 mol H2 và 0,7 mol O2 ở điều kiện tiêu chuẩn là:
A. 15,68 lít. B. 3,36 lít. C. 22,4 lít. D. 6,72 lít.
Câu 6: Lượng chất có chứa N (6.1023) nguyên tử hoặc phân tử chất đó được gọi là:
A. mol. B. khối lượng mol. C. thể tích mol D. tỉ khối.
Câu 7: Cho sơ đồ phản ưng: Fe2O3 + HCl 4 FeCl3 + H2O. Để hòa tan hoàn toàn 8 gam sắt (III) oxit Fe2O3 cần dùng bao nhiêu gam axit clohiđric.
A. 3,65 g. B. 4,475. C. 10,65. D. 10,95.
Câu 8: Nguyên tử khối của cacbon bằng 3/4 nguyên tử khối của oxi. Biết nguyên tử khối của cacbon là 12 đvC, suy ra nguyên tử khối của oxi là
A. 12 đvC. B. 14 đvC. C. 16 đvC. D. 32 đvC.
Câu 9: Trong 1 mol nước chứa số nguyên tử H là
A. 6.1023. B. 12.1023. C. 18.1023. D. 24.1023.
Câu 10: Trong 1,8 mol CH4 có tất cả bao nhiêu phân tử CH4?
A. 6.1023 . B. 1,08.10-23 . C. 1,08.1023 D. 1,08.1024.
Câu 11: Khối lượng mol của hợp chất Ca(H2PO4)2 là:
A. 234 g/mol. B. 170 g.mol. C. 137 g.mol. D. 88 g/mol
Câu 12: Một hợp chất có chứa 50% S còn lại là O. Tỉ lệ số mol nguyên tử tối giản nhất của S và O là:
A. 1:1 B. 2:1. C. 1:2. D. 2:
Câu `5`:
`V_(CO2) = n . 22,4 = 0,1 . 22,4 =2,24 ` (l)
`V_(H_2) = n.22,4 = 0,2 . 22,4=4,48 `( l)
`V_(O_2) = n . 22,4 = 0,7 . 22,4 =15,68` (l)
`=> V_X= 2,24 + 4,48 + 15,68 = 22,4`(l)
`->`Chọn `C`
Câu `6: A `
Câu `7`:
Cân bằng PT: `Fe_2O_3 + 6HCl -> 2FeCl_3 + 3H_2O`
`n_(Fe_2O_3)= 8/(2.56 + 3.16) = 0,05` (mol)
`n_(HCl) = ( 0,05 .6)/1 = 0,3 ` (mol)
`m_(HCl) = 0,3 . (1 + 35,5) = 10,95` (g)
`->` Chọn `D`
Câu `8`:
Nguyên tử khối của oxi `= 12 : 3/4 =16` ( đvC)
`->` Chọn `C`
Câu `9`: `A`
Câu `11`: `=40+ 2( 2.1 + 31 + 4.16) =234` (g)
`->` Chọn `A`
Câu `12`:`C`
Đúng 0
Bình luận (0)
a. Thể tích của 0,8 mol khí NH3 (đktc) b. Thể tích ở đktc của 140 g khí Nitơ ; 96g khí Oxi c. Thể tích của hỗn hợp khí gồm 0,5 mol Cl2 và 0,2 mol N2 ở điều kiện tiêu chuẩn. d. Khối lượng của hỗn hợp 0,25 mol khí NH3 , 28lit khí CO.
\(a.V_{NH_3}=0,8.22,4=17,92\left(l\right)\\ b.n_{N_2}=\dfrac{140}{28}=5\left(mol\right)\\ V_{N_2}=112\left(l\right)\\ n_{O_2}=\dfrac{96}{32}=3\left(mol\right)\\ V_{O_2}=22,4.3=67,2\left(l\right)\)
\(c.n_{hh}=0,5+0,2=0,7\left(mol\right)\\ V_{hh}=0,7.22,4=15,68\left(l\right)\\ d.m_{NH_3}=4,25\left(g\right)\\ n_{CO}=\dfrac{28}{22,4}=1,25\left(mol\right)\\ m_{CO}=1,25.28=35\left(g\right)\\ m_{hh}=4,25+35=39,25\left(g\right)\)
Đúng 0
Bình luận (0)
a. Thể tích của 0,8 mol khí NH3 (đktc)
=>VNH3=0,8.22,4=17,92l
b. Thể tích ở đktc của 140 g khí Nitơ ; 96g khí Oxi
nN2=140\14.2=5 mol
nO2=96\32=3 mol
=>Vhh=(5+3).22,4=179,2l
c. Thể tích của hỗn hợp khí gồm 0,5 mol Cl2 và 0,2 mol N2 ở điều kiện tiêu chuẩn.
=>Vhh=(0,5+0,2).22,4=15,68l
d. Khối lượng của hỗn hợp 0,25 mol khí NH3 , 28lit khí CO.
n CO=28\22,4=1,25 mol
=>mhh=0,25.17+1,25.28=39,25g
Đúng 1
Bình luận (0)
1 tính thể tích khí của các hỗn hợp chất khí sau ở đktc và tính điều kiện thường:
a )0,1 mol CO2 ; 0,2 mol NO2 ; 0,02 mol SO2 và 0,03 mol N2
b) 0,04 mol N2O; 0,015 mol NH3; 0,06 mol H2 ;0,08 mol H2S
2 tính thể tích khí ở đktc của
a )0,5 mol phân tử khí H2 ;0,8 mol phân tử khí O2
B )2 mol CO2 ; 3 mol khí CH4
C) 0,9 m khí N2; 1,5 mol khí H2
1.
\(a.\)
\(V_{hh}=\left(0.1+0.2+0.02+0.03\right)\cdot24=8.4\left(l\right)\)
\(b.\)
\(V_{hh}=\left(0.04+0.015+0.06+0.08\right)\cdot24=4.68\left(l\right)\)
\(2.\)
\(a.\)
\(V_{H_2}=0.5\cdot22.4=11.2\left(l\right)\)
\(V_{O_2}=0.8\cdot22.4=17.92\left(l\right)\)
\(b.\)
\(V_{CO_2}=2\cdot22.4=44.8\left(l\right)\)
\(V_{CH_4}=3\cdot22.4=67.2\left(l\right)\)
\(c.\)
\(V_{N_2}=0.9\cdot22.4=20.16\left(l\right)\)
\(V_{H_2}=1.5\cdot22.4=33.6\left(l\right)\)
Đúng 4
Bình luận (0)
Hỗn hợp X gồm hai amin A và B no, đơn chức, mạch hở (MA MB), hơn kém nhau 2 nguyên tử cacbon), axit axetic và axit maleic (HOOC-CHCH-COOH); hỗn hợp Y gồm anđehit oxalic và axit hydracrylic (HO-C2H4-COOH). Đốt cháy 9,79 gam hỗn hợp M gồm a mol X và b mol Y cần 10,584 lít O2 thu được 0,784 lít N2 và số mol H2O lớn hơn số mol CO2 là 0,055 mol. Biết thể tích các khí đo ở điều kiện tiêu chuẩn. Phần trăm khối lượng của A trong M lớn nhất là A. 9,5%. B. 29,9%. C. 32,5% D. 12,3%
Đọc tiếp
Hỗn hợp X gồm hai amin A và B no, đơn chức, mạch hở (MA < MB), hơn kém nhau 2 nguyên tử cacbon), axit axetic và axit maleic (HOOC-CH=CH-COOH); hỗn hợp Y gồm anđehit oxalic và axit hydracrylic (HO-C2H4-COOH). Đốt cháy 9,79 gam hỗn hợp M gồm a mol X và b mol Y cần 10,584 lít O2 thu được 0,784 lít N2 và số mol H2O lớn hơn số mol CO2 là 0,055 mol. Biết thể tích các khí đo ở điều kiện tiêu chuẩn. Phần trăm khối lượng của A trong M lớn nhất là
A. 9,5%.
B. 29,9%.
C. 32,5%
D. 12,3%
Chọn đáp án B
Nhận thấy: HOOC-C2H4-COOH và OHC-CHO có công thức tối giản là CHO
CH3COOH và HO-C2H4-COOH có công thức tối giản là CH2O
Các amin đều đơn chức, BTNT.N Þ nAmin = 0,035x2 = 0,07
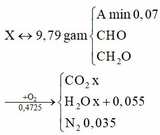
Ta có nH2O – nCO2 = l,5nAmin - 0,5nCHO Þ 1,5x0,07 - 0,5nCHO = 0,055 Þ nCHO = 0,1
BTKL Þ 9,79 + 0,4725x32 = 44x + 18x(x + 0,055) + 0,035x28 Þ x = 0,37
BTNT.O Þ nCH2O = 0,37x2 + (0,37 + 0,055) - 0,4725x2 - 0,1 = 0,12
BTNT.C Þ nC trong amin = 0,37 - 0,12 - 0,1 = 0,15
Þ C trung bình amin = 0,15/0,07 = 2,14 mà 2 amin này lệch nhau 2 nguyên tử cacbon
Þ Có 2 trường hợp có thể xảy ra là:

Đúng 0
Bình luận (0)





















