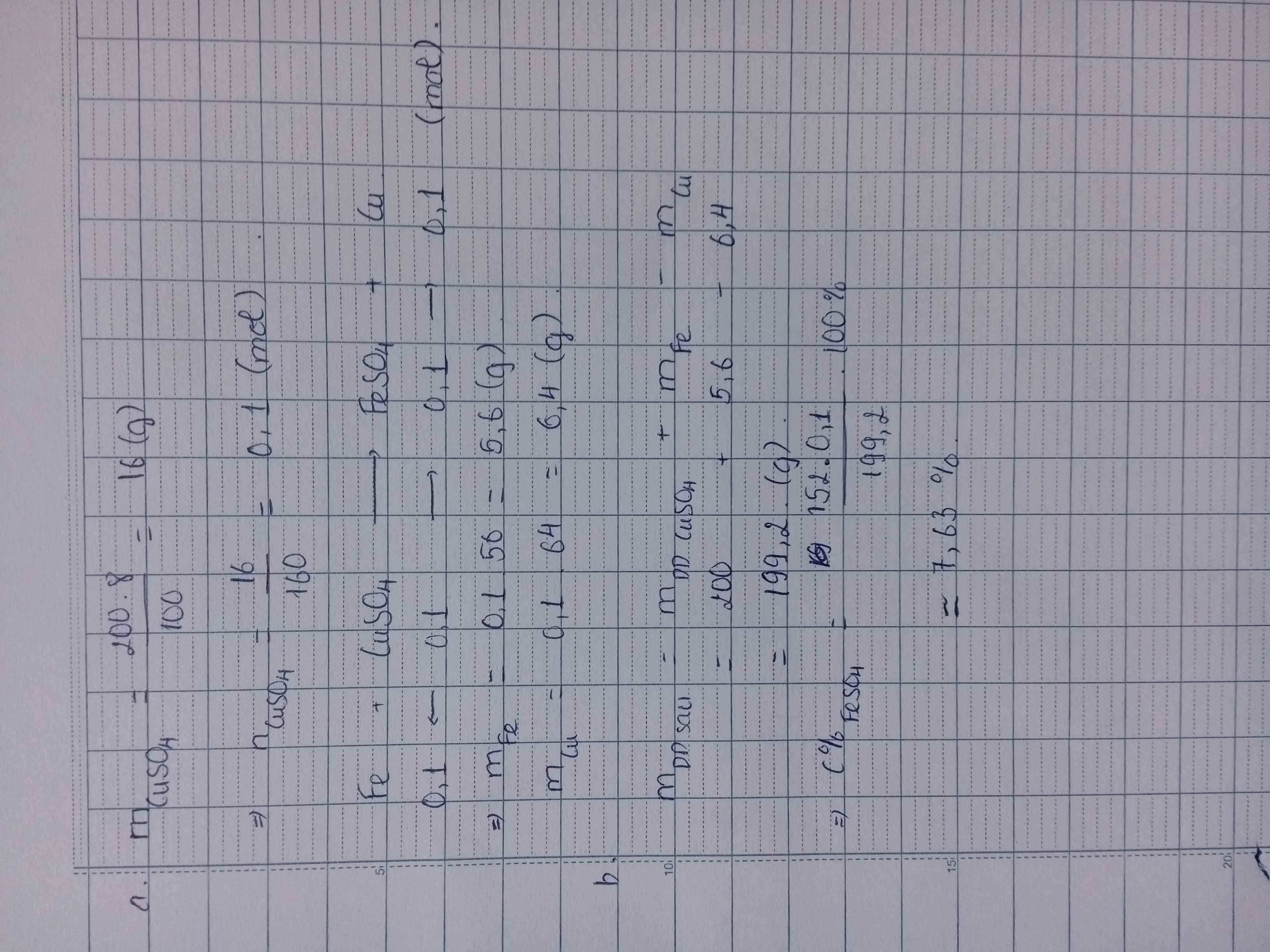Ngâm lá đồng trong 25,5 gam dung dịch AgNO3 10% cho đến khi đồng không tan được nữa. Khối lượng đồng đã tham gia phản ứng là

Những câu hỏi liên quan
Ngâm một lá Zn trong 20 gam dung dịch CuSO4 có nồng độ 10% cho đến khi kẽm không tan được nữa a) Tính khối lượng kém đã tham gia phản ứng với dung dịch trên .b)Tính nồng độ phần trăm của dung dịch sau phản ứng
PTHH : \(Zn+CuSO_4\rightarrow ZnSO_4+Cu_{\downarrow}\)
Đúng 2
Bình luận (0)
b1 ngâm một lá cu trong 150g dung dịch agno3 6,8% cho đến khi cu k tan được nữa tính khối lượng của Cu tham gia phản ứng cà c% của dung dịch sau phản ứng
$n_{AgNO_3} = \dfrac{150.6,8\%}{170} =0,06(mol)$
$Cu+ 2AgNO_3 \to Cu(NO_3)_2 + 2Ag$
Theo PTHH :
$n_{Cu} = \dfrac{1}{2}n_{AgNO_3} = 0,03(mol)$
$m_{Cu} =0,03.64 = 1,92(gam)$
$n_{Ag} = n_{AgNO_3} = 0,06(mol)$
$\Rightarrow m_{dd\ sau\ pư} = 1,92 + 150 - 0,06.108 = 145,44(gam)$
$C\%_{Cu(NO_3)_2} = \dfrac{0,03.188}{145,44}.100\% = 3,88\%$
Đúng 2
Bình luận (0)
Bài 1: Ngâm một lá nhôm có khối lượng 20 gam trong dung dịch đồng (II) sunfat cho tới khi nhôm không thể tan thêm được nữa. Lấy lá nhôm ra, rửa nhẹ, làm khô và cân thì thấy khối lượng là 33,8 g. a. Tính khối lượng nhôm đã phản ứng? b. Tính khối lượng muối thu được.
Ngâm một lá kẽm trong 40 gam dung dịch \(CuSO_4\) 10% cho đến khi kẽm không tan được nữa. Tính khối lượng kẽm đã phản ứng với dd Cu\(SO_4\) và nồng độ phần trăm của dung dịch sau phản ứng
Ta có: \(m_{CuSO_4}=40.10\%=4\left(g\right)\Rightarrow n_{CuSO_4}=\dfrac{4}{160}=0,025\left(mol\right)\)
PT: \(Zn+CuSO_4\rightarrow ZnSO_4+Cu\)
Theo PT: \(n_{Zn}=n_{ZnSO_4}=n_{Cu}=n_{CuSO_4}=0,025\left(mol\right)\)
\(\Rightarrow m_{Zn}=0,025.65=1,625\left(g\right)\)
Ta có: m dd sau pư = 1,625 + 40 - 0,025.64 = 40,025 (g)
\(\Rightarrow C\%_{ZnSO_4}=\dfrac{0,025.161}{40,025}.100\%\approx10,056\%\)
Đúng 2
Bình luận (0)
Ngâm một thanh đồng trong 340 gam dung dịch AgNO3 6%. Sau một thời gian lấy thanh kim loại ra thấy khối lượng AgNO3 trong dung dịch giảm 5,1 gam. Khối lượng đồng tham gia phản ứng là A. 1,92 gam B. 3,24 gam C. 5,1 gam D. 0,96 gam
Đọc tiếp
Ngâm một thanh đồng trong 340 gam dung dịch AgNO3 6%. Sau một thời gian lấy thanh kim loại ra thấy khối lượng AgNO3 trong dung dịch giảm 5,1 gam. Khối lượng đồng tham gia phản ứng là
A. 1,92 gam
B. 3,24 gam
C. 5,1 gam
D. 0,96 gam
Ngâm một thanh đồng trong 340 gam dung dịch AgNO3 6%. Sau một thời gian lấy thanh kim loại ra thấy khối lượng AgNO3 trong dung dịch giảm 5,1 gam. Khối lượng đồng tham gia phản ứng là A. 1,92 gam B. 3,24 gam C. 5,1 gam D. 0,96 gam
Đọc tiếp
Ngâm một thanh đồng trong 340 gam dung dịch AgNO3 6%. Sau một thời gian lấy thanh kim loại ra thấy khối lượng AgNO3 trong dung dịch giảm 5,1 gam. Khối lượng đồng tham gia phản ứng là
A. 1,92 gam
B. 3,24 gam
C. 5,1 gam
D. 0,96 gam
Ngâm thỏi sắt vào 200 gam dung dịch CuSO4 8% cho đến khi sắt không tan được nữa. Tính a/_Khối lượng sắt phản ứng và khối lượng đồng sinh ra b/ Nồng độ % muối trong dung dịch sau phản ứng
\(n_{CuSO_4}=\dfrac{200.8}{100.160}=0,1(mol)\\ PTHH:Fe+CuSO_4\to FeSO_4+Cu\\ a,n_{Cu}=n_{Fe}=n_{CuSO_4}=0,1(mol)\\ \Rightarrow m_{Cu}=0,1.64=6,4(g);m_{Fe}=0,1.56=5,6(g)\\ b,n_{FeSO_4}=0,1(mol)\\ \Rightarrow C\%_{FeSO_4}=\dfrac{0,1.152}{5,6+200-6,4}.100\%=7,63\%\)
Đúng 2
Bình luận (1)
Ngâm lá nhôm vào 241,5 gam dung dịch ZnSO4 10 % cho đến khi nhôm không tan được nữa. Tính: a/ Khối lượng nhôm phản ứng và khối lượng kẽm sinh ra b/ Nồng độ % muối trong dung dịch sau phản ứng
\(m_{ZnSO_4}=\dfrac{241,5.10}{100}=24,15\left(g\right)=>n_{ZnSO_4}=\dfrac{24,15}{161}=0,15\left(mol\right)\)
PTHH: 2Al + 3ZnSO4 --> Al2(SO4)3 + 3Zn
_____0,1<----0,15-------->0,05----->0,15
=> mAl = 0,1.27 = 2,7(g)
=> mZn = 0,15.65=9,75(g)
b) mdd sau pư = 2,7 + 241,5 - 9,75 = 234,45(g)
=> \(C\%\left(Al_2\left(SO_4\right)_3\right)=\dfrac{0,05.342}{234,45}.100\%=7,294\%\)
Đúng 3
Bình luận (1)
Ngâm 1 lá kẽm có khối lượng là 13 gam trong dung dịch CuSO4 10% cho đến khi kẽm không thể tan được nữa
a)viết phương trình hóa học của phản ứng trên ?
b)Tính thể tích chất rắn thu được sau phản ứng ?
c) Tính khối lượng dung dịch CuSO4 đã dùng ?
d)Tính nồng độ phần trăm của dung dịch muối thu được sau phản ứng ?
e)Hoà tan kẽm trên vào 200 ml dung dịch axit HCl 3M tính thể tích khí Hiđro (ở điều kiện tiêu chuẩn) thu được sau phản ứng ?
Giúp mình vs mai mh thi rồi
Đọc tiếp
Ngâm 1 lá kẽm có khối lượng là 13 gam trong dung dịch CuSO4 10% cho đến khi kẽm không thể tan được nữa a)viết phương trình hóa học của phản ứng trên ? b)Tính thể tích chất rắn thu được sau phản ứng ? c) Tính khối lượng dung dịch CuSO4 đã dùng ? d)Tính nồng độ phần trăm của dung dịch muối thu được sau phản ứng ? e)Hoà tan kẽm trên vào 200 ml dung dịch axit HCl 3M tính thể tích khí Hiđro (ở điều kiện tiêu chuẩn) thu được sau phản ứng ? Giúp mình vs mai mh thi rồi