cho 1,3g Zn vào 365g dung dịch HCl 10%
a, Chất nào dư? khối lượng chất dư?
b, tính thể tích khí thoát ra?
c, tính khối lượng dung dịch sau phản ứng? tính C%?
giúp mk vs ạ, mk cần gấp. Cảm ơn!
Cho 13(g) Zn tác dụng với 182,5g) dung dịch Hcl 10% .
a,Chất nào còn dư sau phản ứng?tính khối lượng chất dư ?
b, Tính thể tích khí H2 sinh ra (ĐKTC)?
c, Dung dịch sau phản ứng có những chất tan nào? Tính nồng độ phần trăm của các chất đó?
\(n_{Zn}=\dfrac{13}{65}=0.2\left(mol\right)\)
\(n_{HCl}=\dfrac{182.5\cdot10}{100\cdot36.5}=0.5\left(mol\right)\)
\(Zn+2HCl\rightarrow ZnCl_2+H_2\)
\(0.2......0.4..........0.2........0.2\)
\(n_{HCl\left(dư\right)}=0.5-0.4=0.1\left(mol\right)\)
\(m_{HCl\left(dư\right)}=0.1\cdot36.5=3.65\left(g\right)\)
\(V_{H_2}=0.2\cdot22.4=4.48\left(l\right)\)
\(m_{\text{dung dịch sau phản ứng}}=13+182.5-0.2\cdot2=195.1\left(g\right)\)
\(C\%_{HCl\left(dư\right)}=\dfrac{3.65}{195.1}\cdot100\%=1.87\%\)
\(C\%_{ZnCl_2}=\dfrac{0.2\cdot136}{195.1}\cdot100\%=13.94\%\)
Câu 10: Cho 6,5g Zn tác dụng với dung dịch có chứa 10,95g HCl.
a) Sau phản ứng chất nào còn dư? Tính khối lượng chất dư.
b) Thể tích khí H2( đktc).
c) Để phản ứng xảy ra hoàn toàn phải thêm chất nào ? khối lượng bao nhiêu gam
Cho kim loại kẽm(Zn) tác dụng với 200g axit clohidric sau phản ứng thấy thoát ra 4.48(l) khí H2 (dktc) a)tính khối lượng Zn phả ứng b) Tính nồng độ dung dịch HCl phản ứng c) Khử 24g CuO cho bằng lượng khí H2 nói trên. Chất nào dư. Khối lượng chất dư là bao nhiêu
\(n_{H_2}=\dfrac{4.48}{22.4}=0.2\left(mol\right)\)
\(Zn+2HCl\rightarrow ZnCl_2+H_2\)
\(0.2.......0.4.......................0.2\)
\(m_{Zn}=0.2\cdot65=13\left(g\right)\)
\(C\%_{HCl}=\dfrac{0.4\cdot36.5}{200}\cdot100\%=7.3\%\)
\(n_{CuO}=\dfrac{24}{80}=0.3\left(mol\right)\)
\(CuO+H_2\underrightarrow{^{t^0}}Cu+H_2O\)
\(1..........1\)
\(0.3.........0.2\)
\(LTL:\dfrac{0.3}{1}>\dfrac{0.2}{1}\Rightarrow CuOdư\)
\(m_{CuO\left(dư\right)}=\left(0.3-0.2\right)\cdot64=6.4\left(g\right)\)
Cho 6,5gam Zn tác dụng với 100gam dung dịch HCl 14,6%a, Viết phương trình phản ứng xảy ra. b, Chất nào dư ? Tính thể tích khí thoát ra (ở đktc), khối lượng muối thu đượcc, Tính nồng độ phần trăm của các chất có trong dung dịch sau khi phản ứng kết thúc
\(n_{Zn}=\dfrac{6.5}{65}=0.1\left(mol\right)\)
\(n_{HCl}=\dfrac{100\cdot14.6\%}{36.5}=0.4\left(mol\right)\)
\(Zn+2HCl\rightarrow ZnCl_2+H_2\)
\(1........2\)
\(0.1......0.4\)
\(LTL:\dfrac{0.1}{1}< \dfrac{0.4}{2}\Rightarrow HCldư\)
\(V_{H_2}=0.1\cdot22.4=2.24\left(l\right)\)
\(m_{\text{dung dịch sau phản ứng}}=6.5+100-0.1\cdot2=106.3\left(g\right)\)
\(C\%ZnCl_2=\dfrac{0.1\cdot136}{106.3}\cdot100\%=12.79\%\)
\(C\%HCl\left(dư\right)=\dfrac{\left(0.4-0.2\right)\cdot36.5}{106.3}\cdot100\%=6.87\%\%\)
Cho 19,5g Zn vào dung dịch H2SO4 có nồng độ 10%( Phản ứng đủ) a) Tính thể thích khí H2 thoát ra. b) Tính khối lượng dd H2SO4 10% phản ứng. c) Tính khối lượng muối tạo thành. d) Tính C% chất có trong dung dịch sau phản ứng
Câu 1: Cho 6,5g Zn tác dụng với 200 g dung dịch HCl 14,6%.
a/ Viết phương trình phản ứng xảy ra.
b/ Chất nào còn dư lại sau phản ứng, với khối lượng là bao nhiêu?
c/ Tính thể tích khí Hidro thoát ra ở ĐKTC.
d/ Tính nồng độ phần trăm của các chất có trong dd sau phản ứng.
\(n_{Zn}=\dfrac{6,5}{65}=0,1mol\)
\(m_{HCl}=\dfrac{200\cdot14,6\%}{100\%}=29,2g\Rightarrow n_{HCl}=0,8mol\)
a)\(Zn+2HCl\rightarrow ZnCl_2+H_2\)
0,1 0,8 0 0
0,1 0,2 0,1 0,1
0 0,6 0,1 0,1
b)Chất HCl dư và dư \(m=0,6\cdot36,5=21,9g\)
c)\(V_{H_2}=0,1\cdot22,4=2,24l\)
d)\(m_{H_2}=0,1\cdot2=0,2g\)
\(m_{ZnCl_2}=0,1\cdot136=13,6g\)
\(m_{ddZnCl_2}=6,5+200-0,2=206,3g\)
\(C\%=\dfrac{13,6}{206,3}\cdot100\%=6,59\%\)
a, ta có pt sau : Zn + 2HCl >ZnCl2 + H2 (1)
b, nHCl=\(\dfrac{200\times14,6}{100}=29,2\left(g\right)\)\(\Rightarrow n_{HCl}=\dfrac{29,2}{36,5}=0,8\left(mol\right)\)
Ta có : nZn=\(\dfrac{6,5}{65}=0,1\left(mol\right)\)
Ta có tỉ lệ số mol là : \(\dfrac{n_{Zn}}{1}< \dfrac{n_{HCl}}{2}\left(\dfrac{0,1}{1}< \dfrac{0,8}{2}\right)\)
\(\Rightarrow\) HCl dư , Zn pứ hết
Theo pt : nHClpứ = 2.nZn=2.0,1=0,2(mol)
\(\Rightarrow\)nHCl dư = nHCl bđ - nHCl pứ = 0,8 - 0,2 = 0,6 (mol)
\(\Rightarrow\)mHCl dư=0,6.36,6=21,9 (g)
c,theo pt :nH2=nZn=0,1(mol)
\(\Rightarrow\)VH2=0,1.22,4=2,24(l)
d,Các chất có trong dung dịch sau pứ là: ZnCl2 , HCl dư
mk chịu câu này ![]()
cho 2,5 gam nhôm vào bình chứa 0,5 mol dung dịch axit sunfuric loãng
a,Viết phương trình phản ứng
b,chất nào còn dư sau phản ứng Tính khối lượng chất dư
c,Tính thể tích khí thoát ra ở điều kiện tiêu chuẩn
\(n_{Al}=\dfrac{2,5}{27}=\dfrac{25}{270}=\dfrac{5}{54}\left(mol\right)\\ n_{H_2SO_4}=0,5\left(mol\right)\\ a,2Al+3H_2SO_4\rightarrow Al_2\left(SO_4\right)_3+3H_2\\ b,Vì:\dfrac{\dfrac{5}{54}}{2}< \dfrac{0,5}{4}\Rightarrow H_2SO_4dư\\ b,n_{H_2SO_4\left(dư\right)}=0,5-\dfrac{3}{2}.\dfrac{5}{54}=\dfrac{13}{36}\left(mol\right)\\ \Rightarrow m_{H_2SO_4}=\dfrac{13}{36}.98=\dfrac{637}{18}\left(g\right)\\ c,n_{H_2}=\dfrac{3}{2}.n_{Al}=\dfrac{3}{2}.\dfrac{5}{54}=\dfrac{5}{36}\left(mol\right)\\ \Rightarrow V_{H_2\left(đktc\right)}=\dfrac{5}{36}.22,4=\dfrac{28}{9}\left(l\right)\)
Tóm tắt:
mAl= 2,5(g)
\(n_{H_2SO_4}=0,5\left(mol\right)\)
---
a) PTHH?
b) Chất dư? m?
c) Thể tích khí sau phản ứng?
Anh ít tóm tắt lắm nên không biết tóm tắt như ri ổn không, vì em cần nên anh tóm tắt ra thử
cho 2,5 gam nhôm vào bình chứa 0,25 mol dung dịch axit sunfuric loãng a,Viết phương trình phản ứng b,chất nào còn dư sau phản ứng Tính khối lượng chất dư c,Tính thể tích khí thoát ra ở điều kiện tiêu chuẩn
a: \(2Al+3H_2SO_4\rightarrow Al_2\left(SO_4\right)_3+3H_2\)
b: \(n_{Al}=\dfrac{2.5}{27}< \dfrac{1}{4}\)
=>H2SO4 dư, Al đủ
\(m_{H_2SO_4}=0.25\cdot98=24.5\left(g\right)\)
c: \(n_{Al_2\left(SO_4\right)_3}=\dfrac{2.5}{54}=\dfrac{5}{108}\left(mol\right)\)
\(\Leftrightarrow n_{H_2}=\dfrac{5}{36}\left(mol\right)\)
\(V_{H_2}=\dfrac{5}{36}\cdot22.4=\dfrac{28}{9}\left(lít\right)\)
Mình thấy bạn Thịnh tính lượng dư sai
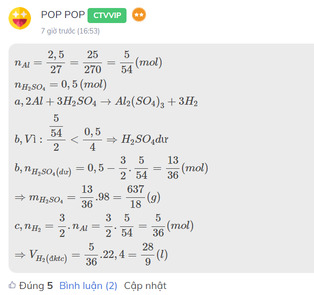
Đây là bài mình từng làm, bạn tham khảo nhé!
Cho 13g kẽm (Zn) vào dung dịch axit clohiđric (HCl) lấy dư, sau phản ứng hoàn toàn.
a, Viết PTHH của phản ứng.
b, Tính thể tích khí H2 (đktc) thoát ra?
c, Nếu cho 13g kẽm (Zn) ở trên vào 200g dung dịch HCl 9.125%, sau phản ứng hoàn toàn, tính khối lượng các chất tan trong dung dịch thu được?
Mk đang cần gấp, các bạn giúp mk vs ạ, camon các bn nhiều.
a, Zn + 2HCl ---> ZnCl2 + H2
b, nZn=\(\dfrac{13}{65}=0,2mol\)
Ta có: 1 mol Zn ---> 1 mol H2
nên 0,2 mol Zn ---> 0,2 mol H2
VH2=0,2.22,4=4,48 mol