Cho kim loại Al phản ứng hết với 100 ml dung dịch HNO3, kết thúc phản ứng thu được 6,72 lít khí N2 (đktc) (sản phẩm khử duy nhất). Viết phương trình phản ứng xảy ra. Tính khối lượng Al phản ứng và nồng độ mol dung dịch HNO3.

Những câu hỏi liên quan
Cho m gam kim loại Fe tan hết trong dung dịch HNO3 25,2%, sau phản ứng hoàn toàn thu được 0,672 lít khí NO (đktc) là sản phẩm khử duy nhất của N trong HNO3. Cô cạn dung dịch sau phản ứng thu được 7,82 gam muỗi khan. Viết phương trình phản ứng xảy ra. Tính giá trị của m và tính nồng độ phần trăm của muối trong dung dịch sau phản ứng
Đọc tiếp
Cho m gam kim loại Fe tan hết trong dung dịch HNO3 25,2%, sau phản ứng hoàn toàn thu được 0,672 lít khí NO (đktc) là sản phẩm khử duy nhất của N trong HNO3. Cô cạn dung dịch sau phản ứng thu được 7,82 gam muỗi khan.
Viết phương trình phản ứng xảy ra. Tính giá trị của m và tính nồng độ phần trăm của muối trong dung dịch sau phản ứng
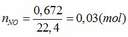
Fe + 4HNO3 → Fe(NO3)3 + NO + 2H2O (1)
a → 4a → a → a (mol)
3Fe + 8HNO3 → 3Fe(NO3)2 + 2NO + 4H2O (2)
B → 8/3b → b →2/3b (mol)
TH1: xảy ra phản ứng (1) tạo muối Fe(NO3)3 => nFe(NO3)3 = nNO = 0,03 (mol)
=> mmuối = mFe(NO3)3 = 0,03. 242 = 7,26 (g) # 7,82 => loại
TH2: xảy ra phản ứng (2) tạo muối Fe(NO3)2 => nFe(NO3)2 = 3/2 nNO = 3/2 . 0,03 = 0,045 (mol)
=> mmuối = mFe(NO3)2 = 0,045. 180 = 8,1 (g) # 7,82 => loại
TH3: xảy ra cả (1) và (2) phản ứng tạo 2 muối.
Gọi số mol của Fe ở phản ứng (1) và (2) lần lượt là a và b (mol)
Đặt vào phương trình ta có:
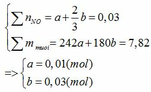
∑ nFe = 0,01 + 0,03 = 0,04 (mol) => mFe = 0,04.56 = 2,24 (g)
∑ nHNO3 pư = 4a + 8/3b = 4. 0,01 + 8/3. 0,03 = 0,12 (mol)
mHNO3 = 0,12.63 = 7,56 (g)
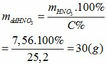
Khối lượng dd sau: mdd sau = mFe + mddHNO3 - mNO = 2,24 + 30 – 0,03.30 = 31,34 (g)
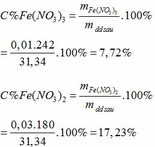
Đúng 1
Bình luận (0)
Cho 14.4 gam hỗn hợp gồm Mg và Al phản ứng vừa đủ với 200,6 gam dung dịch HNO3. Sau phản ứng thu được dd Y và 11,2 lít khí NO(đktc) bay ra.( NO là sản phẩm khử duy nhất)
a) tính % khối lượng kim loại trong hỗn hợp.
b) Tính nồng độ % các chất tan trong dd Y
Cho phản ứng hóa học xảy ra theo phương trình sau: Al + HNO3 ® Al(NO3)3 + N2O + H2O. Sau phản ứng thu được 3,36 (l) khí N2O (đkc) (sản phẩm khử duy nhất). Tính lượng Al và HNO3 đã phản ứng? (theo 2 cách ).
Cách 1:
\(8Al+30HNO_3\rightarrow8Al\left(NO_3\right)_3+3N_2O+15H_2O\\ n_{N_2O}=\dfrac{3,36}{22,4}=0,15\left(mol\right)\\ n_{Al}=\dfrac{8}{3}.0,15=0,4\left(mol\right)\\ m_{Al}=0,4.27=10,8\left(g\right)\\ n_{HNO_3}=\dfrac{30}{3}.0,15=1,5\left(mol\right)\\ m_{HNO_3}=63.1,5=94,5\left(g\right)\\ \)
Cách 2: Làm bằng trao đổi e ấy.
Đúng 1
Bình luận (0)
Nung Al và Fe3O4 (không có không khí, phản ứng xảy ra hoàn toàn) thu được hỗn hợp X. - Nếu cho X phản ứng với dung dịch KOH dư thì thu được 0,672 lít khí (đktc). - Nếu cho X phản ứng với dung dịch H2SO4 đặc, nóng dư được 1,428 lít SO2 (sản phẩm khử duy nhất, đktc). Phần trăm khối lượng Al trong hỗn hợp ban đầu là A. 33,69%. B. 19,88%. C. 38,30%. D. 26,33%.
Đọc tiếp
Nung Al và Fe3O4 (không có không khí, phản ứng xảy ra hoàn toàn) thu được hỗn hợp X.
- Nếu cho X phản ứng với dung dịch KOH dư thì thu được 0,672 lít khí (đktc).
- Nếu cho X phản ứng với dung dịch H2SO4 đặc, nóng dư được 1,428 lít SO2 (sản phẩm khử duy nhất, đktc).
Phần trăm khối lượng Al trong hỗn hợp ban đầu là
A. 33,69%.
B. 19,88%.
C. 38,30%.
D. 26,33%.
Đáp án C
Phản ứng hoàn toàn thu được
sản phẩm + KOH ⇒ H2 ⇒ Al dư.
Ta có phản ứng:
8Al + 3Fe3O4 ![]() 4Al2O3 + 9Fe.
4Al2O3 + 9Fe.
Với nAl dư = 2nH2÷3 = 0,02 mol.
Xem hỗn hợp X gồm: nAl = 0,02
nAl2O3 = a || nFe = b ta có:
PT bảo toàn e với SO2:
3nAl + 3nFe = 2nSO2
Û nFe = b = 0,0225
⇒ nAl2O3 = 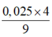 = 0,01.
= 0,01.
Bảo toàn khối lượng
mHỗn hợp ban đầu = mAl + mAl2O3 + mFe
= 2,82 gam.
Bảo toàn nguyên tố Al
⇒ ∑nAl ban đầu = 0,02 + 0,01×2 = 0,04 mol.
⇒ %mAl = 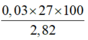
= 38,298%
Đúng 0
Bình luận (0)
Cho 6,72 gam Fe phản ứng với 125 ml dung dịch
H
N
O
3
3,2M thu được dung dịch X và khí NO (sản phẩm khử duy nhất của
N
+
5
). Biết các phản ứng xảy ra hoàn toàn, khối lượng muối trong dung dịch X là A. 21,60 gam B. 25,32 gam C. 29,04 gam D. 24,20 gam
Đọc tiếp
Cho 6,72 gam Fe phản ứng với 125 ml dung dịch H N O 3 3,2M thu được dung dịch X và khí NO (sản phẩm khử duy nhất của N + 5 ). Biết các phản ứng xảy ra hoàn toàn, khối lượng muối trong dung dịch X là
A. 21,60 gam
B. 25,32 gam
C. 29,04 gam
D. 24,20 gam
Câu 1) Cho 11gam hỗn hợp Al,Fe phản ứng hoàn toàn với H2SO4đặc nóng dư thu đc 10,08 lít SO2 sản phẩm khử duy nhất ở điều kiện khuẩn và dung dịch Xa) Viết phương trình phản ứng xảy ra b) TÍnh % theo khối của mỗi kim loại trong hỗn hợpc) Tính khối lượng muối tạo thành trong dung dịch XCâu 2) cho 1,28 gam hỗn hợp Fe và Mg tác dụng vừa đủ với dung dịch H2SO4đặc, nóng thu đc 1,008 lít SO2 ở điều kiện chuẩn a) Viết phương trình phản ứng xảy ra b) Tính % theo khối của mỗi kim loại trong hỗn hợpc) Tính...
Đọc tiếp
Câu 1) Cho 11gam hỗn hợp Al,Fe phản ứng hoàn toàn với H2SO4đặc nóng dư thu đc 10,08 lít SO2 sản phẩm khử duy nhất ở điều kiện khuẩn và dung dịch X
a) Viết phương trình phản ứng xảy ra
b) TÍnh % theo khối của mỗi kim loại trong hỗn hợp
c) Tính khối lượng muối tạo thành trong dung dịch X
Câu 2) cho 1,28 gam hỗn hợp Fe và Mg tác dụng vừa đủ với dung dịch H2SO4đặc, nóng thu đc 1,008 lít SO2 ở điều kiện chuẩn
a) Viết phương trình phản ứng xảy ra
b) Tính % theo khối của mỗi kim loại trong hỗn hợp
c) Tính khối lượng dung dịch H2SO4 80% đã dùng
a)
nSO2=\(\dfrac{10,08}{22,4}\)= 0,45(mol)
2Al + 6H2SO4 --> Al2(SO4)3 + 6H2O +3SO2
x ---------------------------------------------> 3/2x
2Fe + 6H2SO4 --> Fe2(SO4)3 + 6H2O + 3SO2
y --------------------------------------------------> 3/2y
b) ta có hệ pt sau
\(\left\{{}\begin{matrix}27x+56y=11\\\dfrac{3}{2}x+\dfrac{3}{2}y=0,45\end{matrix}\right.\)
\(\left\{{}\begin{matrix}x=0,2\\y=0,1\end{matrix}\right.\)
%mAl = \(\dfrac{0,2.27}{11}.100\)= 49%
%mFe=\(49-100\) =51%
c) m Al2(SO4)3= 0,1.342=34,2 g
mFe2(SO4)3=0,05.400=20 g
Đúng 1
Bình luận (0)
Câu 1. Cho 11 g hỗn hợp Al, Fe phản ứng hoàn toàn với lượng dư dung dịch H,SO4 đặc nóng thu được 11,1555 L SO2 (sản phẩm khử duy nhất, ở đkc ) và dung dịch A. Tính % theo khối lượng của mỗi kim loại trong hỗn hợp.
Đúng 0
Bình luận (0)
Cho 0,87 gam hỗn hợp gồm Fe, Cu, Al vào bình đựng 300 ml dung dịch
H
2
S
O
4
0,1M. Sau khi các phản ứng xảy ra hoàn toàn thu được 0,32 gam chất rắn và có 448 ml khí (đktc) thoát ra. Thêm tiếp vào bình 0,425 gam NaNO3 khi các phản ứng kết thúc thì thể tích khí NO (đktc, sản phẩm khử duy nhất) tạo thành và khối lượng muối trong dung dịch là A. 0,112 lít và 3,750 gam B. 0,224 lít và 3,865 gam C. 0,224 lít và 3,...
Đọc tiếp
Cho 0,87 gam hỗn hợp gồm Fe, Cu, Al vào bình đựng 300 ml dung dịch H 2 S O 4 0,1M. Sau khi các phản ứng xảy ra hoàn toàn thu được 0,32 gam chất rắn và có 448 ml khí (đktc) thoát ra. Thêm tiếp vào bình 0,425 gam NaNO3 khi các phản ứng kết thúc thì thể tích khí NO (đktc, sản phẩm khử duy nhất) tạo thành và khối lượng muối trong dung dịch là
A. 0,112 lít và 3,750 gam
B. 0,224 lít và 3,865 gam
C. 0,224 lít và 3,750 gam
D. 0,112 lít và 3,865 gam
Câu 3. Cho 1 lượng kẽm (Zn) dư tác dụng với 100 ml dung dịch axit HCI, phản ứng kết thúc thu được 6,72 lít khí (đktc).
a) Viết phương trình hóa học xảy ra.
b) Tính khối lượng kẽm đã tham gia phản ứng.
c) Tính nồng độ mol của dung dịch HCl
a, \(Zn+2HCl\rightarrow ZnCl_2+H_2\)
b, \(n_{H_2}=\dfrac{6,72}{22,4}=0,3\left(mol\right)\)
Theo PT: \(n_{Zn}=n_{H_2}=0,3\left(mol\right)\)
\(\Rightarrow m_{Zn}=0,3.65=19,5\left(g\right)\)
c, \(n_{HCl}=2n_{H_2}=0,6\left(mol\right)\)
\(\Rightarrow C_{M_{HCl}}=\dfrac{0,6}{0,1}=6\left(M\right)\)
Đúng 1
Bình luận (0)
Cho 17,4 gam hỗn hợp gồm Fe, Cu, Al vào bình đựng 1 lít dung dịch
H
2
S
O
4
0,6M. Sau khi các phản ứng xảy ra hoàn toàn thu được 6,4 gam chất rắn và có 8,96 lít khí (đktc) thoát ra. Thêm tiếp vào bình 8,5 gam NaNO3 khi các phản ứng kết thúc thì thể tích khí NO (đktc, sản phẩm khử duy nhất) tạo thành và khối lượng muối trong dung dịch là A. 2,24 lít và 77,3 gam B. 6,72 lít và 40,1 gam C. 2,24 lít và 88,1 gam...
Đọc tiếp
Cho 17,4 gam hỗn hợp gồm Fe, Cu, Al vào bình đựng 1 lít dung dịch H 2 S O 4 0,6M. Sau khi các phản ứng xảy ra hoàn toàn thu được 6,4 gam chất rắn và có 8,96 lít khí (đktc) thoát ra. Thêm tiếp vào bình 8,5 gam NaNO3 khi các phản ứng kết thúc thì thể tích khí NO (đktc, sản phẩm khử duy nhất) tạo thành và khối lượng muối trong dung dịch là
A. 2,24 lít và 77,3 gam
B. 6,72 lít và 40,1 gam
C. 2,24 lít và 88,1 gam
D. 11,2 lít và 40,1gam




















