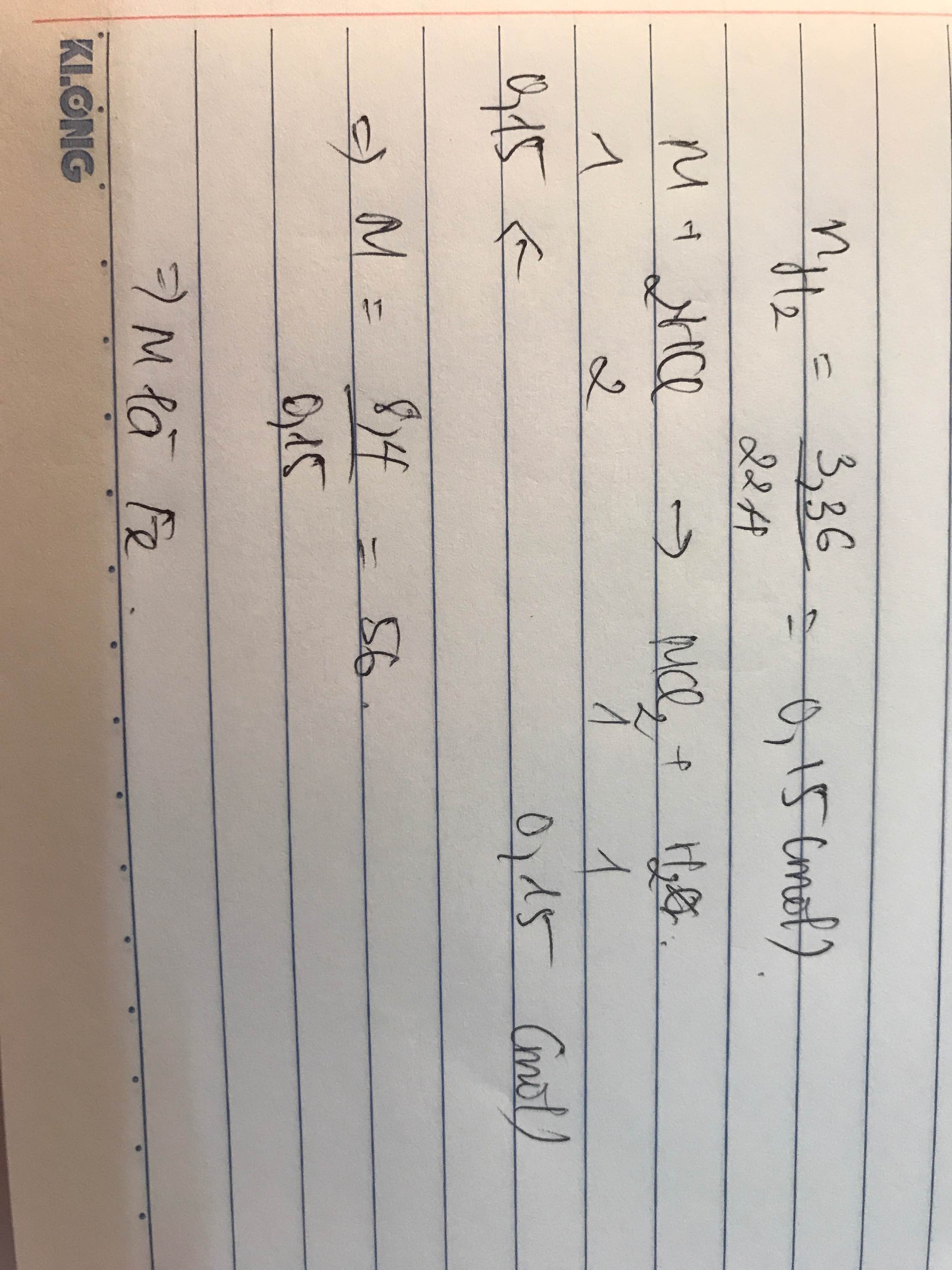Những câu hỏi liên quan
Hòa tan 3,68 g một kim loại kiềm M hòa tan vào nước dư, thu được 1,792 lit khí H, (đktc) và 200 ml dung dịch X. a-Xác định tên kim loại kiểm. b-Tính nồng độ moll của dung dịch X.
Gọi M là khối lượng mol trung bình của 2 nguyên tố
nH2=6.72/22.4=0.3 mol
M + H2O --> MOH + 1/2 H2
0.6mol---------------------0.3mol
-> M=20.2/0.3=67.3333
-->M1<67.33<M2
mà 2 kim loại này thuộc hai chu kì liên tiếp nhau
--> Kim loại đó là KI và Rb
Đúng 1
Bình luận (0)
1. Viết phương trình hóa học và cho biết hiện tượng xảy ra :khi sục khí CO2 vào dung dịch Ca(OH)22. Hòa tan hoàn toàn 2,3 gam một kim loại A nhóm IA vào 200ml nước thu được dung dịch X và 1,12 lít khí (đktc).Xác định tên kim loại A và nồng độ mol/l dung dịch X.3. Hòa tan 3,040 gam hỗn hợp bột sắt và đồng trong dung dịch HNO3 loãng thu được 0,896 lit khí NO ( ở đktc). Xác định thành phần phần trăm về khối lượng của mỗi kim loại trong hỗn hợp
Đọc tiếp
1. Viết phương trình hóa học và cho biết hiện tượng xảy ra :khi sục khí CO2 vào dung dịch Ca(OH)2
2. Hòa tan hoàn toàn 2,3 gam một kim loại A nhóm IA vào 200ml nước thu được dung dịch X và 1,12 lít khí (đktc).Xác định tên kim loại A và nồng độ mol/l dung dịch X.
3. Hòa tan 3,040 gam hỗn hợp bột sắt và đồng trong dung dịch HNO3 loãng thu được 0,896 lit khí NO ( ở đktc). Xác định thành phần phần trăm về khối lượng của mỗi kim loại trong hỗn hợp
Bài 3 :
\(3,040Fe;Cu+HNO3\left(l\right)->\left\{{}\begin{matrix}Fe\left(NO3\right)3\\Cu\left(NO3\right)2\end{matrix}\right.+0,896\left(l\right)NO\)
Gọi Fe là x , Cu là y
Ta có :
nNO = 0,04 ( mol )
Feo - 3e -> Fe+3
x 3x
Cuo - 2e -> Cu+2
y 2y
N+5 + 3e -> N+2
0,12 <- 0,04
n(e) cho = n(e) nhận
Ta có hpt :
\(\left\{{}\begin{matrix}56x+64y=3,040\\3x+2y=0,12\end{matrix}\right.\Leftrightarrow\left\{{}\begin{matrix}x=0,02\left(mol\right)\\y=0,03\left(mol\right)\end{matrix}\right.\)
Xác đinh phần trăm khối lượng trong kim loại :
\(\left\{{}\begin{matrix}\%mFe=\dfrac{56.0,02}{3,04}=36,84\%\\\%mCu=\dfrac{64.0,03}{3,04}=63,15\%\end{matrix}\right.\)
Đúng 2
Bình luận (0)
Hòa tan hoàn toàn 2,3 g một kim loại nhóm 1A vào 57,8 g nước thu được 1,12 lít khí h2 và dung dịch a
a. xác định tên kim loại
b .tính nồng độ phần trăm chất tan trong dung dịch a
a)Gọi A là kim loại cần tìm.
\(n_{H_2}=\dfrac{1,12}{22,4}=0,05mol\)
Ta có PTHH:
\(2A+2H_2O\rightarrow2AOH+H_2\uparrow\)
0,1-----------------0,1--------0,05-----(mol);
Vậy \(M_A=\dfrac{2,3}{0,1}=23\)(g/mol) => A là Na
b) Ta có: \(m_{dd}=2,3+57,8-0,05\cdot2=60g\)
Từ đó suy ra:\(\%C_{NaOH}=\dfrac{0,1\cdot40}{60}\cdot100\%=6,67\%\)
Đúng 1
Bình luận (0)
hòa tan hết 4 g 1 kim loại M vào 96,2 g nước thì thu được dung dịch A có nồng độ 7,4% và V lít khí B ( đktc ) a , Viết PTHH và xác định dung dịch A , khí B b , Xác định kim loại M...
Đọc tiếp
hòa tan hết 4 g 1 kim loại M vào 96,2 g nước thì thu được dung dịch A có nồng độ 7,4% và V lít khí B ( đktc ) a , Viết PTHH và xác định dung dịch A , khí B b , Xác định kim loại M c , Tính V
Hòa tan hoàn toàn a (g) oxit của một Kim loại hóa trị II trong 48g dung dịch H2SO4 lít, nồng độ 6,125% thu được dung dịch chất tan trong đó H2SO4 có nồng độ 0,98%. Mặt khác dùng 2,8 lít CO để khử a (g) oxit trên thành kim loại thu được khí B duy nhất. Nếu lấy 0,896 lít khí B cho vào dung dịch Ca(OH)2 dư thu được 0,8 g kết tủa. tìm giá trị của a và xác định công thức của oxit kim loại đó . Biết các thể tích khí đó cùng đktc
Đọc tiếp
Hòa tan hoàn toàn a (g) oxit của một Kim loại hóa trị II trong 48g dung dịch H2SO4 lít, nồng độ 6,125% thu được dung dịch chất tan trong đó H2SO4 có nồng độ 0,98%. Mặt khác dùng 2,8 lít CO để khử a (g) oxit trên thành kim loại thu được khí B duy nhất. Nếu lấy 0,896 lít khí B cho vào dung dịch Ca(OH)2 dư thu được 0,8 g kết tủa. tìm giá trị của a và xác định công thức của oxit kim loại đó . Biết các thể tích khí đó cùng đktc
Xem thêm câu trả lời
cho 8,4 gam một kim loại M hóa trị II vào dung dịch HCl 10% dư. Sau khi kim loại hòa tan hoàn toàn thu được 3,36 lít khí đo ở đktc và dung dịch A.
a. Xác định kim loại M
b.Để phản ứng hết dung dịch A cần 500ml dung dịch NaOH 1M. Tính nồng độ phần trăm các chất trong dung dịch A
dạ em làm xong câu B rồi mọi người khỏi cần trả lời nữa ạ
Đúng 0
Bình luận (2)
Hòa tan hoàn toàn 4,35 g hỗn hợp gồm kim loại M và oxit của nó vào nước, thu được 500 ml dung dịch chứa 1 chất tan có nồng độ 0,06M và 0,336 lít khí H2 (ở đktc). Xác định kim loại M và oxit của M
Hòa tan hoàn toàn 8 gam một kim loại A nhóm IIA vào 500ml nước thu được dung dịch X và 4,48 lít khí (đktc).
a. Xác định tên kim loại A.
b. Tính nồng độ mol/l dung dịch X
a) \(n_{H_2}=\dfrac{4,48}{22,4}=0,2\left(mol\right)\)
PTHH: A + 2H2O --> A(OH)2 + H2
0,2<--------------0,2<-----0,2
=> \(M_A=\dfrac{8}{0,2}=40\left(g/mol\right)\)
=> A là Ca (Canxi)
b) \(C_M=\dfrac{0,2}{0,5}=0,4M\)
Đúng 5
Bình luận (0)
Hòa tan hết 8,4gam kim loại M vào 80gam dung dịch H2SO4 19,6% sau phản ứng thu được dung dịch X và 3,36 lít khí H2 (đktc)
a) Xác định kim loại M
b) Tính C% của chất tan có trong dung dịch X
a)
\(n_{H_2} = \dfrac{3,36}{22,4} = 0,15(mol)\\ n_{H_2SO_4} = \dfrac{80.19,6\%}{98} = 0,16(mol)\)
Gọi n là hóa trị của kim loại M
\(2M + nH_2SO_4 \to M_2(SO_4)_n + nH_2\)
Theo PTHH :
\(n_M = \dfrac{2}{n}n_{H_2} = \dfrac{0,3}{n}(mol)\\ n_{H_2SO_4\ phản\ ứng} = n_{H_2} = 0,15(mol)\\ \Rightarrow n_{H_2SO_4\ dư} = 0,16-0,15 = 0,01(mol)\)
Ta có : \(M = \dfrac{8,4}{\dfrac{0,3}{n}} = 28n\)
Với n = 2 thì M = 56(Fe)
b)
Sau phản ứng, mdung dịch = 8,4 + 80 - 0,15.2 = 88,1(gam)
\(n_{FeSO_4} = n_{H_2} = 0,15(mol)\)
Vậy :
\(C\%_{FeSO_4} = \dfrac{0,15.152}{88,1}.100\% = 25,88\%\\ C\%_{H_2SO_4} = \dfrac{0,01.98}{88,1}.100\% = 1,11\%\)
Đúng 0
Bình luận (0)