1. Cho 5,4g nhôm vào cốc đựng d.d loãng chứa 30g H2SO4.
a, Sau phản ứng nhôm hay axit còn dư?
b, Tính thể tích H2 thu được ở đkc?
c, Tính khối lượng các chất còn lại trong cốc?
cho 8,1g nhôm vào cốc đựng dung dịch loãng chứa 29,4g H2SO4 a) Sau phản ứng nhôm hay axit còn dư b) tính thể tích H2 thu được ở đktc c) tính khối lượng các chất còn lại trong cốc
\(n_{Al}=\dfrac{8.1}{27}=0.3\left(mol\right)\)
\(n_{H_2SO_4}=\dfrac{29.4}{98}=0.3\left(mol\right)\)
\(2Al+3H_2SO_4\rightarrow Al_2\left(SO_4\right)_3+3H_2\)
\(2.........3\)
\(0.3..........0.3\)
\(LTL:\dfrac{0.3}{2}>\dfrac{0.3}{3}\Rightarrow Aldư\)
\(V_{H_2}=0.3\cdot22.4=6.72\left(l\right)\)
\(m_{Al\left(dư\right)}=\left(0.3-0.2\right)\cdot27=2.7\left(g\right)\)
Bài tập Cho 8,1g nhôm vào cốc đựng dung dịch loãng chứa 29,4g H2SO4.
a) Sau phản ứng nhôm hay axit còn dư ?
b) Tính thể tích H2 thu được ở đktc ?
c) Tính khối lượng các chất còn lại trong cốc ?
BT3. người ta cho 5,4 gam Al vào cốc đựng dung dịch loãng chứa 30 gam H2SO4 . hỏi :
a) sau phản ứng chất nào còn dư?
b) tính thể tích H2 thu đc ở đktc
c) tính khối lượng các chất còn lại trong cốc?
ai bt lm bài này giải giúp mik bài này vs ạ
2Al+3H2SO4->Al2(SO4)3+3H2
0,2-----0,3-------0,1------------0,3
n Al=\(\dfrac{5,4}{27}\)=0,2 mol
n H2SO4= \(\dfrac{30}{98}\)=0,306 mol
=>H2SO4 còn dư
=>VH2=0,3.22,4=6,72l
=>m Al2(SO4)3=0,1.342=34,2g
=>m H2SO4 dư=0,006.98=0,588g
\(n_{Al}=\dfrac{m_{Al}}{M_{Al}}=\dfrac{5,4}{27}=0,2mol\)
\(n_{H_2SO_4}=\dfrac{m_{H_2SO_4}}{M_{H_2SO_4}}=\dfrac{30}{98}=\dfrac{15}{49}mol\)
\(2Al+3H_2SO_4\rightarrow Al_2\left(SO_4\right)_3+3H_2\)
2 3 1 3 ( mol )
0,2 15/49 ( mol )
Ta có: \(\dfrac{0,2}{2}< \dfrac{15}{49}:3\)
=> Chất còn dư là \(H_2SO_4\)
\(V_{H_2}=n_{H_2}.22,4=\left(\dfrac{0,2.3}{2}\right).22,4=6,72l\)
\(m_{Al_2\left(SO_4\right)_3}=n_{Al_2\left(SO_4\right)_3}.M_{Al_2\left(SO_4\right)_3}=\left(\dfrac{0,2.1}{2}\right).342=34,2g\)
\(m_{H_2SO_4\left(du\right)}=n_{H_2SO_4\left(du\right)}.M_{H_2SO_4}=\left(\dfrac{15}{49}-\dfrac{0,2.3}{2}\right).98=0,6g\)
Cho 5,4g nhôm vào dung dịch loãng có chứa 39,2g axit sunfuric . a) Chất nào còn dư sau phản ứng ? Khoiy lượng dư bao nhiêu g ? b) Tính khối lượng muối nhôm sunfat tạo thành. c) Tính thể tích không khí cần dùng để đốt cháy hoàn toàn thể tích khí hiđro trên ( biết thể tích oxi chiếm 20% thể tichy không khí ) . ( Các thể tích khối đo ở đktc ) Biết Al=27, H=1, O=16, S=32, Na=23
a.b.\(n_{Al}=\dfrac{5,4}{27}=0,2mol\)
\(n_{H_2SO_4}=\dfrac{39,2}{98}=0,4mol\)
\(2Al+3H_2SO_4\rightarrow Al_2\left(SO_4\right)_3+3H_2\)
Xét: \(\dfrac{0,2}{2}\) < \(\dfrac{0,4}{3}\) ( mol )
0,2 0,3 0,1 0,3 ( mol )
\(m_{H_2SO_4\left(dư\right)}=\left(0,4-0,3\right).98=9,8g\)
\(m_{Al_2\left(SO_4\right)_3}=0,1.342=34,2g\)
c.\(2H_2+O_2\rightarrow\left(t^o\right)2H_2O\)
0,3 0,15 ( mol )
\(V_{kk}=V_{O_2}.5=\left(0,15.22,4\right).5=16,8l\)
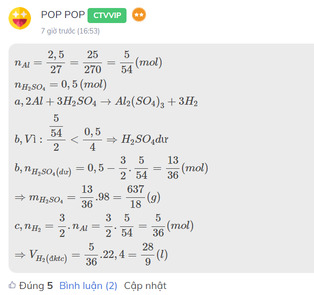
cho 2,5 gam nhôm vào bình chứa 0,5 mol dung dịch axit sunfuric loãng
a,Viết phương trình phản ứng
b,chất nào còn dư sau phản ứng Tính khối lượng chất dư
c,Tính thể tích khí thoát ra ở điều kiện tiêu chuẩn
\(n_{Al}=\dfrac{2,5}{27}=\dfrac{25}{270}=\dfrac{5}{54}\left(mol\right)\\ n_{H_2SO_4}=0,5\left(mol\right)\\ a,2Al+3H_2SO_4\rightarrow Al_2\left(SO_4\right)_3+3H_2\\ b,Vì:\dfrac{\dfrac{5}{54}}{2}< \dfrac{0,5}{4}\Rightarrow H_2SO_4dư\\ b,n_{H_2SO_4\left(dư\right)}=0,5-\dfrac{3}{2}.\dfrac{5}{54}=\dfrac{13}{36}\left(mol\right)\\ \Rightarrow m_{H_2SO_4}=\dfrac{13}{36}.98=\dfrac{637}{18}\left(g\right)\\ c,n_{H_2}=\dfrac{3}{2}.n_{Al}=\dfrac{3}{2}.\dfrac{5}{54}=\dfrac{5}{36}\left(mol\right)\\ \Rightarrow V_{H_2\left(đktc\right)}=\dfrac{5}{36}.22,4=\dfrac{28}{9}\left(l\right)\)
Tóm tắt:
mAl= 2,5(g)
\(n_{H_2SO_4}=0,5\left(mol\right)\)
---
a) PTHH?
b) Chất dư? m?
c) Thể tích khí sau phản ứng?
Anh ít tóm tắt lắm nên không biết tóm tắt như ri ổn không, vì em cần nên anh tóm tắt ra thử
cho 2,5 gam nhôm vào bình chứa 0,25 mol dung dịch axit sunfuric loãng a,Viết phương trình phản ứng b,chất nào còn dư sau phản ứng Tính khối lượng chất dư c,Tính thể tích khí thoát ra ở điều kiện tiêu chuẩn
a: \(2Al+3H_2SO_4\rightarrow Al_2\left(SO_4\right)_3+3H_2\)
b: \(n_{Al}=\dfrac{2.5}{27}< \dfrac{1}{4}\)
=>H2SO4 dư, Al đủ
\(m_{H_2SO_4}=0.25\cdot98=24.5\left(g\right)\)
c: \(n_{Al_2\left(SO_4\right)_3}=\dfrac{2.5}{54}=\dfrac{5}{108}\left(mol\right)\)
\(\Leftrightarrow n_{H_2}=\dfrac{5}{36}\left(mol\right)\)
\(V_{H_2}=\dfrac{5}{36}\cdot22.4=\dfrac{28}{9}\left(lít\right)\)
Mình thấy bạn Thịnh tính lượng dư sai
Đây là bài mình từng làm, bạn tham khảo nhé!
a. Cho hỗn hợp A gồm các kim loại đồng và nhôm vào cốc chứa một lượng dư dung dịch HCl, sau phản ứng thu được 20,16 lít khí H2 (đktc) còn 6,4 g chất rắn không tan.Tính % khối lượng của nhôm trong hỗn hợp? b. Cho hỗn hợp đồng và nhôm đó vào dung dịch H2SO4 đặc, nguội, dư thu được V lít SO2 đktc. Tính V? Câu 2:Cho 5,5 gam hỗn hợp gồm Al và Fe tác dụng với 200 gam dung dịch H2SO4 loãng dư. Sau phản ứng thu
giúp mik vs ạ,mik cảm ơn nhiu
Bài 1:
Cho sơ đồ phản ứng sau: Mg + HCl ->MgCl2 + H2
Nếu cho 2,4g Mg tác dụng với 3,65g HCl. Chất nào còn dư sau phản ứng? Tính khối lượng còn dư? Tính khối lượng MgCl2 tạo thành và thể tích khí H2 thu được (đktc)
Bài 2:
Cho sơ đồ phản ứng sau: Al + H2SO4 -> Al2(SO4)3 + H2
Nếu có 5,4g nhôm tác dụng với 14,7g H2SO4. Chất nào còn dư sau phản ứng? Tính khối lượng còn dư? Tính khối lượng Al2(SO4)3 tạo thành và thể tích khí H2 thu được (đktc)
Bài 3:
Hòa tan hoàn toàn 3,78g với kim loại M (hóa trị III) vào dung dịch HCl thu được 4,704l khí H2 (đktc). Xác định kim loại M?
Bài 4:
Cho sơ đồ phản ứng sau: KMnO4 -> ..........+...........+O2
Tính thể tích Oxi (đktc) thu được khi nhiệt phân hủy hoàn toàn 0,4 mol KMnO4
Đốt cháy 6,2g photpho trong bình chứa lượng Oxi ở trên. Tính khối lượng điphotpho pentaoxit?
bạn từng câu lên sẽ dễ nhìn hơn
PTHH: \(2Al+3H_2SO_4\rightarrow Al_2\left(SO_4\right)_3+3H_2\uparrow\)
Làm gộp các phần còn lại
Ta có: \(n_{Al}=\dfrac{5,4}{27}=0,2\left(mol\right)\) \(\Rightarrow\left\{{}\begin{matrix}n_{Al_2\left(SO_4\right)_3}=0,1mol\\n_{H_2SO_4}=n_{H_2}=0,3mol\end{matrix}\right.\)
\(\Rightarrow\left\{{}\begin{matrix}V_{H_2}=0,3\cdot22,4=6,72\left(l\right)\\m_{Al_2\left(SO_4\right)_3}=0,1\cdot342=34,2\left(g\right)\\m_{H_2SO_4}=0,3\cdot98=29,4\left(g\right)\end{matrix}\right.\)