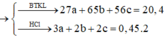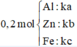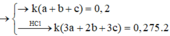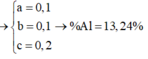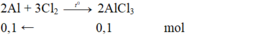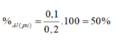Những câu hỏi liên quan
cho Fe tác dụng vừa đủ với dung dịch HCl phản ứng kết thúc thu được 8.96 lít khí H2 đktc
viết PTPU
tính khối lượng Fe tham gia phản ứng
tính khối lượng FeCl2 tạo thành
\(Fe + 2HCl \to FeCl_2 + H_2\\ n_{Fe} = n_{FeCl_2} = n_{H_2} = \dfrac{8,96}{22,4} = 0,4(mol)\\ m_{Fe} = 0,4.56 = 22,4(gam)\\ m_{FeCl_2} = 0,4.127 = 50,8(gam)\)
Đúng 0
Bình luận (0)
\(n_{H_2}=\dfrac{8.96}{22.4}=0.4\left(mol\right)\)
\(Fe+2HCl\rightarrow FeCl_2+H_2\)
\(n_{Fe}=n_{FeCl_2}=n_{H_2}=0.4\left(mol\right)\)
\(m_{Fe}=0.4\cdot56=22.4\left(g\right)\)
\(m_{FeCl_2}=0.4\cdot127=50.8\left(g\right)\)
Đúng 0
Bình luận (0)
a) PTHH : Fe + 2HCl → FeCl2 + H2
b) VH2(đktc)=8,96(l) → nH2= \(\dfrac{8,96}{22,4}\)=0,4(mol)
→ nFe= 0,4(mol)
mFe= 0,4 . 56=22,4(g)
c) Ta có : nH2= \(\dfrac{8,96}{22,4}\)=0,4(mol) → nFeCl2= 0,4(mol)
mFeCl2= 0,4 . 127=50,8(g)
Đúng 0
Bình luận (0)
cho 9.6g kim loại r thuộc nhóm 2a tác dụng với hcl dư tạo ra 8.96 lít khí h2 . tìm kim loại r
Xem chi tiết
Do R thuộc nhóm IIA nên R có hóa trị II.
PT: \(R+2HCl\rightarrow RCl_2+H_2\)
Ta có: \(n_{H_2}=\dfrac{8,96}{22,4}=0,4\left(mol\right)\)
Theo PT: \(n_R=n_{H_2}=0,4\left(mol\right)\)
\(\Rightarrow M_R=\dfrac{9,6}{0,4}=24\left(g/mol\right)\)
Vậy: R là Magie (Mg).
Bạn tham khảo nhé!
Đúng 2
Bình luận (0)
Cho 8,96 lít khí Cl2 (đkc) tác dụng với H2 lấy dư. Tính kg HCl tạo ra biết hiệu suất pư là 75%
8,96l Cl2 + H2 ---H=75%---> 2HCl
0,4............................................0,8
V Hcl lí thuyết : 0,8 . 22,4 = 17,92 (l)
V HCl thực tế : 17,92 . 75% = 13,44 (l)
Đúng 1
Bình luận (0)
\(n_{Cl_2}=\dfrac{8,96}{22,4}=0,25\left(mol\right)\)
PT: Cl2 + H2 → 2HCl
Mol: 0,25 0,5
\(m_{HCl\left(lt\right)}=0,5.36,5=18,25\left(g\right)\)
\(\Rightarrow m_{HCl\left(tt\right)}=75\%.18,25=13,6875\left(g\right)\)
Đúng 1
Bình luận (0)
Cl2+H2-to>2HCl
0,4------------0,8 mol
n Cl2=\(\dfrac{8,96}{22,4}\)=0,4 mol
m HCl pứ =\(\dfrac{0,8.36,5.75}{100}\)=21,9kg
Đúng 1
Bình luận (0)
Hỗn hợp X gồm Fe và Cu-Nếu cho m gam X tác dụng với HCl dư kết thúc thu được 2,24 lít khí H2 (đktc).-Nếu cho m gam X tác dụng với Cl2 thì hết 6,72 lít khí Cl2 (đktc).a) Viết các PTHH.b) Tính thành phần % các kim loại trong X.***Nhân tiện có bạn nào hiểu cách xác định chất nào đứng trước chất nào đứng sau trong dãy hoạt động hóa học của kim loại thì giải thích cho mình với được không ạ??Gần thi cử đến nơi mà học chẳng hiểu...
Đọc tiếp
Hỗn hợp X gồm Fe và Cu
-Nếu cho m gam X tác dụng với HCl dư kết thúc thu được 2,24 lít khí H2 (đktc).
-Nếu cho m gam X tác dụng với Cl2 thì hết 6,72 lít khí Cl2 (đktc).
a) Viết các PTHH.
b) Tính thành phần % các kim loại trong X.
***Nhân tiện có bạn nào hiểu cách xác định chất nào đứng trước chất nào đứng sau trong dãy hoạt động hóa học của kim loại thì giải thích cho mình với được không ạ??Gần thi cử đến nơi mà học chẳng hiểu...
a) PTHH : \(Fe+2HCl-t^o->FeCl_2+H_2\) (1)
\(2Fe+3Cl_2-t^o->2FeCl_3\) (2)
\(Cu+Cl_2-t^o->CuCl_2\) (3)
b) Theo pthh (1) : \(n_{Fe}=n_{H2}=\dfrac{2,24}{22,4}=0,1\left(mol\right)\)
\(\Rightarrow m_{Fe}=0,1.56=5,6\left(g\right)\)
Theo pthh (2) và (3) : \(\Sigma n_{Cl2}=\dfrac{3}{2}n_{Fe}+n_{Cu}\)
\(\Rightarrow\dfrac{6,72}{22,4}=\dfrac{3}{2}.0,1+n_{Cu}\)
\(\Rightarrow0,3=0,15+n_{Cu}\)
\(\Rightarrow n_{Cu}=0,15\left(mol\right)\)
\(\Rightarrow m_{Cu}=0,15.64=9,6\left(g\right)\)
\(\Rightarrow\left\{{}\begin{matrix}\%m_{Fe}=\dfrac{5,6}{5,6+9,6}\cdot100\%\approx36,84\%\\\%m_{Cu}=100\%-36,84\%=63,16\%\end{matrix}\right.\)
Đúng 0
Bình luận (0)
Cho m gam Fe2O3 tác dụng vừa đủ với V lít khí H2(đktc). Toàn bộ lượng kim loại tạo thành tác dụng vừa đủ với dd HCl thu được V' lít khí H2(đktc). Tính tỉ lệ V/V'
$Fe_2O_3+3H_2\rightarrow 2Fe+3H_2O$
$Fe+2HCl\rightarrow FeCl_2+H_2$
Gọi số mol Fe2O3 là a
Ta có: $n_{H_2/(1)}=3a(mol);n_{H_2/(2)}=2a(mol)$
\(\Rightarrow\dfrac{V}{V'}=\dfrac{n_{H_2\left(1\right)}}{n_{H_2\left(2\right)}}=\dfrac{3}{2}\)
Đúng 2
Bình luận (0)
cho 5,4g al tác dụng với 8.96 lít khí clo (đktc) . Khối lượng muối tạo thành sau phản ứng bằng ?
\(n_{Al}=\dfrac{m_{Al}}{M_{Al}}=\dfrac{5,4}{27}=0,2\left(mol\right)\\ n_{Cl_2}=\dfrac{V_{Cl_2\left(ĐKTC\right)}}{22,4}=\dfrac{8,96}{22,4}=0,4\left(mol\right)\\ PTHH:2Al+3Cl_2\rightarrow2AlCl_3\\ \dfrac{n_{Al}}{n_{Cl_2}}=\dfrac{1}{2}< \dfrac{2}{3}\Rightarrow Cl_2\text{ dư, bài toán tính theo }Al\\ \Rightarrow m_{AlCl_3}=n_{AlCl_3}\cdot M_{AlCl_3}=0,2\cdot133,5=26,7\left(g\right)\)
Đúng 1
Bình luận (0)
Cho 20,4 gam hỗn hợp A gồm Al, Zn và Fe tác dụng với dung dịch HCl dư, thu được 10,08 lít H2. Mặt khác 0,2 mol A tác dụng vừa đủ với 6,16 lít Cl2. Tính thành phần phần % về khối lượng của Al trong hỗn hợp A (biết khí đo được ở đktc) A.26,47% B. 19,85% C.33,09% D.13,24%
Đọc tiếp
Cho 20,4 gam hỗn hợp A gồm Al, Zn và Fe tác dụng với dung dịch HCl dư, thu được 10,08 lít H2. Mặt khác 0,2 mol A tác dụng vừa đủ với 6,16 lít Cl2. Tính thành phần phần % về khối lượng của Al trong hỗn hợp A (biết khí đo được ở đktc)
A.26,47%
B. 19,85%
C.33,09%
D.13,24%
Chia 43,4 gam hỗn hợp X gồm fe, zn, cu thành hai phần bằng nhau. Phần 1 tác dụng hoàn toàn với dd hcl dư thu được 4,48 lít khí h2 ( đktc ). Mặt khác, cho phần 2 phản ứng vừa đủ với 8,96 lít khí Cl2 ( đktc ). Tính khối lượng mỗi kim loại trong hỗn hợp X
Rắc bột nhôm đun nóng vào lọ chứa khí C l 2 thu được 0,1 mol muối và Al còn dư. Hỗn hợp sau phản ứng cho tác dụng với dung dịch HCl (dư) thấy có tạo ra 3,36 lít khí H 2 (đktc). Xác định tỉ lệ % lượng Al tác dụng với clo so với lượng Al ban đầu