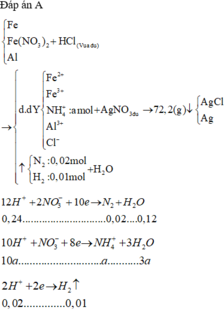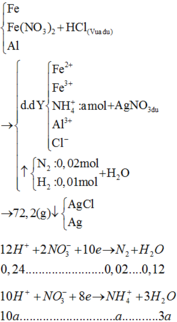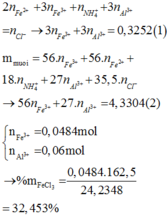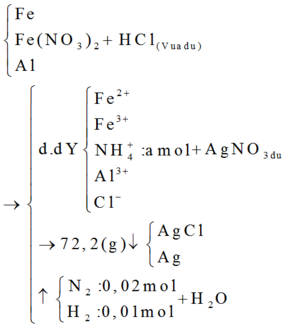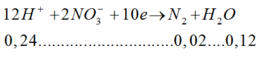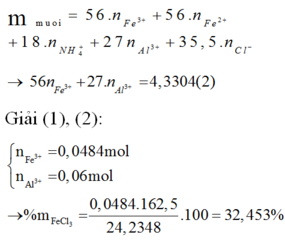Những câu hỏi liên quan
Hoà tan hoàn toàn 5,5 gam hỗn hợp X gồm 2 kim loại Al và Fe cần vừa đủ V lít dung dịch HCl 1M, sau phản ứng thu được 4,48 lít khí H2 ( ở đktc) và dung dịch Y, cô cnaj Y thu được m gam muối khan.a) TÍnh % theo khối lượn các kim loại có trong Xb) Tính các giá trị V và mc) Lấy 1/5 dung dịch Y cho tác dụng với lượng AgNO3 dư thu được bao nhiêu gam chất kết tủa? Biết cá phản ứng đều xảy ra hoàn toàn
Đọc tiếp
Hoà tan hoàn toàn 5,5 gam hỗn hợp X gồm 2 kim loại Al và Fe cần vừa đủ V lít dung dịch HCl 1M, sau phản ứng thu được 4,48 lít khí H2 ( ở đktc) và dung dịch Y, cô cnaj Y thu được m gam muối khan.
a) TÍnh % theo khối lượn các kim loại có trong X
b) Tính các giá trị V và m
c) Lấy 1/5 dung dịch Y cho tác dụng với lượng AgNO3 dư thu được bao nhiêu gam chất kết tủa? Biết cá phản ứng đều xảy ra hoàn toàn
Hoà tan hoàn toàn 11 gam hỗn hợp X gồm Al và Fe bằng dung dịch axit sunfuric loãng dư. Sau khi phản ứng phản ứng kết thúc thu được 8,96 lít khí (đktc).
a) Tính thành phần phần trăm về khối lượng mỗi kim loại trong hỗn hợp X.
b) Tính khối lượng muối khan thu được.
c) Lượng khí hiđro ở trên khử vừa đủ 23,2 gam oxit của kim loại M. Xác định CTHH của oxit đó.
Gọi x,y lần lượt là số mol của Al, Fe
nH2 = \(\dfrac{8,96}{22,4}\)=0,4 mol
Pt: 2Al + 3H2SO4 --> Al2(SO4)3 + 3H2
......x.................................0,5x...........1,5x
.....Fe + H2SO4 --> FeSO4 + H2
.......y..........................y............y
Ta có hệ pt:
{27x+56y=11
1,5x+y=0,4
⇔x=0,2, y=0,1
% mAl = \(\dfrac{0,2.27}{11}\).100%=49,1%
% mFe = \(\dfrac{0,1.56}{11}\).100%=50,9%
mAl2(SO4)3 = 0,5x . 342 = 0,5 . 0,2 . 342 = 34,2 (g)
mFeSO4 = 152y = 152 . 0,1 = 15,2 (g)
Gọi CTTQ: MxOy
Pt: MxOy + yH2 --to--> xM + yH2O
\(\dfrac{0,4}{y}\)<-------0,4
Ta có: 232,2=\(\dfrac{0,4}{y}\)(56x+16y)
⇔23,2=\(\dfrac{22,4x}{y}\)+6,4
⇔\(\dfrac{22,4x}{y}\)=16,8
⇔22,4x=16,8y
⇔x:y=3:4
Vậy CTHH của oxit: Fe3O4
Đúng 1
Bình luận (0)
Hòa tan hoàn toàn 8,975 gam hỗn hợp gồm Al, Fe và Zn vào một lượng vừa đủ dung dịch H2SO4 loãng . Sau phản ứng thu được V lít khí H2 (đktc) và dung dịch X. Cô cạn dung dịch X thu được 32,975 gam muối khan. Vậy giá trị của V là A. 6,72 B. 5,6 C. 11,2 D. 4,48
Đọc tiếp
Hòa tan hoàn toàn 8,975 gam hỗn hợp gồm Al, Fe và Zn vào một lượng vừa đủ dung dịch H2SO4 loãng . Sau phản ứng thu được V lít khí H2 (đktc) và dung dịch X. Cô cạn dung dịch X thu được 32,975 gam muối khan. Vậy giá trị của V là
A. 6,72
B. 5,6
C. 11,2
D. 4,48
Đáp án B
Đặt nH2 = x => nH2SO4 = x
BTKL: mKL + mH2SO4 = m muối + mH2
8,975 + 98x = 32,975 + 2x => x = 0,25 mol
=> V = 5,6 lít
Đúng 0
Bình luận (0)
Hòa tan hoàn toàn 8,975 gam hỗn hợp gồm Al, Fe và Zn vào một lượng vừa đủ dung dịch H2SO4 loãng . Sau phản ứng thu được V lít khí H2 (đktc) và dung dịch X. Cô cạn dung dịch X thu được 32,975 gam muối khan. Vậy giá trị của V là
A. 6,72 .
B. 5,6.
C. 11,2.
D. 4,48.
Đáp án B
Đặt nH2 = x => nH2SO4 = x
BTKL: mKL + mH2SO4 = m muối + mH2
8,975 + 98x = 32,975 + 2x => x = 0,25 mol
=> V = 5,6 lít
Đúng 0
Bình luận (0)
Hòa tan hoàn toàn 8,975 gam hỗn hợp gồm Al, Fe và Zn vào một lượng vừa đủ dung dịch H2SO4 loãng . Sau phản ứng thu được V lít khí H2 (đktc) và dung dịch X. Cô cạn dung dịch X thu được 32,975 gam muối khan. Vậy giá trị của V là A. 6,72 . B. 5,6. C. 11,2. D. 4,48.
Đọc tiếp
Hòa tan hoàn toàn 8,975 gam hỗn hợp gồm Al, Fe và Zn vào một lượng vừa đủ dung dịch H2SO4 loãng . Sau phản ứng thu được V lít khí H2 (đktc) và dung dịch X. Cô cạn dung dịch X thu được 32,975 gam muối khan. Vậy giá trị của V là
A. 6,72 .
B. 5,6.
C. 11,2.
D. 4,48.
Đáp án B
Đặt nH2 = x => nH2SO4 = x
BTKL: mKL + mH2SO4 = m muối + mH2
8,975 + 98x = 32,975 + 2x => x = 0,25 mol
=> V = 5,6 lít
Đúng 0
Bình luận (0)
Hoà tan hoàn toàn 11,2648 gam hỗn hợp X gồm Fe, Fe(NO3)2 và Al vào dung dịch HCl vừa đủ. Sau phản ứng hoàn toàn, thu được dung dịch Y có chứa 24,2348 gam muối và thoát ra 0,672 lít hỗn hợp khí Z (dZ/H2 29/3) gồm 2 khí không màu, đều nhẹ hơn không khí. Cho dung dịch Y tác dụng với dung dịch AgNO3 dư thì thu được 72,2092 gam kết tủa. % khối lượng muối FeCl3 trong hỗn hợp muối là A. 32,453% B. 52,636% C. 33,526% D. 67,453
Đọc tiếp
Hoà tan hoàn toàn 11,2648 gam hỗn hợp X gồm Fe, Fe(NO3)2 và Al vào dung dịch HCl vừa đủ. Sau phản ứng hoàn toàn, thu được dung dịch Y có chứa 24,2348 gam muối và thoát ra 0,672 lít hỗn hợp khí Z (dZ/H2 = 29/3) gồm 2 khí không màu, đều nhẹ hơn không khí. Cho dung dịch Y tác dụng với dung dịch AgNO3 dư thì thu được 72,2092 gam kết tủa. % khối lượng muối FeCl3 trong hỗn hợp muối là
A. 32,453%
B. 52,636%
C. 33,526%
D. 67,453
Hoà tan hoàn toàn 11,2648 gam hỗn hợp X gồm Fe, Fe(NO3)2 và Al vào dung dịch HCl vừa đủ. Sau phản ứng hoàn toàn, thu được dung dịch Y có chứa 24,2348 gam muối và thoát ra 0,672 lít hỗn hợp khí Z (dZ/H2 29/3) gồm 2 khí không màu, đều nhẹ hơn không khí. Cho dung dịch Y tác dụng với dung dịch AgNO3 dư thì thu được 72,2092 gam kết tủa. % khối lượng muối FeCl3 trong hỗn hợp muối là A. 32,453% B. 52,636% C. 33,526% D. 35,247%
Đọc tiếp
Hoà tan hoàn toàn 11,2648 gam hỗn hợp X gồm Fe, Fe(NO3)2 và Al vào dung dịch HCl vừa đủ. Sau phản ứng hoàn toàn, thu được dung dịch Y có chứa 24,2348 gam muối và thoát ra 0,672 lít hỗn hợp khí Z (dZ/H2 = 29/3) gồm 2 khí không màu, đều nhẹ hơn không khí. Cho dung dịch Y tác dụng với dung dịch AgNO3 dư thì thu được 72,2092 gam kết tủa. % khối lượng muối FeCl3 trong hỗn hợp muối là
A. 32,453%
B. 52,636%
C. 33,526%
D. 35,247%
Hoà tan hoàn toàn 57,6 gam hỗn hợp X gồm ,
Fe
2
O
3
, FeO và Fe trong dung dịch HCl thì cần dùng 360 gam dung dịch HCl 18,25% để tác dụng vừa đủ. Sau phản ứng thu được V lít khí
H
2
và dung dịch Y.Cho toàn bộ
H
2
sinh ra tác dụng hết với CuO dư ở nhiệt độ cao, sau phản ứn...
Đọc tiếp
Hoà tan hoàn toàn 57,6 gam hỗn hợp X gồm , Fe 2 O 3 , FeO và Fe trong dung dịch HCl thì cần dùng 360 gam dung dịch HCl 18,25% để tác dụng vừa đủ. Sau phản ứng thu được V lít khí H 2 và dung dịch Y.
Cho toàn bộ H 2 sinh ra tác dụng hết với CuO dư ở nhiệt độ cao, sau phản ứng thu được hỗn hợp rắn gồm Cu và CuO có khối lượng nhỏ hơn khối lượng CuO ban đầu là 3,2 gam. Nếu cô cạn dung dịch Y thì thu được bao nhiêu gam muối khan ?
n HCl = 360 x 18,25/(100x36,5) = 1,8 mol
H 2 + CuO → t ° Cu + H 2 O
n CuO = x
Theo đề bài
m CuO (dư) + m Cu = m CuO (dư) + m Cu p / u - 3,2
m Cu = m Cu p / u - 3,2 => 64x = 80x - 3,2
=> x= 0,2 mol → m H 2 = 0,4g
Fe + 2HCl → FeCl 2 + H 2
Số mol HCl tác dụng với Fe 3 O 4 , Fe 2 O 3 , FeO là 1,8 - 0,4 = 1,4 mol
Phương trình hóa học của phản ứng:
Fe 3 O 4 + 8HCl → 2 FeCl 3 + FeCl 2 + 4 H 2 O (1)
Fe 2 O 3 + 6HCl → 2 FeCl 3 + 3 H 2 O (2)
FeO + 2HCl → FeCl 2 + H 2 O (3)
Qua các phản ứng (1), (2), (3) ta nhận thấy n H 2 O = 1/2 n HCl = 1,4:2 = 0,7 mol
Áp dụng định luật bảo toàn khối lượng, ta có:
m hỗn hợp + m HCl = m muối + m H 2 O + m H 2
57,6 + 1,8 x 36,5 = m muối + 0,7 x 18 +0,4
m muối = 57,6 + 65,7 - 12,6 - 0,4 = 110,3 (gam)
Đúng 1
Bình luận (0)
Hoà tan hoàn toàn 11,2648 gam hỗn hợp X gồm Fe,
F
e
N
O
3
2
và Al vào dung dịch HCl vừa đủ. Sau phản ứng hoàn toàn, thu được dung dịch Y có chứa 24,2348 gam muối và thoát ra 0,672 lít hỗn hợp khí Z (
d
z
/
H
2
29/3) gồm...
Đọc tiếp
Hoà tan hoàn toàn 11,2648 gam hỗn hợp X gồm Fe, F e N O 3 2 và Al vào dung dịch HCl vừa đủ. Sau phản ứng hoàn toàn, thu được dung dịch Y có chứa 24,2348 gam muối và thoát ra 0,672 lít hỗn hợp khí Z ( d z / H 2 = 29/3) gồm 2 khí không màu, đều nhẹ hơn không khí. Cho dung dịch Y tác dụng với dung dịch A g N O 3 dư thì thu được 72,2092 gam kết tủa. % khối lượng muối F e C l 3 trong hỗn hợp muối là
![]()
![]()
![]()
![]()