hòa tan hoàn toàn 11,2 gam kim loại M vào dung dịch HNO3 thu được 4,48 lít khí NO . xác định kim lọai M

Những câu hỏi liên quan
Hòa tan hoàn toàn 9,2 gam kim loại kiềm M vào nước thu được dung dịch A và 4,48 lít khí H2 (đktc) Xác định tên kim loại
Xem chi tiết
\(2M+2H_2O\rightarrow2MOH+H_2\)
0,4 mol \(\leftarrow\) 0,2 mol
Khối lượng mol của \(M\) là:
\(M=\dfrac{m}{n}=\dfrac{9,2}{0,4}=23\)
Vậy \(M\) là kim loại \(Na\)
Đúng 2
Bình luận (0)
Hòa tan hoàn toàn 15,2 gam hỗn hợp gồm Fe và Cu trong dung dịch HNO3, thu được dung dịch X và 4,48 lút khí NO. Cho 3,96 gam kim loại Mg vào X đến khi phản ứng xảy ra hoàn toàn, thu được 224ml khí NO và m gam chất rắn không tan. biết NO là sản phẩm khử duy nhất của N+5. Gía trị cảu m là
A. 6,4 B.12,8 C.9,6 D.4,8
Hòa tan hoàn toàn 15,2 gam hỗn hợp gồm Fe và Cu trong dung dịch HNO3, thu được dung dịch X và 4,48 lút khí NO. Cho 3,96 gam kim loại Mg vào X đến khi phản ứng xảy ra hoàn toàn, thu được 224ml khí NO và m gam chất rắn không tan. biết NO là sản phẩm khử duy nhất của N+5. Gía trị cảu m là
A. 6,4 B.12,8 C.9,6 D.4,8
Đúng 2
Bình luận (0)
Hoà tan hoàn toàn 19,2 gam một kim loại M trong dung dịch HNO 3 ta thu được 4,48 lít NO (đktc). Kim loại M là
A. Zn (M = 65).
B. Fe (M = 56).
C. Mg (M = 24).
D. Cu (M = 64).
Chọn D
Bảo toàn electron có: 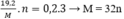 (Với n là số electron nhường)
(Với n là số electron nhường)
Vậy n = 2; M = 64 thỏa mãn. Kim loại cần tìm là Cu.
Đúng 0
Bình luận (0)
Hòa tan hoàn toàn 11,2 gam kim loại R tác dụng với dung dịch HCl dư thu được 6,272 lít khí H2 (đktc). Xác định kim loại R?
Hòa tan hoàn toàn 8 gam một kim loại A nhóm IIA vào 500ml nước thu được dung dịch X và 4,48 lít khí (đktc).
a. Xác định tên kim loại A.
b. Tính nồng độ mol/l dung dịch X
a) \(n_{H_2}=\dfrac{4,48}{22,4}=0,2\left(mol\right)\)
PTHH: A + 2H2O --> A(OH)2 + H2
0,2<--------------0,2<-----0,2
=> \(M_A=\dfrac{8}{0,2}=40\left(g/mol\right)\)
=> A là Ca (Canxi)
b) \(C_M=\dfrac{0,2}{0,5}=0,4M\)
Đúng 5
Bình luận (0)
Hòa tan hoàn toàn 1,35 gam oxit kim loại M hóa trị III vào dung dịch axit HCL thu được 1,68 lít khí H2 (đktc). Hãy xác định kim loại M?
M2O3 + 6 HCl -> 2 MCl3 + 3 H2O
nH2= 0,075(mol)
=>M(M2O3)=1,35/0,075=
Nói chung bài này số nó cứ lì kì á
Đúng 1
Bình luận (0)
Hòa tan hoàn toàn 11,2 gam một kim loại X vào dung dịch H2SO4 loãng dư. Sau phản ứng thu được 4,48 lít khí H2 (đktc). Tên gọi của X là
A. Magie
B. Kẽm
C. Canxi
D. Sắt
Đáp án : D
Nếu hóa trị của X là n. bảo toàn e :
2 n H 2 = n.nX => nX = 0,4/x (mol)
=> MX = 28n
Với n = 2 thì MX = 56(Fe) (TM)
Đúng 0
Bình luận (0)
Hòa tan hết 15,2 gam hỗn hợp gồm Fe và Cu bằng dung dịch HNO3, thu được dung dịch X và 4,48 lít khí NO ( đktc). Thêm từ từ 3,96 gam kim loại Mg vào hỗn hợp X đến khi phản ứng xảy ra hoàn toàn, thu được 224 ml khí NO (đktc), dung dịch Y và m gam chất rắn không tan. Biết NO là sản phẩm khử duy nhất của N+5 trong các phản ứng. Giá trị của m là: A. 9,6 B. 12,4 C. 15,2 D. 6,4
Đọc tiếp
Hòa tan hết 15,2 gam hỗn hợp gồm Fe và Cu bằng dung dịch HNO3, thu được dung dịch X và 4,48 lít khí NO ( đktc). Thêm từ từ 3,96 gam kim loại Mg vào hỗn hợp X đến khi phản ứng xảy ra hoàn toàn, thu được 224 ml khí NO (đktc), dung dịch Y và m gam chất rắn không tan. Biết NO là sản phẩm khử duy nhất của N+5 trong các phản ứng. Giá trị của m là:
A. 9,6
B. 12,4
C. 15,2
D. 6,4
hòa tan hoàn toàn 21,6 gam kim loại M bằng dung dịch HNO3 thu đượ 5,6 lít hỗn hợp khí A nặng 7,2 gam gồm NO và N2 và dung dịch không chứa muối amoni,kim loại M là
Ta có: \(\left\{{}\begin{matrix}n_{NO}+n_{N_2}=\dfrac{5,6}{22,4}\\30n_{NO}+28n_{N_2}=7,2\end{matrix}\right.\)
\(\Rightarrow\left\{{}\begin{matrix}n_{NO}=0,1\left(mol\right)\\n_{N_2}=0,15\left(mol\right)\end{matrix}\right.\)
Giả sử M có số oxi hóa n.
BT e, có: n.nM = 3nNO + 10nN2
\(\Rightarrow n_M=\dfrac{1,8}{n}\left(mol\right)\)
\(\Rightarrow M_M=\dfrac{21,6}{\dfrac{1,8}{n}}=12n\left(g/mol\right)\)
Với n = 2 thì MM = 24 (g/mol) là thỏa mãn.
Vậy: M là Mg.
Đúng 3
Bình luận (0)



















