Đốt cháy 3,2 g lưu huỳnh S trong khí oxi thu được 2,24 lít lưu huỳnh đioxit SO2. Tính m
Bài 3: Đốt cháy m(g) cacbon (C) cần 16 g oxi thì thu được 22 gam khí cacbonic (CO2).
a/ Lập phương trình khối lượng cho quá trình trên.
b/Tính m
Bài 4. Đốt cháy 3,2 g lưu huỳnh ( S) trong không khí thu được 6,4 g lưu huỳnh đioxit(SO2).
a/ Lập phương trình khối lượng cho quá trình trên.
b/ Tính khối lượng của oxi(O2) đã phản ứng
Bài 3:
\(a,m_C+m_{O_2}=m_{CO_2}\\ b,m=22-16=6\left(g\right)\)
Bài 4:
\(a,m_S+m_{O_2}=m_{SO_2}\\ b,m_{O_2}=6,4-3,2=3,2\left(g\right)\)
bài 3:
a) Lập phương trình: C + O2 -> CO2
b) Do: Trong một phản ứng hóa học, tổng khối lượng của các chất tham gia phản ứng bằng tổng khối lượng chất sản phẩm
=> m + 16 = 22 (g)
=> m = 22-16= 6 g
Vậy m bằng 6g.
Bài 4 giải tương tự
Đốt cháy 3,2 gam lưu huỳnh cháy trong không khí thu được 6,4 gam lưu huỳnh đioxit SO2. Tính khối lượng oxi đã tham gia phản ứng? Biết lưu huỳnh cháy là tham gia phản ứng với khí oxi.
Định luật bảo toàn khối lượng :
\(m_S+m_{O2}=m_{SO2}\)
3,2 + \(m_{O2}\) = 6,4
⇒ \(m_{O2}=6,4-3,2=3,2\left(g\right)\)
Chúc bạn học tốt
\(BTKL: \\ m_S+m_{O_2}=m_{SO_2}\\ 3,2+m_{O_2}=6,4\\ m_{O_2}=6,4-3,2=3,1(g)\)
Đốt cháy lưu huỳnh trong bình chứa 3,5 lít khí oxi, thu được 2,24 lít khí SO2. Các thể tích khí đều đo ở đktc. Khối lượng lưu huỳnh đã phản ứng là: *
3,2 gam
3,6 gam
3,4 gam
3,8 gam
\(n_{SO_2}=\dfrac{2.24}{22.4}=0.1\left(mol\right)\)
\(S+O_2\underrightarrow{^{t^0}}SO_2\)
\(n_S=0.1\left(mol\right)\)
\(m_S=0.1\cdot32=3.2\left(g\right)\)
=> A
PTHH : S + O2 -> SO2
nSO2 = V/22,4= 0,1 mol
Theo PTHH : nS = nSO2 = 0,1 mol
=> mS = n.M = 3,2 g
Theo gt ta có: $n_{O_2}=0,15625(mol);n_{SO_2}=0,1(mol)$
$S+O_2\rightarrow SO_2$
Ta có: $n_{S}=0,1(mol)\Rightarrow m_{S}=3,2(g)$
đốt cháy hết một lượng lưu huỳnh (S) cháy trong 2,24 lít khí oxi (ở đktc) sinh ra khí sunfurơ (SO2). Hãy cho biết :a, thể tích khí sunfurơ thu được ở đktc ?b, khối lượng lưu huỳnh đã bị đốt cháy ?
S + O2 →SO2
a) nO2 = 2,24/22,4 = 0,1 mol
=> nSO2 = 0,1 mol
<=> V SO2 = 0,1 .22,4 = 2,24 lít
b) nS = O2 = 0,1 mol
=> mS = 0,1.32 = 3,2 gam
S + O2 →SO2
a) nO2 = 2,24/22,4 = 0,1 mol
=> nSO2 = 0,1 mol
<=> V SO2 = 0,1 .22,4 = 2,24 lít
b) nS = O2 = 0,1 mol
=> mS = 0,1.32 = 3,2 gam
Bài tập 2:
Đốt cháy sắt trong khí oxi, sau phản ứng thu được 11,6g oxit sắt từ Fe3O4
a. Viết PTHH
b. Tính thể tích khí oxi cần dùng (đktc)
Bài tập 3:
Đốt cháy lưu huỳnh (S) trong oxi không khí thu được 6,4g lưu huỳnh đioxit (SO2 ).
a. Viết PTHH của phản ứng xảy ra?
b. Tính khối lượng của lưu huỳnh đã tham gia?
c. Tính thể tích khí oxi cần trong phản ứng trên?
d. Thể tích không khí đã dùng ở phản ứng trên? (Thể tích các khí đo ở đktc)
Bài tập 4: Phân loại và gọi tên các oxit sau:
CO2, HgO, MgO, FeO, N2O, Li2O, SO3, CaO, CO, BaO; P2O5 ;Na2O; NO2 , Al2O3, ZnO
bài tập 2
3Fe + 2O2 -\(-^{t^o}->\) Fe3O4 (1)
ADCT n= m/M
\(n_{fe_3O_4}\)= 11,6/ 232= 0,05 mol
Theo pt(1) có
\(\dfrac{n_{O2}}{n_{Fe3O4}}\)=\(\dfrac{2}{1}\)
-> \(n_{O2}\)= 2/1 x \(n_{fe3o4}\)
= 0,1 mol
ADCT V= n x 22,4
Vo2= 0,1 x 22,4
= 2,24 (l)
bài tập 4
OXIT AXIT:
- CO2: Cacbon đi oxit
- N2O: đi ni tơ oxit
- SO3: Lưu huỳnh tri oxit
- CO: cacbon oxit
P2O5: đi photpho penta oxit
NO2: Nitơ đi oxit
OXIT BA ZƠ
- HgO: thủy ngân (II) oxit
- MgO: Magie oxit
- FeO: sắt (II) oxit
- Li2O: liti oxit
-CaO: canxi oxit
- BaO: bari oxit
- Na2O: natri oxit
- Al2O3 : Nhôm oxit
ZnO: kẽm oxit
Bổ sung bài 3:
\(a,n_{SO_2}=\dfrac{6,4}{64}=0,1\left(mol\right)\\ PTHH:S+O_2\underrightarrow{t^o}SO_2\\ \left(mol\right)..0,1...0,1\leftarrow0,1\\ b,m_S=0,1.32=3,2\left(g\right)\\ c,V_{O_2}=0,1.22,4=2,24\left(l\right)\\ d,V_{kk}=5.V_{O_2}=5.2,24=11,2\left(l\right)\)
Đốt cháy hoàn toàn 3,2 gam lưu huỳnh trong 2,24 lít khí O 2 . Sau phản ứng khối lượng S O 2 thu được là
A. 6,4 gam.
B. 3,2 gam.
C. 8,0 gam.
D. 4 gam.
Đáp án A
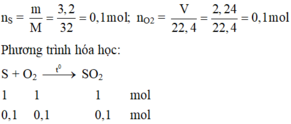
Theo phương trình hóa học S và O 2 phản ứng hết; Sau phản ứng thu được 0,1 mol S O 2 .
m S O 2 = 0 , 1 . ( 32 + 16 . 2 ) = 6 , 4 g a m .
đốt cháy 6,4g lưu huỳnh trong 1 bình chứa 2,24 lít khí oxi ( đktc ) . Tính khối lượng khí sunfuro SO2 thu được
nS=6,4:32=0,2 mol
nO2=2,24:22,4=0,1 mol
PTHH
S+O2->SO2
ban đầu: 0,2 0,1. (Mol)
Phản ứng: 0,1 <-0,1->0,1. (Mol)
Sau pư:. 0,1. 0. 0,1. (Mol)
=> nSO2= 0,1 MOL
=>mSO2= 0,1. 64=6,4 gam
Tích mik nha
Đốt cháy hoàn toàn 64g lưu huỳnh trong bình chứa oxi thu được lưu huỳnh đioxit (SO2) a,Viết phương trình phản ứng xảy ra b,Tính thể tích khí oxi tham gia phương trình ở đktc c,Tính khối lượng Kali clorat (KClO3) cần dùng để phân hủy thì thu được một thể tích khí oxi bằng với thể tích khí oxi đã sử dụng ở phản ứng trên. Gỉa sử hiệu suất của phản ứng là 80%, thể tích đo được ở đktc
a)`S+O_2->SO_2` nhiệt độ
`0,5-0,5`mol
`n_S=32/64=0,5`mol
`V_(O_2)=0,5.22,4=1,12l`l
c) `2KClO_3->2KCl+3O_2` nhiệt độ
`1/3-------0,5` mol
`H=80%`
`m_(KClO_3)=1/3.(122,5).80%=32,67`g
Nếu đốt cháy 3,2 gam lưu huỳnh bằng 22,4l không khí thì khối lượng khí lưu huỳnh đioxit(SO2) thu được là bao nhiêu gam (BiêtSO2=⅕vkk Biết nguyên tử khối:k=39;aln=55;o=16;s=32;c=12
V O2=\(\dfrac{22,4}{5}\)=4,48l
=>n O2=\(\dfrac{4,48}{22,4}\)=0,2 mol
n S=\(\dfrac{3,2}{32}\)=0,1 mol
S+O2-to>SO2
0,1--------------0,1
=>Oxi dư
=>mSO2=0,1.64=6,4g