Một hợp chất X có thành phần phần trăm khối lượng các nguyên tố là: 1.59%H,22.22%N,76.19%O.xác định công thức của X
Hợp chất X có công thức phân tử trùng với công thức đơn giản nhất . Trong phân tử X, thành phần phần trăm khối lượng của các nguyên tố C, H, N lần lượt bằng 40,44% , 7,86% và 15,73%; còn lại là oxi. Tổng các nguyên tố trong phân tử X là
A. 13
B. 12
C. 14
D. 15.
Đáp án A
% m O = 100 – 40,449 – 7,865 – 15,73 = 35,956%
![]()
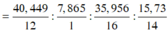
![]()

Bài 7 Một hợp chất có thành phần % về khối lượng các nguyên tố : 24,4%Ca, 17,1 % N, còn lại là O. Công thức của hợp chất đó là
Bài tập 8: Một hợp chất có thành phần % về khối lượng các nguyên tố : 75%C, 25 % H. Công thức của hợp chất đó là?
Bài 7:
Đặt CTHH là \(Ca_xN_yO_z\)
\(\%_O=100\%-24,4\%-17,1\%=58,5\%\\ x:y:z=\dfrac{24,4}{40}:\dfrac{17,1}{14}:\dfrac{58,5}{16}=0,61:1,22:3,66\approx1:2:6\\ \Rightarrow CTHH:Ca\left(NO_3\right)_2\)
Bài 8:
Đặt CTHH là \(C_xH_y\)
\(x:y=\dfrac{75}{12}:\dfrac{25}{1}=6,25:25=1:4\\ \Rightarrow CTHH:CH_4\)
Hãy xác định công thức hóa học của hợp chất X biết: (a) Phần trăm khối lượng của các nguyên tố trong X là 50%S, còn lại là oxi. (b) Phần trăm khối lượng của các nguyên tố trong X là 80%Cu, còn lại là O. (c) Phần trăm khối lượng của các nguyên tố trong X là 2%H, 32,65%S, còn lại là O
nguyên tố x có trong hợp chất x(OH)2 biết nguyên tố x chiếm 54,054% xác định nguyên tố x và viết công thức phân tử hợp chất (tính thành phần, phần trăm về khối lượng của mỗi nguyên tố trong hợp chất)
Một hợp chất X có thành phần phần trăm khối lượng mỗi nguyên tố là : %S=40% và %O=60%
Hãy xác định công thức hóa học của X. Biết tỉ khối của X đối với khí oxi là 2,5.
tìm công thức hóa học của hợp chất X có thành phần phần trăm theo khối lượng các nguyên tố gồm 52,17% carbon 13,05% hydorogen và 34,78% oxygen.Biết khối lượng của hợp chất X là 46 amu
\(m_C=\dfrac{46.52,17}{100}=24g\\ m_H=\dfrac{46.13,05}{100}=6g\\ m_O=\dfrac{46.34,78}{100}=16g\\ n_C=\dfrac{24}{12}=2mol\\ n_H=\dfrac{6}{1}=6mol\\ n_O=\dfrac{16}{16}=1mol\\ \Rightarrow CTHH:C_2H_6O\)
%O = 100% -%C -%H = 100% - 54,54% - 9,1% = 36,36%
\(M_X = 2M_{CO_2} = 2.44 = 88(đvC)\)
Số nguyên tử Cacbon = \(\dfrac{88.54,54\%}{12}= 4\)
Số nguyên tử Hidro = \(\dfrac{88.9,1\%}{1} = 8\)
Số nguyên tử Oxi = \(\dfrac{88.36,36\%}{16} = 2\)
Vậy CTPT của X : C4H8O2
Hợp chất hữu cơ X có thành phần phần trăm khối lượng các nguyên tố như sau: C chiếm 24,24%; H chiếm 4,04%; Cl chiếm 71,72%. Số công thức cấu tạo của X là
A. 3
B. 1
C. 4
D. 2
Đáp án D
Gọi CTPT của X có dạng là CxHyClz
Ta có x : y : z = (24,24 : 12): (4,04 : 1): (71,72:35,5) = 1 : 2 : 1
=> hợp chất có dạng CnH2nCln
=> 2n + 2 ≥ 3n → n ≥2
=> n = 1 hoặc n = 2
Với n = 1 → không thỏa mãn
n = 2 → C2H4Cl2
→ 2 đồng phân
Hợp chất hữu cơ X có thành phần phần trăm khối lượng các nguyên tố như sau: C chiếm 24,24%; H chiếm 4,04%; Cl chiếm 71,72%. Số công thức cấu tạo của X là
A. 4
B. 3
C. 1
D. 2
Chọn D
Gọi CTPT của X có dạng là CxHyClz
Ta có x : y : z = (24,24 : 12): (4,04 : 1): (71,72:35,5) = 1 : 2 : 1
=> hợp chất có dạng CnH2nCln
=> 2n + 2 ≥ 3n => n ≥ 2
=> n = 1 hoặc n = 2
Với n = 1 => không thỏa mãn
n = 2 => C2H4Cl2
=> 2 đồng phân