Phản ứng hóa học nào sau đây chỉ xảy ra trong quá trình điện phân dung dịch?
A. Fe + CuSO4 → FeSO4 + Cu
B. 2CuSO4 + 2H2O → 2Cu + O2+ 2H2SO4
C. CuSO4 + 2NaOH → Cu(OH)2 + Na2SO4
D. Cu + 2AgNO3 → 2Ag+ Cu(NO3)2
Cho biết đã xảy ra sự oxi hóa và sự khử những chất nào trong những phản ứng thế sau:
a) Cu + 2AgNO3 → Cu(NO3)2 + 2Ag.
b) Fe + CuSO4 → FeSO4 + Cu.
c) 2Na + 2H2O → 2NaOH + H2.
Sự oxi hóa và sự khử những chất trong phản ứng thế sau:
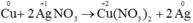
- Sự nhường electron của Cu được gọi là sự oxi hóa nguyên tử đồng: Cu0 → Cu2+ + 2e
- Sự nhận electron của ion bạc được gọi là sự khử ion bạc: Ag+ + 1e → Ag
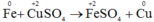
- Sự nhường electron của sắt được gọi là sự oxi hóa nguyên tử sắt: Fe0 → Fe2+ + 2e
- Sự nhận electron của ion đồng được gọi là sự khử ion đồng: Cu2+ + 2e → Cu0
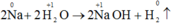
- Sự nhường electron của natri được gọi là sự oxi hóa nguyên tử natri: Na0 → Na+ + 2e
- Sự nhận electron của ion hidro gọi là sự khử ion hiđro: 2H+ + 2e → H2
Cho các phản ứng sau:
(a) CuO + H2 → Cu + H2O;
(b) 2CuSO4 + 2H2O → đpdd 2Cu + O2 + 2H2SO4;
(c) Fe + CuSO4 → FeSO4 + Cu;
(d) 2Al + Cr2O3 → t o Al2O3 + 2Cr
Số phản ứng dùng để điều chế kim loại bằng phương pháp nhiệt luyện là
A. 4
B. 3
C. 2
D. 1
Đáp án C
« Phương pháp nhiệt luyện dùng điều chế các kim loại có độ hoạt động trung bình như Zn, Fe, Sn, Pb, ... bằng cách khử các ion kim loại của chúng trong hợp chất ở nhiệt độ cao bằng các chất khử như C, CO, H2 hoặc các kim loại hoạt động như Al → có 2 phản ứng dùng để điều chế kim loại bằng phương pháp nhiệt luyện là phản ứng (a) và (d).
(a) CuO + H2 → t o Cu + H2O;
(d) 2Al + Cr2O3 → t o Al2O3 + 2Cr.
Cho các phản ứng sau:
(1) CuO + H 2 → Cu + H 2 O
(2) 2 CuSO 4 + 2 H 2 O → 2 Cu + O 2 + 2 H 2 SO 4
(3) Fe + CuSO 4 → FeSO 4 + Cu
(4) 2 Al + Cr 2 O 3 → Al 2 O 3 + 2 Cr
Số phản ứng dùng để điều chế kim loại bằng phương pháp nhiệt luyện là
A. 4
B. 3
C. 2
D. 1
Chọn C
Các phản ứng điều chế kim loại bằng phương pháp nhiệt luyện là (1) và (4). Phản ứng thủy luyện là phản ứng người ta sử dụng các tác nhân khử ở nhiệt độ cao để khử các hợp chất, oxit kim loại về kim loại.
Phản ứng 3 là phương pháp thủy luyện, phản ứng 2 thực chất là điện phân dung dịch.
Cho các phản ứng sau:
(1) CuO + H2® Cu+H2O (2) 2CuSO4+ 2H2O ® 2Cu + O2+2H2SO4
(3) Fe + CuSO4 ® FeSO4+Cu (4) 2Al + Cr2O3® Al2O3+2Cr
Số phản ứng dùng để điều chế kim loại bằng phương pháp nhiệt luyện là.
A. 4
B. 3
C. 2
D. 1
Cho các phản ứng sau:
(1) CuO + H 2 → Cu + H 2 O
(2) 2 CuSO 4 + 2 H 2 O → 2 Cu + O 2 + H 2 SO 4
(3) Fe + CuSO 4 → FeSO 4 + Cu
(4) 2 Al + Cr 2 O 3 → Al 2 O 3 + 2 Cr
Số phản ứng dùng để điều chế kim loại bằng phương pháp nhiệt luyện là
A. 2
B. 4
C. 3
D. 1
Đáp án A
Các phản ứng điều chế kim loại bằng phương pháp nhiệt luyện là (1) và (4). Phản ứng thủy luyện là phản ứng người ta sử dụng các tác nhân khử ở nhiệt độ cao để khử các hợp chất, oxit kim loại về kim loại.
Phản ứng 3 là phương pháp thủy luyện, phản ứng 2 thực chất là điện phân dung dịch
Phản ứng nào sau đây là sai ? A. Fe + HCl-> FeCl2 + H2 B. 2Na + CuSO4 -> Na2SO4 + Cu C. Fe + CuSO4 -> FesO4 + Cu D. CuO + H2 -> (t°) Cu + H2O
Cho các phản ứng sau:
H2SO4 + Fe → FeSO4 + H2 (1)
3H2SO4 + 6NaNO2 → 3Na2SO4 + 4NO + 2HNO3 + 2H2O (2)
Cu + 2H2SO4 đ, nóng → CuSO4 + SO2 + 2H2O (3)
H2SO4 + FeSO3 → FeSO4 + SO2 + H2O (4)
Hăy cho biết phản ứng nào H2SO4 đóng vai trò là chất oxi hóa ?
A. (1), (3), (4)
B. (1), (2), (3)
C. (3)
D. (1), (3)
ĐÁP ÁN D
H2SO4 đóng vai trò là chất oxi hóa khi số oxi hóa của 1 hoạc tất cả các nguyên tố H,S,O giảm. Các phản ứng xảy ra hiện tương này là 1 và 3
=> chọn D
Câu 11: Cho các cặp chất sau:
(a) Fe và dung dịch HCl; (d) Cu và dung dịch FeSO4;
(b) Zn và dung dịch CuSO4; (e) Cu và dung dịch AgNO3; (c) Ag và dung dịch HCl; (f) Pb và dung dịch ZnSO4.
Những cặp chất nào xảy ra phản ứng hóa học?
A. a, c, d. B. c, d, e, f. C. a, b, e. D. a, b, c, d, e.
Câu 12: Đốt cháy hoàn toàn 28,8 gam kim loại M (hóa trị II) trong bình khí clo dư, sau phản ứng thu được 60,75 gam muối. M là kim loại nào dưới đây?
A. Fe. B. Cu. C. Mg. D. Zn.
Câu 13: Cho sơ đồ phản ứng sau: “MgCl2 +............−−− Mg(NO3)2 +……….”. Cặp hệ số và công thức hóa học tương ứng được điền vào chỗ trống để được phương trình hóa học đúng là:
A. 2HNO3 và 2HCl. C. Ba(NO3)2 và BaCl2.
B. 2AgNO3 và 2AgCl. D. 2NaNO3 và 2NaCl.
Câu 14: Ngâm một đinh sắt sạch trong dung dịch CuSO4 loãng một thời gian. Hiện tượng xảy nào quan sát được trong quá trình phản ứng?
A. Xuất hiện sủi bọt khí, màu xanh của dung dịch nhạt dần.
B. Xuất hiện kim loại đồng màu đỏ bám ngoài đinh sắt, màu xanh của dung dịch đậm dần.
C. Xuất hiện kim loại đồng màu đỏ bám ngoài đinh sắt, dung dịch không đổi màu.
D. Một phần đinh sắt bị hòa tan, màu xanh của dung dịch nhạt dần, xuất hiện kim loại đồng màu đỏ bám ngoài đinh sắt.
Câu 15: Hoà tan hoàn toàn 3,25 gam một kim loại X (hoá trị II) bằng dung dịch H2SO4 loãng dư thu được 1,12 lít khí H2 (đktc). X là kim loại nào trong số các kim loại dưới đây?
A. Fe. B. Mg. C. Ca. D. Zn.
Câu 16: Cho 13 gam kim loại Zn tác dụng vừa đủ với 200 gam dung dịch HCl. Giá trị nào dưới đây là nồng độ phần trăm của dung dịch HCl đã dùng?
A. 7,3%. B. 6,5%. C. 3,65%. D. 14,6%.
Câu 17: Phân bón hóa học có chứa chất nào sau đây thuộc loại phân bón kép?
A. KCl . B. CO(NH2)2. C. (NH4)2 HPO4. D. Ca(H2PO4)2.
Câu 18: Kim loại vonfam được dùng làm dây tóc bóng đèn là do A. vonfam có độ cứng cao.
B. vonfam có tính dẫn điện, nhiệt độ nóng chảy cao.
C. vonfam có tính dẻo.
D. vonfam có tính dẫn nhiệt tốt.
Câu 19: Cho 13,35 gam nhôm clorua tác dụng với dung dịch bạc nitrat (dư). Tính khối lượng kết tủa (mkt) thu được.
A. mkt = 40,05 gam. C. mkt = 162 gam.
B. mkt = 43,05 gam. D. mkt = 133,5 gam.
Câu 20: Cho hỗn hợp Mg, Zn, Fe tác dụng vừa đủ với dung dịch HCl 0,5M thấy thoát ra 4,48 lít H2 (ở đktc). Thể tích dung dịch HCl cần dùng bằng bao nhiêu?
A. VddHCl = 100 ml. C. VddHCl = 600 ml.
B. VddHCl = 500 ml. D. VddHCl = 800 ml.
Câu 11: Cho các cặp chất sau:
(a) Fe và dung dịch HCl; (d) Cu và dung dịch FeSO4;
(b) Zn và dung dịch CuSO4; (e) Cu và dung dịch AgNO3; (c) Ag và dung dịch HCl; (f) Pb và dung dịch ZnSO4.
Những cặp chất nào xảy ra phản ứng hóa học?
A. a, c, d. B. c, d, e, f. C. a, b, e. D. a, b, c, d, e.
Câu 12: Đốt cháy hoàn toàn 28,8 gam kim loại M (hóa trị II) trong bình khí clo dư, sau phản ứng thu được 60,75 gam muối. M là kim loại nào dưới đây?
A. Fe. B. Cu. C. Mg. D. Zn.
Câu 13: Cho sơ đồ phản ứng sau: “MgCl2 +............−−− Mg(NO3)2 +……….”. Cặp hệ số và công thức hóa học tương ứng được điền vào chỗ trống để được phương trình hóa học đúng là:
A. 2HNO3 và 2HCl. C. Ba(NO3)2 và BaCl2.
B. 2AgNO3 và 2AgCl. D. 2NaNO3 và 2NaCl.
Câu 14: Ngâm một đinh sắt sạch trong dung dịch CuSO4 loãng một thời gian. Hiện tượng xảy nào quan sát được trong quá trình phản ứng?
A. Xuất hiện sủi bọt khí, màu xanh của dung dịch nhạt dần.
B. Xuất hiện kim loại đồng màu đỏ bám ngoài đinh sắt, màu xanh của dung dịch đậm dần.
C. Xuất hiện kim loại đồng màu đỏ bám ngoài đinh sắt, dung dịch không đổi màu.
D. Một phần đinh sắt bị hòa tan, màu xanh của dung dịch nhạt dần, xuất hiện kim loại đồng màu đỏ bám ngoài đinh sắt.
Câu 15: Hoà tan hoàn toàn 3,25 gam một kim loại X (hoá trị II) bằng dung dịch H2SO4 loãng dư thu được 1,12 lít khí H2 (đktc). X là kim loại nào trong số các kim loại dưới đây?
A. Fe. B. Mg. C. Ca. D. Zn.
Câu 16: Cho 13 gam kim loại Zn tác dụng vừa đủ với 200 gam dung dịch HCl. Giá trị nào dưới đây là nồng độ phần trăm của dung dịch HCl đã dùng?
A. 7,3%. B. 6,5%. C. 3,65%. D. 14,6%.
Câu 17: Phân bón hóa học có chứa chất nào sau đây thuộc loại phân bón kép?
A. KCl . B. CO(NH2)2. C. (NH4)2 HPO4. D. Ca(H2PO4)2.
Câu 18: Kim loại vonfam được dùng làm dây tóc bóng đèn là do
A. vonfam có độ cứng cao.
B. vonfam có tính dẫn điện, nhiệt độ nóng chảy cao.
C. vonfam có tính dẻo.
D. vonfam có tính dẫn nhiệt tốt.
Câu 19: Cho 13,35 gam nhôm clorua tác dụng với dung dịch bạc nitrat (dư). Tính khối lượng kết tủa (mkt) thu được.
A. mkt = 40,05 gam. C. mkt = 162 gam.
B. mkt = 43,05 gam. D. mkt = 133,5 gam.
Câu 20: Cho hỗn hợp Mg, Zn, Fe tác dụng vừa đủ với dung dịch HCl 0,5M thấy thoát ra 4,48 lít H2 (ở đktc). Thể tích dung dịch HCl cần dùng bằng bao nhiêu?
A. VddHCl = 100 ml. C. VddHCl = 600 ml.
B. VddHCl = 500 ml. D. VddHCl = 800 ml.
Cho phản ứng hóa học sau: Fe + CuSO4 ® FeSO4 + Cu
Trong phản ứng trên xảy ra:
A. sự khử Fe2+ và sự oxi hóa Cu.
B. sự khử Fe2+ và sự khử Cu2+.
C. sự oxi hóa Fe và sự oxi hóa Cu.
D. sự oxi hóa Fe và sự khử Cu2+.
1.a)Tính khối lượng dung dịch H2SO4 98% tối thiểu cần dùng để điều chế cùng 1 mol CuSO4 theo 2 cách sau:
a1)Pha loãng dung dịch H2SO4,cho Cu tác dụng với dugn dịch H2SO4 loãng với sự có mặt của O2 theo pthh: 2Cu+O2+2H2SO4 --->2CuSO4+2H2O
a2)Cho Cu tác dụng với H2SO4 98% đun nóng.
b)Phương pháp nào tiết kiệm H2SO4 hơn ?
2.Từ 1 tấn lưu quỳnh có 2% tập chất trơ người ta có thể sản xuất bao nhiêu tấn dung dịch H2SO4 98% với hiệu suất của quá tình sản xuất là 98%
a1)Pha loãng dung dịch H2SO4,cho Cu tác dụng với dugn dịch H2SO4 loãng với sự có mặt của O2 theo pthh:
2Cu+O2+2H2SO4 --->2CuSO4+2H2O
Theo PT: \(n_{H_2SO_4}=n_{CuSO_4}=1\left(mol\right)\)
=> \(m_{ddH_2SO_4}=\dfrac{1.98}{98\%}=100\left(g\right)\)
a2)Cho Cu tác dụng với H2SO4 98% đun nóng.
Cu + 2H2SO4 → CuSO4 + SO2 + 2H2O
Theo PT: \(n_{H_2SO_4}=2n_{CuSO_4}=2\left(mol\right)\)
=> \(m_{ddH_2SO_4}=\dfrac{2.98}{98\%}=200\left(g\right)\)
b)Phương pháp nào tiết kiệm H2SO4 hơn ?
Phương pháp thứ nhất tiết kiệm H2SO4 hơn vì chỉ sử dụng có 100g dd H2SO4 98%