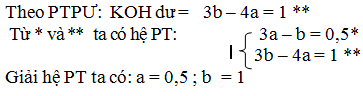Trộn dung dịch chứa a mol AlCl3 với dung dịch chứa b mol KOH. Để thu được kết tủa thì cần có tỉ lệ
A. a : b = 1 : 4
B. a : b < 1 : 4
C. a : b = 1 : 5
D. a : b > 1 : 4
Trộn dung dịch chứa a mol A l C l 3 với dung dịch chứa b mol NaOH. Để thu được kết tủa thì cần có tỉ lệ
A. a : b = 1 : 4
B. a : b < 1 : 4
C. a : b = 1 : 5
D. a : b > 1 : 4
Trộn dung dịch chứa a mol AlCl3 với dung dịch chứa b mol NaOH. Để thu được kết tủa thì cần có tỉ lệ
A. a:b = 1:4
B. a:b < 1:4
C. a:b = 1:5
D. a:b > 1:4
Trộn dung dịch chứa a mol AlCl 3 với dung dịch chứa b mol NaOH. Để thu được kết tủa thì cần có tỉ lệ
A. a : b < 1 : 4
B. a : b = 1 : 3
C. a : b = 1 : 4
D. a : b > 1 : 4
Trộn dung dịch chứa a mol AlCl3 với dung dịch chứa b mol NaOH. Để thu được kết tủa thì cần có tỉ lệ
A. a : b = 1 : 4
B. a : b < 1 : 4
C. a : b = 1 : 5
D. a : b > 1 : 4
Đáp án D
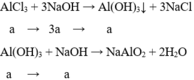
Nếu n NaOH = 4a thì kết tủa sẽ tan hết => để có kết tủa thì: n NaOH < 4a => b < 4a
=> a : b > 1 : 4
Trộn dung dịch chứa a mol AlC3 với dung dịch chứa b mol KOH. Để thu được kết tủa thì cần có tỉ lệ
A. a : b = 1 : 4
B. a : b < 1 : 4
C. a : b = 1 : 5
D. a : b > 1 : 4
Trộn dung dịch chứa a (mol) AlCl3 với dung dịch chứa b (mol) NaOH.
Tính tỉ lệ a:b để thu được kết tủa.
AlCl3: a mol
NaOH: b mol
Al3+a+→3OH−3a→Al(OH)3↓aAl3++3OH−→Al(OH)3↓a→3aa (kết tủa cực đại)
Al(OH)3a+→OH−a→AlO2−+2H2OAl(OH)3+OH−→AlO2−+2H2Oa→a
Nếu nNaOH = 4a thì kết tủa sẽ tan hết ⇒ để có kết tủa thì:
nNaOH < 4a ⇒ b < 4a
⇒ a : b > 1 : 4
Dung dịch X chứa a mol HCl và b mol AlCl3 . Thêm từ từ dung dịch NaOH 1M vào dung dịch X, đến khi hết 100 ml thì bắt đầu xuất hiện kết tủa, còn khi hết 800 ml hoặc 1200 ml thì đều thu được 15,6 gam kết tủa. Tỉ lệ a : b là
A. 4 : 3
B. 2 : 3
C. 1 : 1.
D. 1 : 2
Trộn dung dịch A chứa NaOH và dung dịch B chứa Ba(OH)2 theo tỉ lệ thể tích bằng nhau thu được dung dịch C. Trung hoà 100 ml dung dịch C cần dùng hết 35 ml dung dịch H2SO4 2M và thu được 9,32 gam kết tủa. Tính nồng độ mol của các dung dịch A và B. Cần phải trộn bao nhiêu ml dung dịch B với 20 ml dung dịch A để thu được dung dịch D có thể hoà tan vừa hết 20,4 gam bột Al2O3
Gọi \(\left\{{}\begin{matrix}C_{M\left(A\right)}=aM\\C_{M\left(B\right)}=bM\end{matrix}\right.\)
Giả sử trộn 50ml dd A với 50ml dd B để thu được 100ml dd C
=> \(\left\{{}\begin{matrix}n_{NaOH}=0,05a\left(mol\right)\\n_{Ba\left(OH\right)_2}=0,05b\left(mol\right)\end{matrix}\right.\)
\(n_{BaSO_4}=\dfrac{9,32}{233}=0,04\left(mol\right)\)
nH2SO4 = 0,035.2 = 0,07 (mol)
PTHH: Ba(OH)2 + H2SO4 --> BaSO4 + 2H2O
0,04<----0,04<-------0,04
2NaOH + H2SO4 --> Na2SO4 + 2H2O
0,06<----0,03
=> \(\left\{{}\begin{matrix}0,05a=0,06\\0,05b=0,04\end{matrix}\right.\)
=> a = 1,2; b = 0,8
20 ml dd A chứa nNaOH = 0,02.1,2 = 0,024 (mol)
\(n_{Al_2O_3}=\dfrac{20,4}{102}=0,2\left(mol\right)\)
PTHH: 2NaOH + Al2O3 --> 2NaAlO2 + H2O
0,024-->0,012
Ba(OH)2 + Al2O3 --> Ba(AlO2)2 + H2O
0,188<---0,188
=> \(V_{dd.B}=\dfrac{0,188}{0,8}=0,235\left(l\right)=235\left(ml\right)\)
đặt nồng độ mol của dd a là a , dd b la b. khi trộn 3 l a (có 3a mol) với 2 lit b (có 2b mol) được 5 lit dd x có dư axit. trung hoà 5 lit dd x cần
nKOH =0,2.5 = 1mol -> số mol H2SO4 dư: 0,5 mol.
H2SO4+ 2KOH -> K2SO4 +2 H2O
b-------------- 2b
số mol h2so4 dư = 3a – b = 0,5*
trộn 2l dd a (có 2a mol) với 3 lít ddb (có 3b mol) tạo 5 l dd y có koh dư. trung hoà 5 lit y cần 0,2 .5 = 1 mol hcl
pt: H2SO4 + 2KOH -> K2SO4 + 2H2O
2a---------------- 4a