Cho phản ứng hóa học: F e + C u S O 4 → F e S O 4 + C u . Trong phản ứng trên xảy ra
A. sự khử F e 2 + và sự oxi hóa Cu.
B. sự khử F e 2 + và sự khử C u 2 +
C. sự oxi hóa Fe và sự oxi hóa Cu
D. sự oxi hóa Fe và sự khử C u 2 +
Cho các chất tham gia phản ứng:
a) S+F2 → ....
b) SO2+H2S →...
c) SO2+O2 (xt) →...
d) S+H2SO4 (đặc, nóng) →...
e) H2S+Cl2(dư)+H2O→...
f) SO2+Br2+H2O→....
Số phản ứng tạo ra sản phẩm mà lưu huỳnh ở mức số oxi hóa +6 là:
A. 2
B. 5
C. 4
D. 3
Cho các chất tham gia phản ứng:
a. S + F2 b. SO2 + Br2 + H2O
c. SO2 + O2 d. SO2 + H2SO4 đặc, nóng
e. SO2 và H2O f. H2S + Cl2(dư) + H2O
Số phản ứng tạo ra lưu huỳnh ở mức oxi hóa +6 là:
A. 2
B. 3
C. 4
D. 5
Cho các chất tham gia phản ứng:
a. S + F2 b. SO2 + Br2 + H2O
c. SO2 + O2 d. SO2 + H2SO4 đặc, nóng
e. SO2 và H2O f. H2S + Cl2(dư) + H2O
Số phản ứng tạo ra lưu huỳnh ở mức oxi hóa +6 là:
A. 2
B. 3
C. 4
D. 5
Hoàn thành đầy đủ các phương trình hóa học sau, ghi rõ điều kiện của phản ứng (nếu có). a) Mg + ? → MgSO4 + ? b) KClO3 → ? + ? c) H2 + Fe2O3 → ? + ? d) Al + O2 → ? e) CH4 + O2 → ? + ? f) ? + S → SO2 g) H2 + ? → Cu + H2O h) KMnO4 → ? + ? + O2 i) ? + HCl → ZnCl2 + ? j) P + O2 → P2O5
\(Mg+H_2SO_4->MgSO_4+H_2\\ 2KClO_3-^{t^o}>2KCl+3O_2\\ 3H_2+Fe_2O_3->2Fe+3H_2O\\ 4Al+3O_2-^{t^o}>2Al_2O_3\\ CH_4+2O_2-^{t^o}>CO_2+2H_2O\\ O_2+S-^{t^o}>SO_2\\ H_2+CuO-^{t^o}>Cu+H_2O\\ 2KMnO_4-^{t^o}>K_2MnO_4+MnO_2+O_2\\ Zn+2HCl->ZnCl_2+H_2\\ 4P+5O_2-^{t^o}>2P_2O_5\)
Đốt cháy hoàn toàn 5,4 g kim loại nhôm Al trong khí oxi. a. Tính thể tích khí oxi (đktc) cần dùng cho phản ứng. b. Tính khối lượng KClO3 cần dùng để điều chế lượng oxi trên.
1.r/f/a/e/h/t/e/s 2. n/o/c/a/h/e/m/e/l 3. p/n/e/g/n/i/u 4. s/ e/ s/ l/ a/ c 5. w/a/n/s
1. feathers (n) : lông vũ
2. chameleon (n) : tắc kè
3. penguin (n) : cánh cụt
4. scales (n) : vảy
5. swan (n) : thiên nga
1. feathers
2. chameleon
3. penguin
4. scales
5. swan
1. Feathers
2. Chameleon
3. Penguin
4. Scales
5. Swan
Hãy xác định các chữ cái A, B, C, D, E, F, G, I, J, L là những công thức hóa học nào và viết phương trình phản ứng.( Ghi rõ điều kiện phản ứng)
E -> A + B
B + C -> D
D + E -> F
Zn + F -> Zn3(PO4)2 + A
A + B -> E
CaCO3 -> I + L
J + E -> L
Biết L làm quỳ tím hóa xanh
\(2KClO_3\underrightarrow{t^o}2KCl+3O_2\\ 5O_2+4P\underrightarrow{t^o}2P_2O_5\\ P_2O_5+3H_2O\rightarrow2H_3PO_4\\ 3Zn+2H_3PO_4\rightarrow Zn_3\left(PO_4\right)_2+3H_2\\ 2H_2+O_2\underrightarrow{t^o}2H_2O\\ CaCO_3\underrightarrow{t^o}CO_2+CO_2\\ CaO+H_2O\rightarrow Ca\left(OH\right)_2\)
Hoàn thành các phương trình hóa học sau:
a. ? t o → KCl + O2 d. KMnO4 t o → ? + ? + ?
b. ? + ? t o → MgO e. S + O2 t o → ?
c. C4H10 + O2 t o → ? + ? f. FeS2 + ? t o → Fe2O3 + ?
Hãy cho biết trong các phản ứng trên, phản ứng nào thuộc phản ứng hóa hợp, phân hủy? Phản ứng nào là sự oxi hóa?
a. \(2KClO_3\xrightarrow[]{t^o}2KCl+3O_2\)
b. \(2Mg+O_2\xrightarrow[]{t^o}2MgO\)
c. \(2C_4H_{10}+13O_2\xrightarrow[]{t^o}8CO_2+10H_2O\)
d. \(2KMnO_4\xrightarrow[]{t^o}K_2MnO_4+MnO_2+O_2\)
e. \(S+O_2\xrightarrow[]{t^o}SO_2\)
f. \(4FeS_2+11O_2\xrightarrow[]{t^o}2Fe_2O_3+8SO_2\)
Có những sơ đồ phản ứng hóa học sau:
a) Cl2 + H2O → HCl + HClO
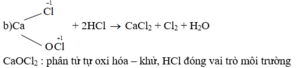
b) CaOCl2 + 2HCl → CaCl2 + Cl2 + H2O
c) Cl2 + KOH → KCl + KClO3 + H2O
d) HCl + KClO3 → KCl + Cl2 + H2O
e) NaClO + CO2 + H2O → NaHCO3 + HClO
f) CaOCl3 → CaCl2 + O2
Cho biết những phản ứng nào là phản ứng oxi hóa – khử? Vai trò các chất tham gia phản ứng oxi hóa – khử. Hoàn thành phương trình hóa học của các phản ứng.
Những phản ứng sau là phản ứng oxi hóa – khử:


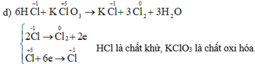
![]()
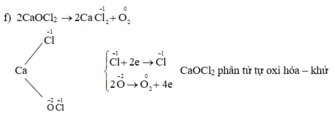
Order the letters to form jobs
1. t c a n t o u n a c =>............
2, n t e l e c c r i i a =>...........
3, s a t p o l k e o r r w => .........
4, i d h a r r r e e s s => ............
5, c t a e e r h =>..........
6, c o e f f i r e k o r m =>..................
Order the letters to form jobs
1. t c a n t o u n a c => accountant
2, n t e l e c c r i i a => electricant
còn lại tự lm
4, i d h a r r r e e s s =>Hairdresser
5, c t a e e r h =>teacher
Hãy lập các phương trình hóa học sau đây và cho biết phản ứng thuộc loại phản ứng hóa hợp hay phản ứng phân hủy?
a. KMnO4 à ? + MnO2 + ?
b. ? + ? à Fe3O4
c. ? + ? à P2O5
d. HgO à ? + ?
e. KClO3 à ? + ?
f. ? + ? à MgO
g. Fe(OH)3 à Fe2O3 + ?
h. N2 + ? à N2O5
\(2KMnO_4\underrightarrow{^{t^0}}K_2MnO_4+MnO_2+O_2\left(PH\right)\)
\(3Fe+2O_2\underrightarrow{^{t^0}}Fe_3O_4\left(HH\right)\)
\(4P+5O_2\underrightarrow{^{t^0}}2P_2O_5\left(HH\right)\)
\(2HgO\underrightarrow{^{t^0}}2Hg+O_2\left(PH\right)\)
\(2KClO_3\underrightarrow{^{t^0}}2KCl+3O_2\left(PH\right)\)
\(2Mg+O_2\underrightarrow{^{t^0}}2MgO\left(HH\right)\)
\(2Fe\left(OH\right)_3\underrightarrow{^{t^0}}Fe_2O_3+3H_2O\left(PH\right)\)
\(N_2+\dfrac{5}{2}O_2\underrightarrow{^{t^0}}N_2O_5\left(HH\right)\)