100 ml dung dịch Fe2(SO4)3 1M có thể hòa tan tối đa m gam Cu. Giá trị của m là
A. 9,6 gam
B. 3,2 gam
C. 6,4 gam
D. 12,8 gam
100 ml dung dịch Fe2(SO4)3 1M có thể hòa tan tối đa m gam Cu. Giá trị của m là
A. 9,6 gam.
B. 3,2 gam.
C. 6,4 gam.
D. 12,8 gam.
cho 6,4 gam Cu vào 150 ml dung dịch HNO3 4M thu được khí NO và dung dịch X. thêm 200 ml dung dịch HCl 2M vào dung dịch thu được dung dịch Y. Hãy cho biết dung dịch Y có thể hòa tan tối đa bao nhiêu gam Cu
A. 17,6 B.12,8 C 3,2 D.6,4
\(n_{Cu} = 0,1\ mol\\ n_{HNO_3} = 0,6\ mol\)
3Cu + 8HNO3 → 3Cu(NO3)2 + 2NO + 4H2O
0,1........\(\dfrac{4}{15}\)..........................................................(mol)
\(n_{H^+\ dư} = 0,6 - \dfrac{4}{15} = \dfrac{1}{3}(mol)\)
Khi thêm HCl,\(n_{H^+} = \dfrac{1}{3} + 0,2.2 = \dfrac{11}{15}\)
\(3Cu + 8H^+ + 2NO_3^- \to 3Cu^{2+} + 2NO + 4H_2O\)
\(n_{H^+} < 4n_{NO_3^-} = 0,6.4\) nên NO3- dư.
Theo PTHH :
\(n_{Cu} = \dfrac{3}{8}n_{H^+} = \dfrac{3}{8}.\dfrac{11}{15} = 0,275(mol)\\ \Rightarrow m_{Cu} = 0,275.64 = 17,6(gam)\)
1.Phân hủy hoàn toàn 12 gam đồng (II) hiđroxit ở nhiệt độ cao sau phản ứng thu được m gam đồng (II) oxit. Giá trị của m là
A. 12,8 gam. B. 9,6 gam. C. 6,4 gam. D. 3,2 gam.
2.Trung hòa 200 gam dung dịch NaOH 6% cần dùng 150 gam dung dịch H2SO4C%. Giá trị của C% là
A. 4,9%. B. 7,84% .C. 9,8%. D. 11,76%.
Cho 6,72 gam Fe vào 400 ml dung dịch HNO3 1M, đến khi phản ứng xảy ra hoàn toàn, thu được khí NO (sản phẩm khử duy nhất) và dung dịch X. Dung dịch X có thể hoà tan tối đa m gam Cu. Giá trị của m là:
A. 1,92 gam B. 3,20 gam C. 0,64 gam D. 3,84 gam
nFe = 0,12 mol → ne cho = 0,36 mol; nHNO3 = 0,4 mol → ne nhận = 0,3 mol
- Do ne cho > ne nhận → Fe còn dư → dung dịch X có Fe2+ và Fe3+
- Các phản ứng xảy ra là:
Fe + 4HNO3 → Fe(NO3)3 + NO + 2H2O
0,1 ← 0,4 → 0,1
Fe (dư) + 2Fe3+ → 3Fe2+
0,02 → 0,04
Cu + 2Fe3+ (dư) → Cu2+ + 2Fe2+
0,03 ← 0,06
→ mCu = 0,03.64 = 1,92 gam → đáp án A
Coi hỗn hợp Cu và Fe cho vào HNO3
=> 8/3nFe + 8/3nCu = n HNO3 pư = 0,4
=> n Cu = 0,03 mol
=> m Cu = 1,92 gam
D/an :A
Cho 6,72 gam Fe vào 400 ml dung dịch HNO3 1M, đến khi phản ứng xảy ra hoàn toàn, thu được khí NO (sản phẩm khử duy nhất) và dung dịch X. Dung dịch X có thể hòa tan tối đa m gam Cu. Giá trị của m là
A. 3,84.
B. 3,20
C. 1,92
D. 0,64
Chọn C
Ta có nFe = 0,12 mol; nHNO3 = 0,4 mol
Fe + 4HNO3 → Fe(NO3)3 + NO + 2H2O
0,1 ← 0,4 → 0,1
(dư 0,02)
Fe còn dư + 2Fe(NO3)3 → 3Fe(NO3)2
0,02 → 0,04
(còn dư 0,06)
Dung dịch X chứa Fe(NO3)2 và Fe(NO3)3 còn dư
Khi cho Cu và dung dịch X thì:
Cu + 2Fe(NO3)3còn dư →Cu(NO3)2 + 2Fe(NO3)2
0,03 ← 0,06
Vậy mCu tối đa = 64.0,03 = 1,92g
Hòa tan hỗn hợp bột kim loại gồm 8,4 gam Fe và 6,4 gam Cu vào 350 ml dung dịch AgNO3 2M. Sau khi phản ứng xảy ra hoàn toàn thu được m gam chất rắn. Giá trị của m là:
A. 70,2 gam B. 54 gam C. 75,6 gam D. 64,8 gam
nFe = 0,15 mol ; nCu = 0,1 ; nAg+ = 0,7 mol
Fe + 2Ag+ → Fe2+ + 2Ag (1)
0,15→ 0,3 0,15 0,3
Cu + 2Ag+ → Cu2+ + 2Ag
0,1 → 0,2 0,2
Fe2+ + Ag+ → Fe3+ + Ag (3)
0,15 → 0,15 0,15
Từ (1) ; (2) → m = (0,3 + 0,2 + 0,15).108 = 70,2 gam → Đáp án A
Hòa tan hết 31,2 gam hỗn hợp Fe, FeO, Fe2O3 vào 800 ml dung dịch HNO3 2M vừa đủ, thu được V lít NO (đktc, sản phẩm khử duy nhất) và dung dịch X. Dung dịch X hòa tan tối đa 9,6 gam Cu. Giá trị của V là:
A. 8,21 lít
B. 6,72 lít
C. 3,36 lít.
D. 3,73 lít.
Đáp án B
Sơ đồ phản ứng
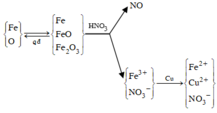
Xét toàn bộ quá trình phản ứng, ta thấy : Chất khử là Fe, Cu; chất oxi hóa là O và N + 5 trong HNO3. Theo bảo toàn electron, bảo toàn điện tích trong dung dịch sau phản ứng và giả thiết, ta có
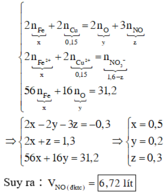
Hòa tan hết 31,2 gam hỗn hợp Fe, FeO, Fe2O3 vào 800 ml dung dịch HNO3 2M vừa đủ thu được V lít NO (đkc, sản phẩm khử duy nhất) và dung dịch X. Dung dịch X hòa tan tối đa 9,6 gam Cu. Giá trị của V là:
A. 8,21 lít
B. 6,72 lít
C. 3,36 lít
D. 3,73 lít
Hòa tan hết 31,2 gam hỗn hợp Fe, FeO, Fe2O3 vào 800 ml dung dịch HNO3 2M vừa đủ, thu được V lít NO (đktc, sản phẩm khử duy nhất) và dung dịch X. Dung dịch X hòa tan tối đa 9,6 gam Cu. Giá trị của V là
A. 8,21 lít
B. 6,72 lít
C. 3,36 lít
D. 3,73 lít