Đốt cháy hoàn toàn một lượng hiđrocacbon X thu được 8,4 lít khí CO2 ở đktc và 5,4 gam nước. Xác định CTPT của X là:
![]()
![]()
![]()
![]()
Đốt cháy hoàn toàn một lượng hiđrocacbon X thu được 8,4 lít khí CO 2 ở đktc và 5,4 gam nước. Xác định CTPT của X là:
A. C 4 H 6
B. C 5 H 6
C. C 4 H 8
D. C 5 H 8
Đốt cháy hoàn toàn một hidrocacbon X thu được 8,96 lít khí CO2 (đktc) và 9 gam nước. Xác định CTPT của X.
A . C 4 H 10
B . C 5 H 12
C . C 4 H 8
D . C 5 H 10
nCO2 = 0,4 mol => nC = 0,4 mol
nH2O = 0,5 mol => nH = 0,5 . 2 = 1 mol
C : H = 0,4 : 1 = 4 : 10
X là C4H10
Đốt cháy hoàn toàn 4,4 gam Anđehit X thu được 4,48 lít khí co2 (đktc) và 3,6 gam Nước. Xác định CTPT của X
\(n_{CO_2}=0,2\left(mol\right)\Rightarrow n_C=0,2\left(mol\right)\\ n_{H_2O}=0,2\left(mol\right)\Rightarrow n_H=0,4\left(mol\right)\\ n_O=\dfrac{4,4-\left(0,2.12+0,4.1\right)}{16}=0,1\left(mol\right)\\ĐặtCTPTandehitlà:C_xH_yO_z\\ Tacó:x:y:z=0,2:0,4:0,1=2:4:1\\ VậyCTPTandehitlà:C_2H_4O\left(CH_3CHO\right) \)
Đốt cháy hoàn toàn m gam hợp chất hữu cơ A cần dùng 11,2 gam khí oxi, thu được 8,8 gam C O 2 và 5,4 gam H 2 O . Ở đktc 2,24 lít khí A có khối lượng 3 gam. Xác định CTPT của A?
A. C 2 H 6
B. C 2 H 4
C. C 3 H 8
D. C 3 H 6
n O 2 = 11,2/32 = 0,35 mol
n C O 2 = 8,8/44 = 0,2 mol ⇒ n C = 0,2 mol
n H 2 O = 5,4/18 = 0,3 mol
⇒ n H = 2.0,3 = 0,6 mol
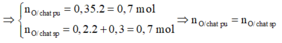
Vậy hợp chất hữu cơ A chỉ có C và H.
Gọi CTTQ của A là C x H y , khi đó ta có:
Vậy CTĐGN của A là C H 3 n
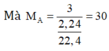
⇒ n = 30/15 = 2
Vậy A là C 2 H 6 .
⇒ Chọn A.
Đốt cháy hoàn toàn 0,1 mol một hiđrocacbon mạch hở X thu được 4,48 lít CO2 (đktc) và 3,6 gam H2O
1. Xác định CTPT, viết CTCT và gọi tên của X.
2. Dẫn 3,36 lít hỗn hợp gồm axetilen và X đi vào một lượng dư dung dịch AgNO3 trong NH3 thấy còn 0,84 lít khí thoát ra và có m gam kết tủa. Các thể tích khí đo ở đktc.
a. Tính phần trăm thể tích của X trong hỗn hợp.
b. Viết PTHH xảy ra và tính m. ( Cho Ag=108, C=12, H=1, O=16) Mọi người giúp mình với ạ, mình cảm ơn
1)
\(n_{CO_2}=\dfrac{4,48}{22,4}=0,2\left(mol\right)\)
=> nC = 0,2 (mol)
Số nguyên tử C = \(\dfrac{0,2}{0,1}=2\) (nguyên tử)
\(n_{H_2O}=\dfrac{3,6}{18}=0,2\left(mol\right)\)
=> nH = 0,4 (mol)
Số nguyên tử H = \(\dfrac{0,4}{0,1}=4\) (nguyên tử)
CTPT: C2H4
CTCT: \(CH_2=CH_2\) (etilen)
2)
a) Khí thoát ra là C2H4
\(\%V_{C_2H_4}=\dfrac{0,84}{3,36}.100\%=25\%\)
b)
PTHH: \(CH\equiv CH+2AgNO_3+2NH_3\rightarrow CAg\equiv CAg\downarrow+2NH_4NO_3\)
\(n_{C_2H_2}=\dfrac{3,36-0,84}{22,4}=0,1125\left(mol\right)\)
=> \(n_{C_2Ag_2}=0,1125\left(mol\right)\)
=> m = 0,1125.240 = 27 (g)
1)
\(n_{CO_2}=\dfrac{4,48}{22,4}=0,2\left(mol\right)\)
=> nC = 0,2 (mol)
Số nguyên tử C = \(\dfrac{0,2}{0,1}=2\) (nguyên tử)
\(n_{H_2O}=\dfrac{3,6}{18}=0,2\left(mol\right)\)
=> nH = 0,4 (mol)
Số nguyên tử H = \(\dfrac{0,4}{0,1}=4\) (nguyên tử)
CTPT: C2H4
CTCT: \(CH_2=CH_2\) (etilen)
2)
đốt cháy hoàn toàn 2 hiđrocacbon đồng đẳng kế tiếp nhau thu được 3,36 lít khí co2(đktc) và 4,5 gam h20.
a) Xác định CTPT của 2 hidrocacbon
B) Tính thể tích của từng khí trong hỗn hợp ở đktc
n CO2=\(\dfrac{3,36}{22,4}\)=0,15 mol
n H2O=\(\dfrac{4,5}{18}\)=0,25 mol
n ankan=0,25-0,15=0,1 mol
C=\(\dfrac{0,15}{0,1}\)=1,5
=>Công thức là CH4 , C2H6
Đốt cháy hoàn toàn 7,4 gam este X, thu được 6,72 lít CO2 (ở đktc) và 5,4 gam H2O. Tìm CTPT của X.
Đốt cháy hoàn toàn 7,4 gam este X đơn chức thu được 6,72 lít CO2 (đktc) và 5,4 gam nước. Xác định công thức phân tử của X.
Ta có:
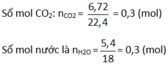
Vì nCO2 = nH2O ⇒ X là este no đơn chức mạch hở. Gọi CTPT của este X là CnH2nO2

⇔ 3(14n + 32) = 74n ⇒ n = 3
⇒ Công thức phân tử của este X là C3H6O2
Đốt cháy hoàn toàn 5,8 gam một ankan thu được 8,96 lít khí CO2 ở đktc a) xác định CTPT, CTCT gọi tên ankan b) đốt cháy hoàn toàn lượng anken trên, dẫn sản phẩm cháy vào Ca(OH)2 dư. Tính khối lượng kết tủa thu được
nCO2=8,96/22,4=0,4 mol
=> nC=nCO2=0,4 mol
mC=0,4.12=4,8g
=> mH=5,8-4,8=1g
nH=1 mol -> nH2O=0,5
nH=0,5 mol
Pt: CnH2n+2 + (3n+1/2)O2-> nCO2 + (n+1)H2O
0,4 0,5 mol
=> n/0,4=n+1/0,5 -> n=4
Vậy cthh cần tìm là C4H10