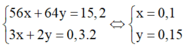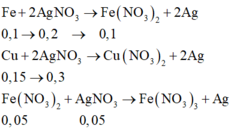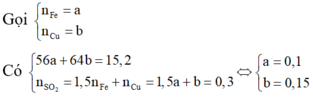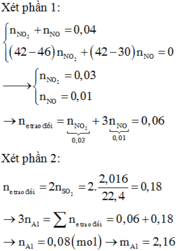Nung m gam hỗn hợp X gồm Al và Fe3O4 trong khí trơ, sau một thời gian, thu được hỗn hợp chất rắn Y. Chia Y thành hai phần bằng nhau. Phần một phản ứng vừa đủ với dung dịch HCl, thu được 50,27 gam muối và thoát ra 5,6 lít H2 (đktc). Phần hai phản ứng với dung dịch NaOH (dư), thu được 3,36 lít H2 (đktc) và còn lại phần rắn Z không tan. Hòa tan hoàn toàn Z trong dung dịch H2SO4 (đặc, nóng, dư), thu được 4,032 lít SO2 (đktc, sản phẩm khử duy nhất của S+6. Phần trăm khối lượng Al đã phản ứng là A. 50...
Đọc tiếp
Nung m gam hỗn hợp X gồm Al và Fe3O4 trong khí trơ, sau một thời gian, thu được hỗn hợp chất rắn Y. Chia Y thành hai phần bằng nhau. Phần một phản ứng vừa đủ với dung dịch HCl, thu được 50,27 gam muối và thoát ra 5,6 lít H2 (đktc). Phần hai phản ứng với dung dịch NaOH (dư), thu được 3,36 lít H2 (đktc) và còn lại phần rắn Z không tan. Hòa tan hoàn toàn Z trong dung dịch H2SO4 (đặc, nóng, dư), thu được 4,032 lít SO2 (đktc, sản phẩm khử duy nhất của S+6. Phần trăm khối lượng Al đã phản ứng là
A. 50,0%.
B. 66,7%.
C. 75,0%.
D. 83,3%.