. Xác định khoảng pH của:
a. nước tinh khiết (nước cất)
b. Nước để lâu trong không khí.
c. Dung dịch NaOH
d. Dung dịch H2SO4 loãng.
e. Dung dịch NaCl f. Dung dịch Ca(OH)2
Nêu phương pháp xác định từng chất trong bốn lọ mất nhãn đựng riêng biệt nước cất dung dịch NaOH, dung dịch H2SO4 và dung dịch NaCL
- Dùng quỳ tím
+) Hóa đỏ: H2SO4
+) Hóa xanh: NaOH
+) Không đổi màu: NaCl và nước cất
- Đổ dd AgNO3 vào 2 lọ còn lại
+) Xuất hiện kết tủa: NaCl
PTHH: \(NaCl+AgNO_3\rightarrow NaNO_3+AgCl\downarrow\)
+) Không hiện tượng: Nước cất
Trích mẫu thử
Cho quỳ tím vào các mẫu thử
Quỳ tím hóa đỏ=>H2SO4
Quỳ tím hóa xanh=>NaOH
Quỳ tím không đổi màu=> H2O và NaCl(*)
Cho AgNO3 vào (*)
Tạo kết tủa trắng=>NaCl
pt: NaCl+AgNO3--->AgCl↓↓+NaNO3
Trình bày phương pháp phân biệt 5 lọ bị mất nhãn chứa 5 hóa chất riêng biệt sau: nước cất, dung dịch NaCl, dung dịch KOH, dung dịch Ca(OH)2, dung dịch H2SO4
- Cho quỳ tím vào các mẫu thử :
+ Quỳ tím chuyển thành màu xanh : Ca(OH)2 ; KOH (I)
+ Quỳ tím chuyển thành màu đỏ : H2SO4
+ Không hiện tượng : NaCl
- Sục khí CO2 qua 2 dd (I)
+ Hiện tượng kết tủa : Ca(OH)2
\(Ca\left(OH\right)_2+CO_2\rightarrow CaCO_3+H_2O\)
+ Không hiện tượng : KOH
Tiến hành các thí nghiệm sau:
(a) Sục khí CO2 dư vào dung dịch NaOH
(b) Cho dung dịch NaOH dư vào dung dịch Ca(HCO3)2.
(c) Cho dung dịch Ba(HCO3)2 dư vào dung dịch H2SO4.
(d) Cho Mg vào dung dịch CuSO4 dư.
(e) Cho Na đến dư vào dung dịch CH3COOH.
(f) Cho 2 ml benzen vào ống nghiệm có chứa 2 ml dung dịch nước Br2, lắc mạnh, sau đó để yên.
Viết phương trình hóa học (nếu có) và xác định các chất có trong dung dịch sau mỗi thí nghiệm. Cho rằng các phản ứng xảy ra hoàn toàn, các chất khí tan trong nước không đáng kể.
(a) CO2 + NaOH → NaHCO3
Dung dịch sau pứ chỉ có NaHCO3
(b) 2NaOH + Ca(HCO3)2 → Na2CO3 + CaCO3 + H2O
Dung dịch sau pứ: (Na2CO3; NaOH dư)
(c) Ba(HCO3)2 + H2SO4 → BaSO4 + 2CO2 + 2H2O
Dung dịch sau pứ: Ba(HCO3)2 dư
(d) Mg + CuSO4 → MgSO4 + Cu
Dung dịch sau pứ: (MgSO4; CuSO4 dư)
(e) Na + H2O → NaOH + ½ H2
NaOH + CH3COOH → CH3COONa + H2O
Dung dịch sau pứ: (NaOH dư; CH3COONa)
(f) Dung dịch sau pứ: (C6H6; Br2/H2O)
Có các dung dịch bị mất nhãn : NaCl, NaOH, H2SO4, Ca(OH)2, nước cất. Nêu phương pháp hóa học để nhận biết mỗi chất, viết PTHH xảy ra.
Trích mẫu thử
Cho quỳ tím vào các mẫu thử
- mẫu thử nào làm quỳ tím hóa đỏ là H2SO4
- mẫu thử nào làm quỳ tím hóa xanh là NaOH và Ca(OH)2. Gọi là nhóm 1
- mẫu thử nào không đổi màu quỳ tím là NaCl và nước cất. Gọi là nhóm 2
Cho dung dịch axit sunfuric vào nhóm 1
- mẫu thử nào xuất hiện kết tủa trắng là Ca(OH)2
\(Ca(OH)_2 + H_2SO_4 \to CaSO_4 + 2H_2O\)
- mẫu thử nào không hiện tượng là NaOH
Cho dung dịch bạc nitrat vào các mẫu thử nhóm 2
- mẫu thử nào tạo kết tủa trắng là NaCl
\(NaCl + AgNO_3 \to AgCl + NaNO_3\)
- mẫu thử nào không hiện tượng là nước cất
Mục đích của việc tách muối ăn (sodium chloride, NaCl) ra khỏi hỗn hợp nước muối (dung dịch sodium chloride, dung dịch NaCl) để thu được
a) Chất không tan
b) Chất tinh khiết là nước (H2O)
c) Hỗn hợp nước muối ( dung dịch sodium chloride, dung dịch NaCl)
d) Chất tinh khiết là muối ăn (sodium chloride, NaCl)
Trong số các chất sau: dung dịch Na2CO3, dung dịch Ca(OH)2, dung dịch NaCl, dung dịch H2SO4, dung dịch Na3PO4. Số chất có khả năng làm mềm nước cứng tạm thời là:
A. 2.
B. 1.
C. 3.
D. 4.
Nước cứng tạm thời là muối của Ca2+ và Mg2+.
Các chất làm mềm nước là: dung dịch Na2CO3, dung dịch Ca(OH)2, dung dịch Na3PO4.
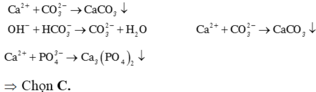
Trong số các chất sau: dung dịch Na2CO3, dung dịch Ca(OH)2, dung dịch NaCl, dung dịch H2SO4, dung dịch Na3PO4. Số chất có khả năng làm mềm nước cứng tạm thời là
A. 2
B. 1
C. 3.
D. 4
Có 4 lọ đựng riêng biệt: nước cất, dung dịch H2SO4, dung dịch NaOH, dung dịch NaCl. Bằng cách nào có thể nhận biết được mỗi chất trong các lọ ?
Trích mẫu thử
Cho quỳ tím vào các mẫu thử
Quỳ tím hóa đỏ=>H2SO4
Quỳ tím hóa xanh=>NaOH
Quỳ tím không đổi màu=> H2O và NaCl(*)
Cho AgNO3 vào (*)
Tạo kết tủa trắng=>NaCl
pt: NaCl+AgNO3--->AgCl↓+NaNO3
a,tính khối lượng NaOH có trong 200ml dung dịch NaOh 1M b,tính số mol H2SO4 có trong 100ml dung dịch H2SO4 2M c,hoà tan 6g NaCl vào nước thu được 200g dung dịch tính nồng độ phần trăm của dung dịch d,tính khối lượng NaCl có trong 200g dung dịch NaCl 8%
a, \(n_{NaOH}=0,2.1=0,2\left(mol\right)\)
\(m_{NaOH}=0,2.40=8\left(g\right)\)
b, \(n_{H_2SO_4}=2.0,1=0,2\left(mol\right)\)
\(c,C\%=\dfrac{6}{200}.100\%=3\%\)
\(m_{NaCl}=\dfrac{200.8}{100}=16\left(g\right)\)