Phản ứng nhiệt phân không đúng là:
A. 2KNO3 → t o 2KNO2 + O2.
B. NH4NO3 → t o N2 + 2H2O.
C. NH4Cl → t o NH3 + HCl.
D. 2NaHCO3 → t o Na2CO3 + CO2 + H2O
Dựa vào sự thay đổi số oxi hóa, tìm chất oxi hóa và chất khử trong những phản ứng sau:
a) 2H2 + O2 → 2H2O.
b) 2KNO3 → 2KNO2 + O2.
c) NH4NO2 → N2 + 2H2O.
d) Fe2O3 + 2Al → 2Fe + Al2O3.
Chất khử và chất oxi hóa trong các phản ứng sau là:
a) 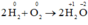 : Chất khử : H2, chất oxi hóa O2
: Chất khử : H2, chất oxi hóa O2
b) 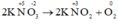 : KNO3 vừa là chất oxi hóa, vừa là chất khử.
: KNO3 vừa là chất oxi hóa, vừa là chất khử.
c) 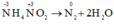
NH4NO2 vừa là chất oxi hóa, vừa là chất khử
d) 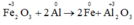
chất khử: Al, chất oxi hóa: Fe2O3
Câu 5. Cho biết các phản ứng sau đây thuộc loại phản ứng nào, phản ứng nào xảy ra sự oxi hóa?
a. 2FeCl2 + Cl2 2FeCl3
b. CuO + H2 Cu + H2O.
c. 2KNO3 2KNO2 + O2
d.2Fe(OH)3 Fe2O3 +3H2O
e. CH4 + 2O2 CO2 + 2H2O
Bạn ưi, bạn có thể ghi đúng đề ra đc ko? PƯHH phải gồm các chất tham gia, chất sản phẩm, phân biệt 2 chất này phải nhờ vào mũi tên, chứ đề ko thấy mũi tên đâu~
a, Phản ứng hóa hợp .
b, Phản ứng oxi hóa - khử .
c, Phản ứng phân hủy .
d, Phản ứng phân hủy .
e, Phản ứng cháy ( tỏa nhiệt )
Câu 5. Cho biết các phản ứng sau đây thuộc loại phản ứng nào, phản ứng nào xảy ra sự oxi hóa?
a. 2FeCl2 + Cl2---> 2FeCl3
b. CuO + H2---> Cu + H2O.
c. 2KNO3---> 2KNO2 + O2
d.2Fe(OH)3---> Fe2O3 +3H2O
e. CH4 + 2O2---> CO2 + 2H2O
trên mỗi dấu---> các bạn tự thêm t độ hộ mình
a) Phản ứng hóa hợp xảy ra sự oxi hóa Fe+2 lên Fe+3
b) Phản ứng trao đổi:
Xảy ra sự oxi hóa H0 lên H+1
c) Phản ứng phân hủy xảy ra sự oxi hóa O-2 lên O 0
d0 Phản ứng phân hủy, không xảy ra sự oxi hóa.
e) Phản ứng cháy, xảy ra sự oxi hóa.
a)FeCl2+ Cl2---> 2FeCl3
=> Phản ứng hóa hợp
b. CuO + H2---> Cu + H2O.
=> Phản ứng thế
c. 2KNO3---> 2KNO2 + O2
=> Phản ứng phân hủy
d.2Fe(OH)3---> Fe2O3 +3H2O
=> Phản ứng phân hủy
e. CH4 + 2O2---> CO2 + 2H2O
=> Phản ứng oxi hóa
trên mỗi dấu---> các bạn tự thêm t độ hộ mình
Chúc bạn học tốt
I. Nhiệt phân hoàn toàn 1 lượng muối KNO3 xảy ra phản ứng sau:
2KNO3 = 2KNO2 + 02
Tính lượng muối cần dùng để thu đc 5,264 lít O2(đktc)
II. Đốt cháy hoàn toàn 2,7g nhôm trong khí O2 dư thấy thu đc 5,1g nhôm oxit. Tìm CTHH của nhôm oxit, bt CT đơn giản cũng chính là CTHH.
III. Cho 6,885g nhôm kim loại phản ứng với dung dịch axit H2SO4 loãng có chứa 34,4g H2SO4 tinh khiết
a) Tính V khí H2 sinh ra (đktc)
b) Để thu đc lượng H2 trên thì phải dùng bn g kim loại sắ cho phản ứng với axit HCl dư
I.
\(2KNO3-->2KNO2+O2\)
\(n_{O2}=\frac{5,264}{22,4}=0,235\left(mol\right)\)
\(\)\(n_{KNO3}=2n_{O2}=0,47\left(mol\right)\)
\(m_{KNO3}=0,47.101=47,47\left(g\right)\)
II.
\(xAl+yO2-->2AlxOy\)
\(n_{Al}=\frac{2,7}{27}=0,1\left(mol\right)\)
\(n_{AlxOy}=\frac{2}{x}n_{Al}=\frac{0,2}{x}\left(mol\right)\)
\(M_{AlxOy}=5,1:\frac{0,2}{x}=25,5x\)
\(x=2,y=3\Rightarrow CTHH:Al2O3\)
III. Cho 6,885g nhôm kim loại phản ứng với dung dịch axit H2S
O4 loãng có chứa 34,4g H2SO4 tinh khiết
a) Tính V khí H2 sinh ra (đktc)
b) Để thu đc lượng H2 trên thì phải dùng bn g kim loại sắ cho phản ứng với axit HCl dư
a) \(2Al+3H2SO4-->Al2\left(SO4\right)3+3H2\)
\(n_{Al}=\frac{6,885}{27}=0,255\left(mol\right)\)
\(n_{H2SO4}=\frac{34,4}{98}=0,35\left(mol\right)\)
\(\frac{0,255}{2}>\frac{0,35}{3}\Rightarrow Aldư\)
\(n_{H2}=n_{H2SO4}=0,35\left(mol\right)\)
\(V_{H2}=0,35.22,4=7,84\left(l\right)\)
b) \(Fe+2HCl--.>FeCl2+H2\)
\(n_{Fe}=n_{H2}=0,35\left(mol\right)\)
\(m_{Fe}=0,35.56=19,6\left(g\right)\)
I. Đốt cháy hoàn toàn 2,7g nhôm trong khí O2 dư thấy thu đc 5,1g nhôm oxit. Tìm CTHH của nhôm oxit, bt CT đơn giản cũng chính là CTHH.
II. Cho 6,855g nhôm kim loại phản ứng với dung dịch axit H2SO4 loãng có chứa 34,4g H2SO4 tinh khiết[Sinh ra Al2(SO4)3 và giải phóng khí hidro].
a) Tính V khí hidro sinh ra (đktc)
b) Để thu đc lượng hidro trên thì phải dùng bn g kim loại sắt cho phản ứng với axit HCl dư
III. Nhiệt phân hoàn toàn 1 lượng muối KNO3 xảy ra phản ứng sau: 2KNO3 = 2KNO2 + O2
Tính lượng muối cần dùng để thu đc 5,264 lít O2(đktc)
Trong các phản ứng sau: (a) Nhiệt phân KClO 3 có xúc tác MnO 2 ; (b) nhiệt phân CaCO 3 ; (c) nhiệt phân KMnO 4 ; (d) nhiệt phân NH 4 NO 3 ; (e) nhiệt phân AgNO 3 , có bao nhiêu phản ứng là phản ứng oxi hóa – khử nội phân tử ?
A. 2.
B. 3.
C. 4.
D. 5.
Đáp án C
4 phản ứng oxi hóa – khử nội phân tử là (a), (c), (d), (e).
Trong các phản ứng sau: (a) Nhiệt phân KClO3 có xúc tác MnO2; (b) nhiệt phân CaCO3; (c) nhiệt phân KMnO4; (d) nhiệt phân NH4NO3; (e) nhiệt phân AgNO3, có bao nhiêu phản ứng là phản ứng oxi hóa – khử nội phân tử ?
A. 2.
B. 3.
C. 4.
D. 5
Đáp án C
4 phản ứng oxi hóa – khử nội phân tử là (a), (c), (d), (e).
Trong các phản ứng sau: (a) Nhiệt phân KClO3 có xúc tác MnO2; (b) nhiệt phân CaCO3; (c) nhiệt phân KMnO4; (d) nhiệt phân NH4NO3; (e) nhiệt phân AgNO3, có bao nhiêu phản ứng là phản ứng oxi hóa – khử nội phân tử ?
A. 2.
B. 3.
C. 4.
D. 5.
Chọn C
(a) Nhiệt phân KClO3 có xúc tác MnO2,
(c) nhiệt phân KMnO4;
(d) nhiệt phân NH4NO3;
(e) nhiệt phân AgNO3
Cho các phản ứng sau:
a A g N O 3 → t ° b N H 4 C l + N a N O 2 → t °
c N H 3 + C u O → t ° d N H 4 N O 3 → t °
e N H 3 + O 2 → P t , t ° f N H 4 N O 3 + N a O H → t °
Số phản ứng tạo ra khí N2 là
A. 2.
B. 3.
C. 4.
D. 5.
Chọn A.
(a) 2 A g N O 3 → t ° 2Ag + 2NO2 + O2
(b) 2 N H 4 C l + 2 N a N O 2 → t ° 2NaCl + N2 + 4H2O
(c) 2 N H 3 + 3 C u O → t ° N2 + 3Cu + 3H2O
(d) N H 4 N O 3 → t ° N2O + 2H2O
(e) 4 N H 3 + 5 O 2 → P t , t ° 4NO + 6H2O
(f) N H 4 N O 3 + N a O H → t ° NH3 + NaNO3 + H2O
Trong các phản ứng sau: Nhiệt phân KClO3 có xúc tác MnO2; nhiệt phân CaCO3; nhiệt phân KMnO4; nhiệt phân NH4NO3; nhiệt phân AgNO3, có bao nhiêu phản ứng là phản ứng nội oxi hóa khử?
A. 2
B. 3
C. 4
D. 5