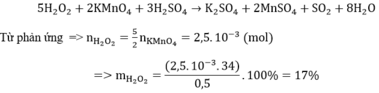Để xác định hàm lượng của Ag trong hợp kim người ta hòa tan 0,5 gam hợp kim đó vào dung dịch axit nitric. Cho thêm dung dịch axit clohidric vào dung dịch trên thu được 0,398 gam kết tủa. Tính hàm lượng A trong hợp kim.

Những câu hỏi liên quan
Để xác định hàm lượng của Ag trong hợp kim người ta hòa tan 0,5 gam hợp kim đó vào dung dịch axit nitric. Cho thêm dung dịch axit clohidric vào dung dịch trên thu được 0,398 gam kết tủa. Tính hàm lượng A trong hợp kim.
Ag → Ag+ + 1e
Ag+ + HCl → AgCl ↓ + H+
Số mol kết tủa là
nAgCl = 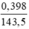 (mol)
(mol)
Theo pt nAg = nAg+ = nAgCl = 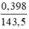 (mol)
(mol)
Khối lượng Ag là: mAg = 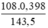 = 0,3 (g)
= 0,3 (g)
%mAg= 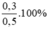 = 60%
= 60%
Đúng 0
Bình luận (0)
Để xác định hàm lượng của bạc trong hợp kim, người ta hoà tan 0,5 gam hợp kim đó vào dung dịch axit nitric. Cho thêm dung dịch axit HCl dư vào dung dịch trên, thu được 0,398 gam kết tủa. Tính hàm lượng của bạc trong hợp kim.
Đọc tiếp
Để xác định hàm lượng của bạc trong hợp kim, người ta hoà tan 0,5 gam hợp kim đó vào dung dịch axit nitric. Cho thêm dung dịch axit HCl dư vào dung dịch trên, thu được 0,398 gam kết tủa. Tính hàm lượng của bạc trong hợp kim.
Ag + 2 HNO3 → AgNO3 + NO2 + H2O (1)
AgNO3 + HCl → AgCl + HNO3 (2)
Từ (1) và (2), ta có: nAg = = 0,00277 (mol)
=> %mAg= .100% = 59,9%
Đúng 0
Bình luận (0)
Để xác định nồng độ dung dịch H2O2 , người ta hòa tan 0,5 gam nước oxi già vào nước, thêm H2SO4 tạo môi trường axit. Chuẩn độ dung dịch thu được cần vừa đủ 10 ml dung dịch KMnO4 0,1M . Xác định hàm lượng H2O2 trong nước oxi già. A. 9% B. 17% C. 12% D. 21%
Đọc tiếp
Để xác định nồng độ dung dịch H2O2 , người ta hòa tan 0,5 gam nước oxi già vào nước, thêm H2SO4 tạo môi trường axit. Chuẩn độ dung dịch thu được cần vừa đủ 10 ml dung dịch KMnO4 0,1M . Xác định hàm lượng H2O2 trong nước oxi già.
A. 9%
B. 17%
C. 12%
D. 21%
Hòa tan 5,94 gam hỗn hợp 2 muối clorua của 2 kim loại A, B (đều có hoá trị II) vào nước được dung dịch X. Để làm kết tủa hết ion Cl- có trong dung dịch X người ta cho dung dịch X tác dụng với dung dịch AgNO3 thu được 17,22 gam kết tủa. Xác định công thức hóa học của 2 muối chloride
Đọc tiếp
Hòa tan 5,94 gam hỗn hợp 2 muối clorua của 2 kim loại A, B (đều có hoá trị II) vào nước được dung dịch X. Để làm kết tủa hết ion Cl- có trong dung dịch X người ta cho dung dịch X tác dụng với dung dịch AgNO3 thu được 17,22 gam kết tủa. Xác định công thức hóa học của 2 muối chloride
Hòa tan hòa toàn a gam kim loại M (có hóa trị không đổi) vào b gam dung dịch HCl thu được dung dịch D. Thêm 179,88 gam dung dịch NaHCO3 9,34% vào dung dịch D thì vừa đủ tác dụng hết với lượng HCl dư, thu được dung dịch E. Trong dung dịch E nồng độ phần trăm của NaCl và muối clorua của kim loại M tương ứng là 2,378% và 7,724%. Thêm tiếp một lượng dư dung dịch NaOH vào E, sau đố lọc kết tủa rồi nung đến khối lượng không đổi thì thu được 16,0 gam chất rắn. Xác định kim loại M và nồng độ phần trăm c...
Đọc tiếp
Hòa tan hòa toàn a gam kim loại M (có hóa trị không đổi) vào b gam dung dịch HCl thu được dung dịch D. Thêm 179,88 gam dung dịch NaHCO3 9,34% vào dung dịch D thì vừa đủ tác dụng hết với lượng HCl dư, thu được dung dịch E. Trong dung dịch E nồng độ phần trăm của NaCl và muối clorua của kim loại M tương ứng là 2,378% và 7,724%. Thêm tiếp một lượng dư dung dịch NaOH vào E, sau đố lọc kết tủa rồi nung đến khối lượng không đổi thì thu được 16,0 gam chất rắn. Xác định kim loại M và nồng độ phần trăm của dung dịch axit clohiđric đã dùng?

BTKL: mD + mNaHCO3 = mCO2 + mE
mD + 179,88 = 44.0,2 + 492 => mD = 320,92
BTKL: mMg + mddHCl = mH2 + mD
=> 24 . 0,4 + mddHCl = 2 . 0,4 + 320,92 => mddHCl = 312,12
=> C%HCl = 11,69%
Đúng 0
Bình luận (0)
Cho một thanh hợp kim nặng 8,8 gam chứa các kim loại Ag, Fe, Mg hòa tan trong 750 ml CuSO4 0,1M. Sau một thời gian, thu được thanh hợp kim X và dung dịch Y. Rửa sạch và sấy khô thanh hợp kim X và cân thấy khối lượng tăng thêm so với thanh hợp kim ban đầu là 1,16 gam. Nhúng thanh X vào dung dịch H2SO4 đặc nóng dư thì thu được 2,576 lít khí SO2 (đktc). Cho 800 ml dung dịch NaOH 0,2M vào dung dịch Y, lọc lấy kết tủa rửa sạch, nung trong không khí đến khối lượng không đổi thu được 5 gam chất rắn. Ph...
Đọc tiếp
Cho một thanh hợp kim nặng 8,8 gam chứa các kim loại Ag, Fe, Mg hòa tan trong 750 ml CuSO4 0,1M. Sau một thời gian, thu được thanh hợp kim X và dung dịch Y. Rửa sạch và sấy khô thanh hợp kim X và cân thấy khối lượng tăng thêm so với thanh hợp kim ban đầu là 1,16 gam. Nhúng thanh X vào dung dịch H2SO4 đặc nóng dư thì thu được 2,576 lít khí SO2 (đktc). Cho 800 ml dung dịch NaOH 0,2M vào dung dịch Y, lọc lấy kết tủa rửa sạch, nung trong không khí đến khối lượng không đổi thu được 5 gam chất rắn. Phần trăm khối lượng của Ag trong hợp kim là:
A. 61,36%
B. 36,82%
C. 49,09%
C. 49,09%
Đáp án A
Nếu Mg còn dư trong phản ứng
=> mthanh hợp kim tăng = (64-24).0,075=3g > 1,16 g
=> Chứng tỏ Mg phản ứng hết.
Đặt số mol Mg và Fe phản ứng lần lượt là x, y.
=> mthanh hợp kim tăng =x(64-24)+y(64-56)=1,16g
Có ![]()
=> NaOH phản ứng với Y còn dư => 5 gam chất rắn gồm MgO, Fe2O3, có thể có CuO
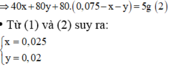
Đặt số mol Al và Fe còn dư lần lượt là a, b
=> mthanh hợp kim = 108a+24.0,025+56.(0,02+b)=8,8g
→ BTe a + 3 b + 2 . ( 0 , 025 + 0 , 02 ) = 2 . n S O 2 = 2 . 2 , 576 22 , 4 = 0 , 23 m o l

Đúng 0
Bình luận (0)
A là hỗn hợp hai kim loại Ba và Mg, cho a gam A vào nước dư thì thu được 2,24 lít khí hidro (đktc). CŨng cho a gam A nhưng cho vào dung dịch axit clohidric dư thì thu được 4,48 lít khí hidro và một dung dịch B.
a) Tính a
b) Thêm vào B 0,1 mol axit sunfuric, sau đó thêm 0,3 mol natri hidroxit. Tính khối lượng phần kết tủa thu được
a. Lúc cho A vào nước:
\(Ba+2H_2O\rightarrow Ba\left(OH\right)_2+H_2\uparrow\left(1\right)\)
Theo phương trình (1)
\(n_{Ba}=n_{H_2\left(1\right)}=\dfrac{2,24}{22,4}=0,1mol\)
Lúc cho A vào HCl dư:
\(Ba+2HCl\rightarrow BaCl_2+H_2\uparrow\left(2\right)\)
\(Mg+2HCl\rightarrow MgCl_2+H_2\uparrow\left(3\right)\)
\(n_{H_2\left(2+3\right)}=\dfrac{4,48}{22,4}=0,2mol\)
\(\rightarrow n_{Ba}+n_{Mg}=0,2mol\)
\(\rightarrow n_{Mg}=0,1mol\)
\(\rightarrow a=m_A=0,1.24+0,1.137=16,1g\)
b. Dung dịch B:
\(MgCl_2:0,1mol\) và \(BaCl_2:0,1mol\)
\(BaCl_2+H_2SO_4\rightarrow BaSO_4\downarrow+2HCl\)
Xét \(n_{BaCl_2}=n_{H_2SO_4}\rightarrow P/ứ\) hoàn toàn
\(HCl+NaOH\rightarrow NaCl+H_2O\)
\(MgCl_2+2NaOH\rightarrow Mg\left(OH\right)_2\downarrow+2NaCl\)
Từ các phương trình \(n_{BaSO_4}=0,1mol;n_{Mg\left(OH\right)_2}=0,05mol\)
\(\rightarrow m\downarrow=0,1.233+0,05.58=26,2g\)
Đúng 0
Bình luận (0)
Hào tan 10 gam dung dịch axit sunfuric vào côc đựng sẵn 100gam nc. Cho tiếp vào cốc 20 gam dung dịch bari clorua thấy có kết tủa trắng xuất hiện, cho thêm 0,65 gam kim loại kẽm vào cốc, kẽm tan hết và thấy có khí thoát ra. Khối lượng khí thoát ra xác định được là 0,02 gam. Lọc kết tủa cân được 2gam. Xác định khối lượng dung dịch còn lại?
mdd = 10 + 100 + 20 + 0,65 - 0,02 - 2 = 130,43 g.
Đúng 0
Bình luận (0)
Hòa tan 5,94 gam hỗn hợp 2 muối clorua của 2 kim loại A, B (đều có hoá trị II) vào nước được dung dịch X. Để làm kết tủa hết ion Cl- có trong dung dịch X người ta cho dung dịch X tác dụng với dung dịch AgNO3 thu được 17,22 gam kết tủa. Lọc bỏ kết tủa, thu được dung dịch Y. Cô cạn Y được m gam hỗn hợp muối khan. Giá trị m là A. 6,36 g. B. 63,6 g. C. 9,12g. D. 91,2g.
Đọc tiếp
Hòa tan 5,94 gam hỗn hợp 2 muối clorua của 2 kim loại A, B (đều có hoá trị II) vào nước được dung dịch X. Để làm kết tủa hết ion Cl- có trong dung dịch X người ta cho dung dịch X tác dụng với dung dịch AgNO3 thu được 17,22 gam kết tủa. Lọc bỏ kết tủa, thu được dung dịch Y. Cô cạn Y được m gam hỗn hợp muối khan. Giá trị m là
A. 6,36 g.
B. 63,6 g.
C. 9,12g.
D. 91,2g.
Áp dụng phương pháp tăng giảm khối lượng:
Cứ 1 mol MCl2 → 1 mol M(NO3)2 và 2 mol AgCl thì m tăng 2.62 - 2.35,5 = 53 gam
Phản ứng tạo 0,12 mol AgCl có khối lượng muối tăng 3,18 gam
mmuối nitrat = mmuối clorua + mtăng = 5,94 + 3,18 = 9,12 (gam)
Đáp án C
Đúng 0
Bình luận (0)