Cho 6,72 gam hỗn hợp A gồm Mg, Fe và Ni tan trong 200ml dung dịch B chứa HCl, HBr và H2SO4 loãng, kết thúc phản ứng thu được 2,24 lít H2 (đktc)
pH của dung dịch B là:
A. 2
B. 3
C. l
D. 0
Cho 6,72 gam hỗn hợp A gồm Mg, Fe và Ni tan trong 200ml dung dịch B chứa HCl, HBr và H2SO4 loãng, kết thúc phản ứng thu được 2,24 lít H2 (đktc). Khi kết thúc các phản ứng:
A. Kim loại trong A hết và axit trong B cũng hết.
B. Kim loại dư, axit trong B hết.
C. Kim loại hết, axit trong B dư.
D. Kim loại hết hay dư phụ thuộc tỉ lệ mol các axit trong dung dịch B.
![]()
Hỗn hợp A gồm 3 kim loại là Mg, Fe, Ni với kim loại có khối lượng mol lớn nhất là Ni nên
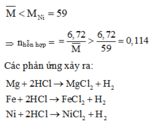
⇒ n H + cần để hòa tan kim loại > 2.0,114 = 0,228 > 0,2 = n H + phản ứng
Do đó sau phản ứng axit hết, kim loại còn dư.
Đáp án b
Cho 6,72 gam hỗn hợp A gồm Mg, Fe và Ni tan trong 200ml dung dịch B chứa HCl, HBr và H2SO4 loãng, kết thúc phản ứng thu được 2,24 lít H2 (đktc)
Khi kết thúc các phản ứng:
A. Kim loại trong A hết và axit trong B cũng hết.
B. Kim loại dư, axit trong B hết.
C. Kim loại hết, axit trong B dư.
D. Kim loại hết hay dư phụ thuộc tỉ lệ mol các axit trong dung dịch B.
Đáp án B
Có nH+ phản ứng = 2 n H 2 = 0,2
Hỗn hợp A gồm 3 kim loại là Mg, Fe, Ni với kim loại có khối lượng mol lớn nhất là Ni nên
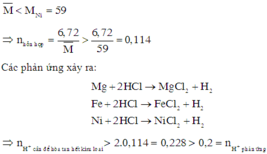
Do đó sau phản ứng axit hết, kim loại còn dư.
Hòa tan 10 gam hỗn hợp chất rắn gồm Fe, FeO và Cu vào dung dịch HCl loãng dư. Kết thúc phản ứng thấy có 2,24 lít khí H 2 (đktc) thoát ra và thu được dung dịch B và 0,8 gam chất rắn C. Cô cạn dung dịch B thu được m gam muối. Gía trị của m là:
A. 19,00 gam
B. 19,05 gam
C. 20 gam
D. 20,05 gam
Chọn B
Cho hỗn hợp chất rắn phản ứng với HCl dư có Cu không phản ứng.
Phương trình hóa học:
F e + 2 H C l → F e C l 2 + H 2 F e O + 2 H C l → F e C l 2 + H 2 O

Hỗn hợp A gồm hai kim loại Mg và Zn. Dung dịch B là dung dịch HCl nồng độ a mol/lít.
Thí nghiệm 1: Cho 8,9 gam hỗn hợp A vào 2 lít dung dịch B, kết thúc phản ứng thu được 4,48 lít H2 (đktc).
Thí nghiệm 2: Cho 8,9 gam hỗn hợp A vào 3 lít dung dịch B, kết thúc phản ứng cũng thu được 4,48 lít H2 (đktc).
Giá trị của a là:
A. 0,1
B. 0,15
C. 0,05
D. 0,3
Đáp án D
Nhận thấy ở hai thí nghiệm có lượng kim loại tham gia phản ứng như nhau, lượng HCl sử dụng lớn hơn lượng HCl sử dụng ở thí nghiệm 1 nhưng lượng H2 ở hai thí nghiệm thu được như nhau.
Do đó ở thí nghiệm 2 HCl phản ứng dư, thí nghiệm 1 có HCl phản ứng đủ hoặc dư.
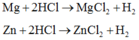
Có
![]()
Quan sát 4 đáp án nhận thấy chỉ có giá trị 0,3 là phù hợp.
Cho m gam hỗn hợp X gồm Cu và Fe vào dung dịch H2SO4 loãng (dư) , kết thúc phản ứng thu được 2,24 lít khí H2 (đktc). Khối lượng của Fe trong 2m gam X là
A. 1,12 gam.
B. 16,8 gam.
C. 11,2 gam.
D. 4,48 gam.
Ta có nFe/m gam = nH2 = 0,1 mol.
⇒ mFe/m gam = 5,6 gam ⇒ mFe/2m gam = 11,2 gam
Đáp án C
Cho m gam hỗn hợp X gồm Cu và Fe vào dung dịch H2SO4 loãng (dư), kết thúc phản ứng thu được 2,24 lít khí H2 (đktc). Khối lượng của Fe trong 2m gam X là
A. 4.48.
B. 11,2.
C. 16,8.
D. 1,12.
Đáp án B
+ Khi cho X phản ứng với dung dịch H2SO4 loãng chỉ có Fe tham gia phản ứng.
+ T r o n g m g a m X : B T E ⇒ n F e = n H 2 = 0 , 1 m o l ⇒ m F e = 5 , 6 g a m . ⇒ m F e t r o n g 2 m g a m X = 5 , 6 . 2 = 11 , 2 g a m
Cho m gam hỗn hợp X gồm Cu và Fe vào dung dịch H2SO4 loãng (dư) , kết thúc phản ứng thu được 2,24 lít khí H2 (đktc). Khối lượng của Fe trong 2m gam X là
A. 4,48
B. 11,2
C. 16,8
D. 5,6
Cho m gam hỗn hợp X gồm Cu và Fe vào dung dịch H2SO4 loãng (dư), kết thúc phản ứng thu được 2,24 lít khí H2 (đktc). Khối lượng của Fe trong 2m gam X là
A. 1,12 gam
B. 16,8 gam
C. 11,2 gam
D. 4,48 gam
Đáp án C
Ta có nFe/m gam = nH2 = 0,1 mol.
⇒ mFe/m gam = 5,6 gam ⇒ mFe/2m gam = 11,2 gam
Cho m gam hỗn hợp X gồm Cu và Fe vào dung dịch H2SO4 loãng (dư) kết thúc phản ứng thu được 2,24 lít khí H2 (đktc). Khối lượng Fe trong m gam X là:
A. 2,8 gam
B.16,8 gam
C. 11,2 gam
D.5,6 gam