Cho 0,2 gam một kim loại thuộc nhóm IIA tác dụng hết với dung dịch HCl thấy tạo ra 0,555 gam muối. Kim loại đó là
A. Be.
B. Mg.
C. Ba.
D. Ca.
Cho 2 kim loại nhóm IIA tác dụng hết với dung dịch HCl tạo ra 5,55g muối clorua. Kim loại đó là kim loại nào sau đây?
A. Be.
B. Mg.
C. Ca.
D. Ba.
Đáp án C.
Gọi M là kim loại nhóm II, số mol là x
M + 2HCl → MCl2 + H2
x x(mol)
theo bài ra ta có hệ pt
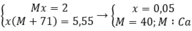
Vậy M là Ca
Cho 2 gam một kim loại thuộc nhóm IIA tác dụng hết với dung dịch HCl tạo ra 5,55 gam muối clorua. Kim loại đó là kim loại nào sau đây.
A. Ba
B. Mg
C. Ca
D. Be
Đáp án C
Gọi kim loại nhóm IIA là M: M + 2HCl → MCl2 + H2
Mol x → 2x → x
Bảo toàn khối lượng: mM + mHCl = mmuối + mH2
=> 2 + 36,5.2x = 5,55 + 2x
=> x = 0,05 mol
=> MM = m: n = 2: 0,05 = 40 g/mol (Ca)
Cho 2 gam một kim loại thuộc nhóm IIA tác dụng hết với dung dịch HCl tạo ra 5,55 gam muối clorua. Kim loại đó là kim loại nào sau đây?
A. Be; B. Mg; C. Ca; D. Ba.
Chọn C.
M + 2HCl → MCl2 + H2
NCl- trong muối = = 0,1 (mol) => M =
= 40 (g/mol)
Kim loại là Ca.
Cho 1,67 gam hỗn hợp gồm hai kim loại ở 2 chu kỳ liên tiếp thuộc nhóm IIA (phân nhóm chính nhóm II) tác dụng hết với dung dịch HCl (dư), thoát ra 0,672 lít khí H2 (ở đktc). Hai kim loại đó là (cho Be = 9, Mg = 24, Ca = 40, Sr = 87, Ba = 137)
A. Ca và Sr
B. Sr và Ba
C. Mg và Ca
D. Be và Mg
Đáp án A
Kim loại nhóm IIA, có mức oxi hóa = +2 trong hợp chất
nH2 = 0,03 mol
Gọi X là kí hiệu chung của 2 kim loại
X + 2HCl → XCl2 + H2
0,03 ← 0,03 (mol)
⇒ M = 55,6
MCa = 40 < 55,67 < MSr = 88
. Cho 8 gam một kim loại R thuộc nhóm IIA tác dụng hết với nước tạo ra 4,48 lít khí hiđro (đktc). Tìm tên kim loại R. (biết Mg=24, Be=9, Ca=40, Ba=137)
$R + 2HCl \to RCl_2 + H_2$
$n_{H_2} = \dfrac{4,48}{22,4} = 0,2(mol)$
Theo PTHH : $n_R = n_{H_2} = 0,2(mol)$
$\Rightarrow M_R = \dfrac{8}{0,2} = 40$
Vậy R là Canxi
Cho 2 kim loại nhóm IIA tác dụng hết với dung dịch HCl tạo ra 5,55g muối clorua. Kim loại đó là kim loại nào sau đây?
A. Be.
B. Mg.
C. Ca.
D. Ba.
Đáp án C
Gọi M là kim loại nhóm II, số mol là x
M + 2HCl " MCl2 + H2
x(mol) x(mol)
Theo đề bài ra ta có hệ phương trình:
(tham khảo)
Cho 2,2 gam một hỗn hợp gồm 2 kim loại ở hai chu kì liên tiếp thuộc nhóm IIA tác dụng với dung dịch HCl dư cho 1,68 lít khí hidro ( đktc ) . Xác định hai kim loại . ( Be = 9 , Mg = 24 , Ca = 40 , Sr = 87 , Ba = 137 )
Gọi nguyên tử khối trung bình của 2 kim loại cần tìm là R
\(R+2HCl\rightarrow RCl_2+H_2\\ n_R=n_{H_2}=0,075\left(mol\right)\\ \Rightarrow M_R=\dfrac{2,2}{0,075}=29,33\\ \Rightarrow2kimloạicầntìmlà:Mg,Ca\)
Câu 12. Cho 2,4 gam kim loại M thuộc nhóm IIA trong bảng tuần hoàn tác dụng với HCl thu được 2,24 lít khí (dktc). M là
A. Be (M=9). B. Mg (M=24). C. Ca (M=40). D. Ba( M=137).
Gọi x là hóa trị của M
PTHH: M + xHCl ---> MClx + \(\dfrac{x}{2}\)H2
Ta có: \(n_{H_2}=\dfrac{2,24}{22,4}=0,1\left(mol\right)\)
Theo PT: \(n_M=\dfrac{1}{\dfrac{x}{2}}.n_{H_2}=\dfrac{2}{x}.0,1=\dfrac{0,2}{x}\left(mol\right)\)
=> \(M_M=\dfrac{2,4}{\dfrac{0,2}{x}}=\dfrac{2,4x}{0,2}=12x\left(g\right)\)
Biện luận:
| x | 1 | 2 | 3 | 4 |
| M | 12 | 24 | 36 | 48 |
| loại | Mg | loại | loại |
Vậy M là magie (Mg)
Chọn B
Cho 1,67 gam hỗn hợp gồm hai kim loại ở 2 chu kỳ liên tiếp thuộc nhóm IIA tác dụng hết với H2O (dư), thoát ra 0,672 lít khí H2 (ở đktc). Hai kim loại đó là (cho Be = 9, Mg = 24, Ca = 40, Sr = 87, Ba = 137)
A. Be và Mg
B. Mg và Ca
C. Sr và Ba
D. Ca và Sr