Khi lấy cùng số mol H2SO4 tác dụng hoàn toàn với mỗi chất sau đây thì trường hợp thu được lượng CuSO4 ít nhất là
A. H2SO4 đặc + Cu →
B. H2SO4 + CuCO3 →
C. H2SO4 + CuO →
D. H2SO4 + Cu(OH)2 →
cho 12gam hỗn hợp cu và cuo tác dụng hoàn toàn với dung dịch hcl loãng sau phản ứng thấy còn lại m gam chất rắn không tan, lọc lấy lượng chất rắn này vào dung dịch h2so4 đặc nóng thì thu được 2,24 lít khi so2
Dãy chất nào sau đây tác dụng được với Al ? *
A HCl, MgCl2, S.
B H2SO4 đặc nguội, Cl2, Cu(NO3)2.
C H2SO4 loãng, NaOH, CuCl2.
D HCl, Cl2, Cu(OH)2.
Chọn C
\(2Al+3H_2SO_4\to Al_2(SO_4)_3+3H_2\\ Al+NaOH+H_2O\to NaAlO_2+\dfrac{3}{2}H_2\\ 2Al+3CuCl_2\to 2AlCl_3+3Cu\)
cho 10g hỗn hợp Cu, CuO tác dụng vừa đủ với dd H2SO4 24,5%, lọc lấy chất rắn không tan cho vào dung dịch H2SO4 đặc,nóng dư thu được 1,12l khí A. Tính khối lượng dd H2SO4 24,5% đã dùng
\(CuO+H_2SO_{4\left(24,5\%\right)}\rightarrow CuSO_4+H_2O\)
\(Cu+2H_2SO_{4đ}\underrightarrow{t^o}CuSO_4+SO_2+2H_2O\)
\(n_{SO_2}=\dfrac{1,12}{22,4}=0,05\left(mol\right)\)
\(\Rightarrow n_{Cu}=0,05\left(mol\right)\)
\(\Rightarrow m_{CuO}=10-64.0,05=6,8\left(g\right)\)
\(\Rightarrow n_{CuO}=0,085\left(mol\right)\)
\(\Rightarrow n_{H_2SO_4\left(24,5\%\right)}=0,085\left(mol\right)\)
\(\Rightarrow m_{H_2SO_4\left(24,5\%\right)}=8,33\left(g\right)\)
\(\Rightarrow m_{ddH_2SO_4\left(24,5\%\right)}=34\left(g\right)\)
Cho 10g hỗn hợp Cu, CuO tác dụng vừa đủ với dd H2SO4 24,5%, lọc lấy chất rắn không tan cho vào dung dịch H2SO4 đặc, nóng dư thu được 1,12 lít khí A (đktc) a) Tính thành phần % khối lượng các chất trong hỗn hợp? b) Tính khối lượng dung dịch H2SO4 24,5% đã dùng?
hòa tan hoàn toàn 18,4g hỗn hợp Fe và Cu vào CuSO4 đặc nóng thì thu được 8,96l SO2.
a) tính %khối lượng mỗi kim loại trong hỗn hợp.
b) tính thể tích H2 thoát ra khi cho hh trên tác dụng với H2SO4 loãng
a) nFe = x mol ; nCu = y mol
Ta có: nSO2 = 0,4 mol
e cho: Fe0 - 3e → Fe3+
x mol → 3x mol → x mol
Cu0 - 2e → Cu2+
y mol → 2y mol → y mol
e nhận: S6+ + 2e → S4+
0,4 mol → 0,8 mol → 0,4 mol
Theo định luật bảo toàn electron, ta có: tổng số mol e cho = tổng số mol e nhận→ 3x + 2y = 0,8 (1)
Khối lượng hỗn hợp ban đầu: mFe + mCu = 18,4 (g)→ 56x + 64y = 18,4 (2)
Giải hệ hai phương trình (1) và (2), ta được: x = 0,18 mol ; y = 0,13 mol
mFe = 0,18 x 56 = 10,08 (g) → %mFe = 54,78% → %mCu = 100% - %mFe = 45,22%
b) Theo định luật bảo toàn electron, ta có: tổng số mol e cho = tổng số mol e nhận
→ ne nhận= 3x + 2y = 0,8
2H+ + 2e → H2
0,8 mol → 0,4 mol
VH2= 8,96 (l)
Hòa tan hoàn toàn hỗn hợp X gồm Cu, CuO, Cu(NO3)2 (trong đó số mol Cu bằng số mol CuO) vào 350 ml dung dịch H2SO4 2M (loãng), thu được dung dịch X chỉ chứa một chất tan duy nhất và có khí NO thoát rA. Phần trăm khối lượng Cu trong X có giá trị gần nhất với giá trị nào sau đây?
A. 23,8%.
B. 30,97%
C. 26,9%
D. 19,28%.
Đáp án B
nCu = nCuO = x; nCu(NO3)2 = y
Dung dịch X chỉ chứa 1 chất tan (CuSO4) => Ion NO3- đã hết
3Cu + 8H+ + 2NO3-→ 3Cu2+ + 2NO + 4H2O
3y ← 8y ← 2y
O2- + 2H+→ H2O
x → 2x
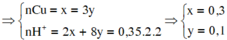
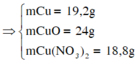
=> %mCu = 30,968% => Chọn B.
Hòa tan hoàn toàn hỗn hợp X gồm Cu, CuO, Cu(NO3)2 (trong đó số mol Cu bằng số mol CuO) vào 350 ml dung dịch H2SO4 2M (loãng), thu được dung dịch X chỉ chứa một chất tan duy nhất, và có khí NO thoát ra. Phần trăm khối lượng Cu trong X có giá trị gần nhất với giá trị nào sau đây?
A. 23,8 %.
B. 26,90%.
C. 30,97%.
D. 19,28%
Hòa tan hoàn toàn hỗn hợp X gồm Cu, CuO, Cu(NO3)2 (trong đó số mol Cu bằng số mol CuO) vào 350 ml dung dịch H2SO4 2M (loãng), thu được dung dịch X chỉ chứa một chất tan duy nhất, và có khí NO thoát ra. Phần trăm khối lượng Cu trong X có giá trị gần nhất với giá trị nào sau đây?
A. 23,80%.
B. 30,97%.
C. 26,90%.
D. 19,28%.
Hòa tan hoàn toàn hỗn hợp X gồm Cu, CuO, Cu(NO3)2 (trong đó số mol Cu bằng số mol CuO) vào 350 ml dung dịch H2SO4 2M (loãng), thu được dung dịch X chỉ chứa một chất tan duy nhất, và có khí NO thoát ra. Phần trăm khối lượng Cu trong X có giá trị gần nhất với giá trị nào sau đây?
![]()
![]()
![]()
![]()