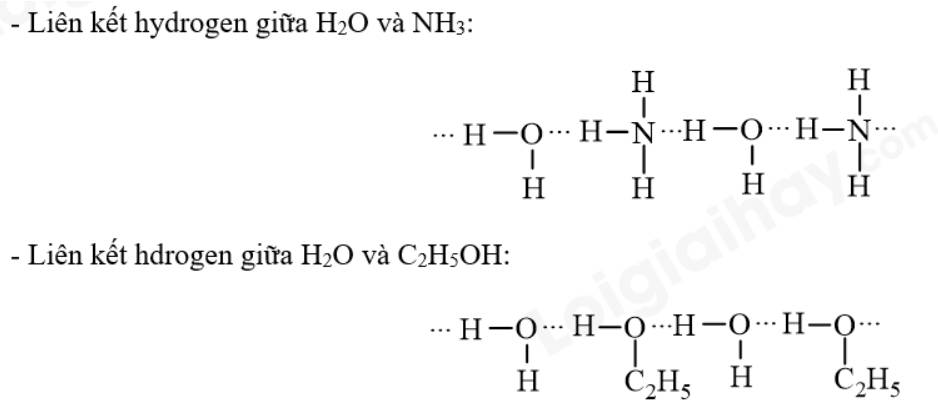
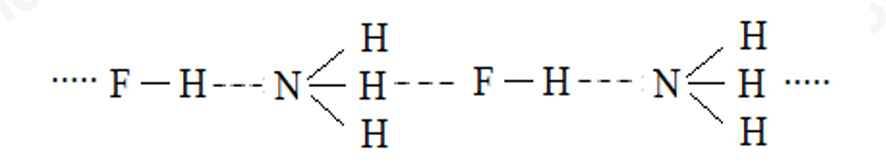Viết các khả năng tạo thành liên kết hydrogen giữa một phân tử H2O và một phân tử NH3.
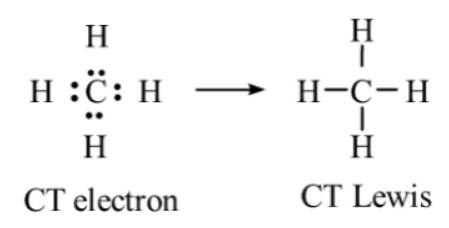
- CT electron và CT Lewis của NH3:
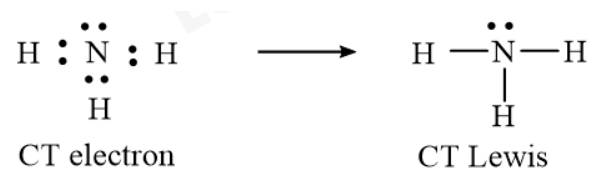
⟹ NH3 còn 1 cặp electron riêng của N.
- Vì N còn 1 của phân tử NH3 còn 1 cặp electron riêng và có độ âm điện lớn hơn nguyên tử H của phân tử H2O.
⟹ Một phân tử H2O có khả năng tạo thành liên kết hydrogen với một phân tử NH3, liên kết tạo bởi H và N.
Đúng 0
Bình luận (0)
Vẽ các liên kết hydrogen được hình thành giữa H2O với mỗi phân tử NH3, C2H5OH.
Vì sao nguyên tử H của của phân tử H2O không tạo được liên kết hydrogen với nguyên tử C của phân tử CH4?
Nguyên tử H của H của của phân tử H2O không tạo được liên kết hydrogen với nguyên tử C của phân tử CH4. Vì nguyên tử C của phân tử CH4 không còn cặp electron riêng:
Đúng 0
Bình luận (0)
Vẽ sơ đồ biểu diễn liên kết hydrogen giữa:
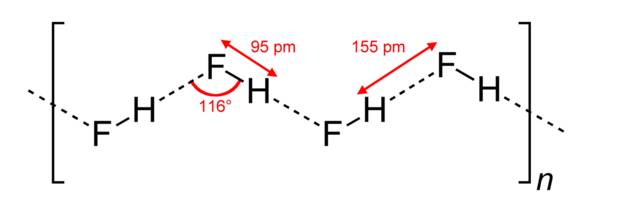
a) hai phân tử hydrogen fluoride (HF)
b) phân tử hydrogen fluoride (HF) và phân tử ammonia (NH3).
Ở hình bên, ta thấy 1 nguyên tử carbon liên kết với 4 nguyên tử hydrogen hoặc chỉ liên kết với 2 nguyên tử oxygen; 1 nguyên tử oxygen liên kết được với 2 nguyên tử hydrogen;… Các nguyên tử liên kết với nhau theo nguyên tắc nào? Bằng cách nào để lập được công thức hóa học của các chất?
Đọc tiếp
Ở hình bên, ta thấy 1 nguyên tử carbon liên kết với 4 nguyên tử hydrogen hoặc chỉ liên kết với 2 nguyên tử oxygen; 1 nguyên tử oxygen liên kết được với 2 nguyên tử hydrogen;… Các nguyên tử liên kết với nhau theo nguyên tắc nào? Bằng cách nào để lập được công thức hóa học của các chất?
Các nguyên tử liên kết với nhau theo nguyên tắc hóa trị: trong phân tử hợp chất 2 nguyên tố, tích hóa trị và số nguyên tử của nguyên tố này bằng tích hóa trị và số nguyên tử của nguyên tố kia
- Để lập được công thức hóa học của các chất:
+ Xác định công thức hóa học dựa vào phần trăm nguyên tố và khối lượng phân tử
+ Xác định công thức hóa học dựa vào quy tắc hóa trị
Đúng 0
Bình luận (0)
So sánh được tính chất vật lí giữa các phân tử dựa vào liên kết hydrogen và tương tác van der Waals.
Để so sánh được tính chất vật lí giữa các phân tử, chúng ta cần nắm được những ý sau:
- Liên kết hydrogen được hình thành giữa nguyên tử H (đã liên kết với một nguyên tử có độ âm điện lớn) với một nguyên tử khác (có độ âm điện lớn) còn cặp electron hóa trị chưa tham gia liên kết.
⇒ Liên kết hydrogen làm tăng nhiệt độ nóng chảy và nhiệt độ sôi của nước.
- Tương tác van der Waals là tương tác tĩnh điện lưỡng cực – lưỡng cực được hình thành giữa các phân tử hay nguyên tử.
⇒ Tương tác van der Waals làm tăng nhiệt độ nóng chảy và nhiệt độ sôi của các chất.
Đúng 0
Bình luận (0)
Viết CTHH và tính phân tử khối của các hợp chất sau :
a)Barium hydrogen carbonate biết trong phân tử gồm 1Ba , 2H , 2C và 6O liên kết với nhau
b) Khí Hydrogen Chlorid biết phân tử gồm 1H và 1Cl liên kết với nhau
c) Iron (III) oxide biết trong phân tử gồm 2Fe và 3O liên kết với nhau
a) CTHH: Ba(HCO3)2
M = 137 + 2 + 2 .12 + 16.6 = 259 ( g/mol )
b) CTHH: HCL
M = 36,5 ( g/mol )
c) CTHH Fe2O3
M = 56.2 + 16.3 = 160 ( g/mol )
Đúng 0
Bình luận (0)
Liên kết hydrogen xuất hiện giữa những phân tử cùng loại nào sau đây?
A. CH4
B. NH3
C. H3C – O – CH3
D. PH3
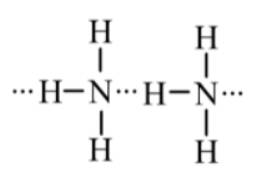
Liên kết hydrogen xuất hiện giữa những phân tử cùng loại NH3:
Đúng 0
Bình luận (0)
Một hợp chất có phân tử gồm 2 nguyên tử nguyên tố X liên kết với 1 nguyên tử O và nặng hơn phân tử hydrogen 31 lần.
Công thức của hợp chất: \(X_2O\)
\(d\dfrac{X_2O}{H_2}=31\) \(\Rightarrow M_{X_2O}=62\)
\(\Rightarrow2M_X+16=62\Leftrightarrow2M_X=46\)
\(\Rightarrow M_X=23\Rightarrow X:Na\)
Vậy hợp chất là: \(Na_2O\): sodium oxide
Đúng 2
Bình luận (0)
Liên kết hóa học giữa các nguyên tử trong phân tử H 2 O là liên kết
A. cộng hóa trị không phân cực
B. hiđro
C. ion
D. cộng hóa trị phân cực
Chọn D
Do oxi có độ âm điện lớn hơn nhiều so với hiđro nên liên kết hóa học giữa các nguyên tử trong phân tử H2O là liên kết cộng hóa trị phân cực.
Hoặc có thể giải thích định tính bằng tính hiệu độ âm điện:
Hiệu độ âm điện của O và H là 3,44 – 2,2 = 1,24. Vậy liên kết hóa học giữa các nguyên tử trong phân tử H2O là liên kết cộng hóa trị phân cực.
Đúng 0
Bình luận (0)