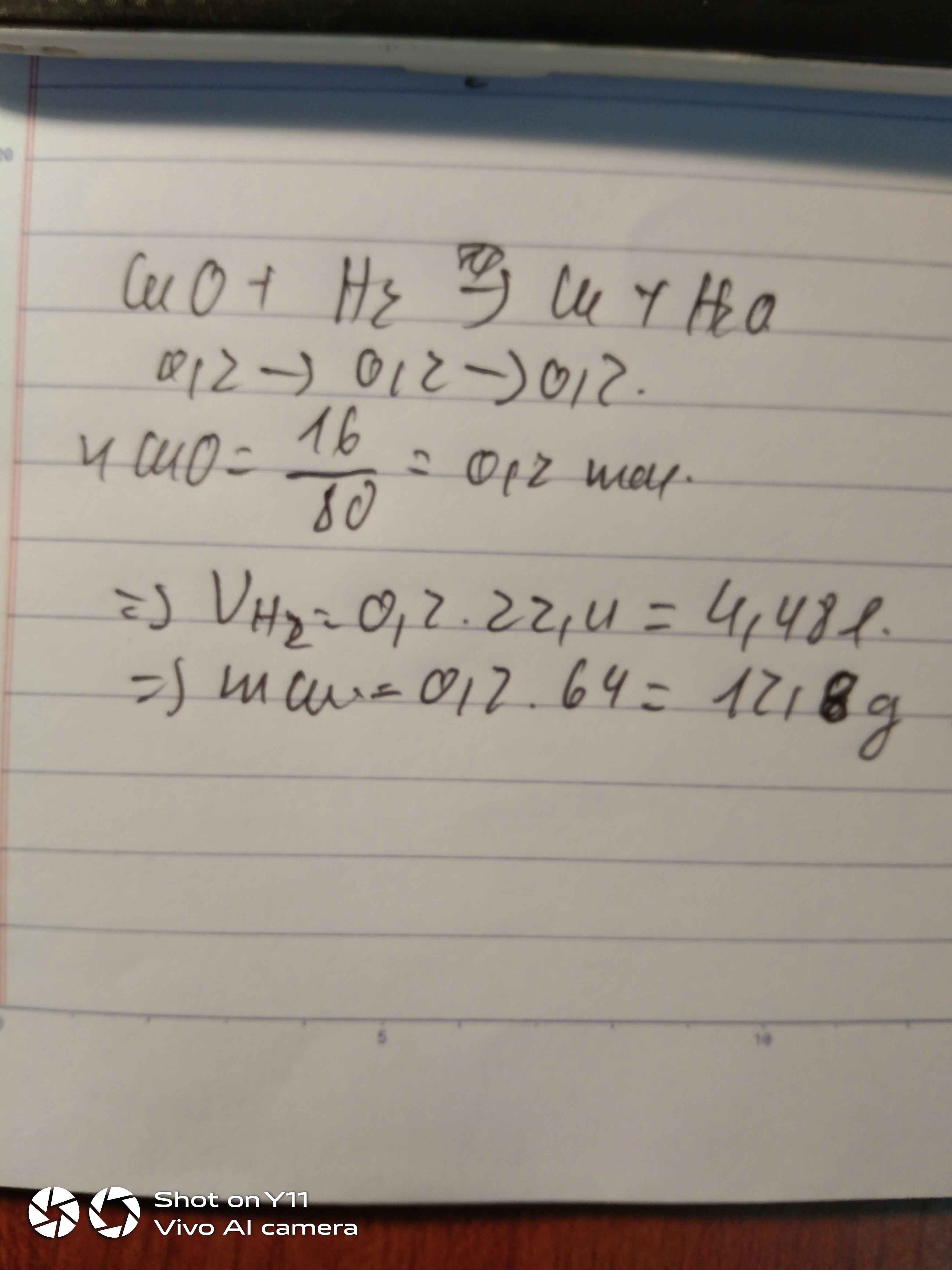Cho H 2 khử 16g hỗm hợp FeO và CuO trong đó CuO chiếm 25% khối lượng. Tính tổng thể tích khí H 2 (đktc) đã tham gia phản ứng.

Những câu hỏi liên quan
Cho H 2 khử 16g hỗm hợp FeO và CuO trong đó CuO chiếm 25% khối lượng. Tính khối lượng Fe và khối lượng Cu thu được sau phản ứng.
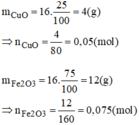
PTHH của phản ứng là:
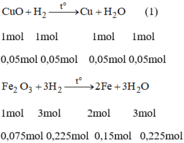
Từ pt (1), ta có: n C u = n C u O = 0,05 mol
m C u = 0,05.64 = 3,2(g)
Từ pt (2), ta có n F e = 2 . n F e 2 O 3 = 2. 0,075 = 0,15 mol
m F e = 0,15.56 = 8,4(g)
Đúng 0
Bình luận (0)
Dùng H² để khử 50g hỗn hợp CuO và Fe²O³ , trong đó Fe²O³ chiếm 80% khối lượng hỗn hợp a) viết pthh b) tính khối lượng mỗi kim loại thu được c) tính thể tích khí H² cần dùng
a, PT: \(CuO+H_2\underrightarrow{t^o}Cu+H_2O\)
\(Fe_2O_3+3H_2\underrightarrow{t^o}2Fe+3H_2O\)
b, Ta có: \(m_{Fe_2O_3}=50.80\%=40\left(g\right)\Rightarrow n_{Fe_2O_3}=\dfrac{40}{160}=0,25\left(mol\right)\)
\(\Rightarrow m_{CuO}=10\left(g\right)\Rightarrow n_{CuO}=\dfrac{10}{80}=0,125\left(mol\right)\)
Theo PT: \(\left\{{}\begin{matrix}n_{Cu}=n_{CuO}=0,125\left(mol\right)\\n_{Fe}=2n_{Fe_2O_3}=0,5\left(mol\right)\end{matrix}\right.\)
\(\Rightarrow\left\{{}\begin{matrix}m_{Cu}=0,125.64=8\left(g\right)\\m_{Fe}=0,5.56=28\left(g\right)\end{matrix}\right.\)
b, Theo PT: \(n_{H_2}=n_{CuO}+3n_{Fe_2O_3}=0,875\left(mol\right)\)
\(\Rightarrow V_{H_2}=0,875.22,4=19,6\left(l\right)\)
Bạn tham khảo nhé!
Đúng 2
Bình luận (0)
Bài 6: Cho H2 khử 20 gam hỗn hợp Fe2O3 và CuO trong đó CuO chiếm 40% khối lượng.
a) Tính khối lượng Fe và khối lượng Cu thu được sau phản ứng?
b) Tính thể tích khí Hiđro (đktc) cần dùng?
a) \(m_{CuO}=\dfrac{20.40}{100}=8\left(g\right)\) => \(n_{CuO}=\dfrac{8}{80}=0,1\left(mol\right)\)
\(m_{Fe_2O_3}=20-8=12\left(g\right)\) => \(n_{Fe_2O_3}=\dfrac{12}{160}=0,075\left(mol\right)\)
PTHH: CuO + H2 --to--> Cu + H2O
0,1--->0,1------>0,1
Fe2O3 + 3H2 --to--> 2Fe + 3H2O
0,075--->0,225----->0,15
=> mCu = 0,1.64 = 6,4 (g)
=> mFe = 0,15.56 = 8,4 (g)
b) \(V_{H_2}=\left(0,1+0,225\right).22,4=7,28\left(l\right)\)
Đúng 4
Bình luận (0)
Khử 24g hỗn hợp 2 oxit CuO và Fe2O3 bằng khí H2 theo sơ đồ sau: CuO + H𝟸 ---> Cu + H𝟸O; Fe𝟸O𝟹 + H𝟸 ---> Fe + H𝟸O Tính thể tích H𝟸(đktc) cần dùng, biết rằng trong hỗn hợp Fe𝟸O𝟹 chiếm 75% khối lượng
\(n_{Fe_2O_3}=24.75\%=18g\)
\(n_{Fe_2O_3}=\dfrac{18}{160}=0,1125mol\)
\(n_{CuO}=\dfrac{24-18}{80}=0,075mol\)
\(Fe_2O_3+3H_2\rightarrow\left(t^o\right)2Fe+3H_2O\)
0,1125 0,3375 ( mol )
\(CuO+H_2\rightarrow\left(t^o\right)Cu+H_2O\)
0,075 0,075 ( mol )
\(V_{H_2}=\left(0,3375+0,075\right).22,4=9,24l\)
Đúng 2
Bình luận (0)
a) Co bao nhieu gam H2O khi cho nổ hỗn hợp gồm 1mol hiđro và 20g oxi?
b) Cho 50g hỗn hợp đồng (III) ôxít (CuO) vá sắt (II) ôxít (FeO) tác dụng với khí hidro cho hỗn hợp 2 kim laoi và nước
tính thể tích khí hiđro cần dùng biết rằng trong hỗn hợp đồng(III) oxit chiếm 20% về khối lượng
CHÚC BẠN HỌC TỐT![]()
a) Theo đề bài, ta có: \(n_{O2}=\dfrac{20}{32}=0,625\left(mol\right)\)
PTHH: \(2H_2+O_2\underrightarrow{o}2H_2O\)
pư............1.........0,5......1 (mol)
Ta có tỉ lệ: \(\dfrac{1}{2}< 0,625\). Vậy O2 dư, H2 hết.
\(\Rightarrow m_{H2O}=18.1=18\left(g\right)\)
Vậy.........
Đúng 0
Bình luận (0)
b) Đề nhầm bạn ơi, Cu chỉ có hóa trị là: I hoặc II![]()
Đúng 0
Bình luận (0)
Dùng khí H2 để khử 40g hỗn hợp CuO và Fe2O3, biết trong hỗn hợp Fe2O3 chiếm 80% về khối lượng. a/ Tính thể tích khí H2 đã dùng ở đktc.b/ Tính khối lượng và thành phần % về khối lượng mỗi kim loại sinh ra.c/ Nếu cho toàn bộ lượng kim loại sinh ra ở trên cho tác dụng với H2SO4 loãng dư thì thu được bao nhiêu lít khí H2
Đọc tiếp
Dùng khí H2 để khử 40g hỗn hợp CuO và Fe2O3, biết trong hỗn hợp Fe2O3 chiếm 80% về khối lượng. a/ Tính thể tích khí H2 đã dùng ở đktc.
b/ Tính khối lượng và thành phần % về khối lượng mỗi kim loại sinh ra.
c/ Nếu cho toàn bộ lượng kim loại sinh ra ở trên cho tác dụng với H2SO4 loãng dư thì thu được bao nhiêu lít khí H2
a.b.
\(\left\{{}\begin{matrix}n_{Fe_2O_3}=40.80\%=32g\\m_{CuO}=40-32=8g\end{matrix}\right.\)
\(\left\{{}\begin{matrix}n_{Fe_2O_3}=\dfrac{32}{160}=0,2mol\\n_{CuO}=\dfrac{8}{80}=0,1mol\end{matrix}\right.\)
\(CuO+H_2\rightarrow\left(t^o\right)Cu+H_2O\)
0,1 0,1 0,1 ( mol )
\(Fe_2O_3+3H_2\rightarrow\left(t^o\right)2Fe+3H_2O\)
0,2 0,6 0,4 ( mol )
\(V_{H_2}=\left(0,1+0,6\right).22,4=15,68l\)
\(\left\{{}\begin{matrix}m_{Cu}=0,1.64=6,4g\\m_{Fe}=0,4.56=22,4g\end{matrix}\right.\)
\(\rightarrow\left\{{}\begin{matrix}\%m_{Cu}=\dfrac{6,4}{6,4+22,4}.100=22,22\%\\\%m_{Fe}=100\%-22,22\%=77,78\%\end{matrix}\right.\)
c.
\(Fe+H_2SO_4\rightarrow FeSO_4+H_2\) ( Cu không phản ứng với H2SO4 loãng )
0,4 0,4 ( mol )
\(V_{H_2}=0,4.22,4=8,96l\)
Đúng 2
Bình luận (0)
Khử 16g Copper(II) oxide (CuO ) bằng khí hydrogen (H2 ) a.Tính thể tích khí hydrogen (H2 ) tham gia phản ứng? b. Tính khối lượng kim loại tạo thành? Fe= 56, O=16, Cu=64, H=1
Khử hoàn toàn 19,6 gam hỗn hợp X (gồm CuO và FeO) bằng H2. a. Tính khối lượng mỗi chất trong X biết số mol CuO gấp 4 lần số mol FeO. b. Tính thể tích H2 cần dùng (đktc) c. Tính khối lượng chất rắn tạo thành sau phản ứng?
\(n_{CuO}=4a\left(mol\right)\Rightarrow n_{FeO}=a\left(mol\right)\)
\(m_X=80\cdot4a+72a=19.6\left(g\right)\)
\(\Rightarrow a=0.05\)
\(CuO+H_2\underrightarrow{^{^{t^0}}}Cu+H_2O\)
\(FeO+H_2\underrightarrow{^{^{t^0}}}Fe+H_2O\)
\(m_{cr}=0.2\cdot64+0.05\cdot56=15.6\left(g\right)\)
\(V_{H_2}=\left(0.05\cdot4+0.05\right)\cdot22.4=5.6\left(l\right)\)
Đúng 2
Bình luận (0)
Cho 31,3 gam CuO và Fe3O4 trong đó Fe3O4 hơn CuO là 15,2 gam . dùng H2 khử hỗn hợp trên
a, tính khối lượng đồng và sắt thu đk b, tính thể tích H2 tham gia tất cả là bao nhiêu lít (đktc)a) Ta giải hệ: \(m_{CuO}+m_{Fe_2O_3}=37,6\) và \(m_{CuO}-m_{Fe_2O_3}=-15,2\)
\(m_{CuO}=8,05(g) \) ; \( m_{Fe_{2}O_{3}}=23,25(g)\)\(\Rightarrow\) \(n_{CuO}\)=0,1(mol) và \(n_{Fe_3O_4}\)=0,1(mol) CuO+H2 \(\rightarrow\) H2O+Cu(1)\(\Rightarrow\) \(n_{H_2\left(1\right)}\)=\(n_{CuO}\)=0,1(mol)và tiếp theo là phương trình \(Fe_3O_4\) tác dụng với \(H_2\): 4H2+Fe2O3\(\rightarrow\)3Fe+4H2O(2)\(\Rightarrow\) \(n_{H_2\left(2\right)}\)=\(4n_{CuO}\)=0,4(mol)\(\Rightarrow\)\(n_{H_2}\)=0,4+0,1=0,5(mol)\(\Rightarrow\)V=11,2(l)
Đúng 0
Bình luận (1)