Có 4 lọ không có nhãn đựng riêng biệt các muối : KF, KCl, KBr, KI.
Từ những muối đã cho điều chế các halogen tương ứng và các hiđro halogenua tương ứng.
Có 4 lọ không có nhãn đựng riêng biệt các muối : KF, KCl, KBr, KI.
Hãy cho biết : Cách phân biệt muối đựng trong mỗi lọ bằng phương pháp hoá học.
Lấy một ít muối trong mỗi lọ đem hoà tan vào nước được các dung dịch riêng biệt.
Dung dịch nào tác dụng được với Br 2 hoặc nước brom tạo ra tinh thể có màu đen tím, đó là dung dịch KI.
Br 2 + 2KI → 2KBr + I 2
Những dung dịch còn lại, dung dịch nào tác dụng được với Cl 2 tạo ra dung dịch có màu vàng nâu (màu của Br 2 tan trong nước), đó là dung dịch KBr.
Cl 2 + 2KBr → 2KCl + Br 2
Hai dung dịch còn lại là KF và KCl : cho tác dụng với dung dịch Ag NO 3 , dung dịch nào tạo kết tủa trắng, đó là dung dịch KCl.
KCl + Ag NO 3 → AgCl + K NO 3
Dung dịch còn lại là KF.
Có các chất khí sau: cacbon đioxit, hiđro, oxi đựng trong các lọ riêng biệt mất nhãn. Một học sinh đã đánh sỗ tương ứng là (1), (2), (3) vào các lọ trên rồi dẫn khí đi thử. Kết quả thí nghiệm được ghi lại ở bảng sau:
Mẫu thử Thuốc thử Hiện tượng
-----------------------------------------------------------------------------
(1) Que đóm còn tàn đỏ Tàn đóm đỏ bùng cháy
-----------------------------------------------------------------------------
(2), (3) Que đóm còn tàn đỏ Tàn đóm tắt
-----------------------------------------------------------------------------
(3) Đồng (II) oxit Chất bột màu đen chuyển thành màu đỏ
Hãy xác định mẫu thử (1) (2) (3) là chất khí nào? Giải thích.
(1) là O2 vì chỉ có O2 mới làm tàn que đóm bùng cháy
(3) là H2 hoặc CO vì chỉ có H2 và CO mới khử được oxi trong oxit của đồng (II) oxit (màu đen) thành đồng (màu đỏ)
(2) là các chất khí khác
Vì sao người ta có thể điều chế hiđro clorua (HCl), hiđro florua (HF) bằng cách cho dung dịch H 2 SO 4 đặc tác dụng với muối clorua hoặc florua, nhưng không thể áp dụng phương pháp này để điều chế hiđro bromua (HBr) hoặc hiđro iotua (HI) ? Viết PTHH của các phản ứng điều chế các hiđro halogenua.
Điều chế HF, HCl bằng cách cho H 2 SO 4 đặc tác dụng với muối florua, clorua vì H 2 SO 4 à chất oxi hoá không đủ mạnh để oxi hoá được HF và HCl. Nói cách khác, HF và HCl có tính khử yếu, chúng không khử được H 2 SO 4 đặc
Ca F 2 + H 2 SO 4 → Ca SO 4 + 2HF
NaCl + H 2 SO 4 → NaH SO 4 + HCl
Nhưng không thể dùng phương pháp trên để điều chế HBr và HI vì H 2 SO 4 đặc oxi hoá được những chất này thành Br 2 và I 2 . Nói cách khác, HBr và HI là những chất có tính khử mạnh hơn HCl và HF.
NaBr + H 2 SO 4 → HBr + NaH SO 4
2HBr + H 2 SO 4 → Br 2 + SO 2 + 2 H 2 O
NaI + H 2 SO 4 → NaH SO 4 + HI
2HI + H 2 SO 4 → I 2 + SO 2 + 2 H 2 O
Chỉ được dùng thêm nước và các thiết bị cần thiết (lò nung, đèn cồn…). Hãy trình bày cách phân biệt 4 chất bột màu trắng (tương tự nhau) đựng riêng biệt trong 4 lọ mất nhãn: KNO3, Al(NO3)3, MgCO3, CaCO3. Viết phương trình hóa học của các phản ứng xảy ra (ghi rõ điều kiện nếu có).
Có các dung dịch muối AlCl3, (NH4)2SO4, NH4NO3, MgCl2, FeCl3 đựng trong các lọ riêng biệt bị mất nhãn. Đánh dấu ngẫu nhiên 5 mẫu thử tương ứng với X, Y, Z, T, U rồi nhỏ từ từ dung dịch Ba(OH)2 vào các mẫu thử trên thì thu được kết quả trong bảng như sau:
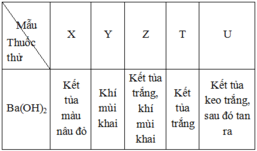
Các chất X, Y, Z, T, U lần lượt là
A. FeCl3, NH4NO3, (NH4)2SO4, AlCl3, MgCl2.
B. FeCl3, NH4NO3, (NH4)2SO4, MgCl2, AlCl3.
C. FeCl3, (NH4)2SO4, NH4NO3, AlCl3, MgCl2.
D. FeCl3, (NH4)2SO4, NH4NO3, MgCl2, AlCl3.
Có các lọ mất nhãn đựng riêng biệt các chất rắn sau: CaCO3, K2CO3, NaHCO3, KCl. Trình bày cách phân biệt các lọ trên bằng phương pháp hoá học.
Có các lọ mất nhãn đựng riêng biệt các dung dịch sau: Na2CO3, NaOH, Ca(OH)2, HCl. Không dùng quỳ tím, hãy phân biệt các lọ này bằng phương pháp hoá học.
1. - Trích mẫu thử.
- Hòa tan từng mẫu thử vào nước.
+ Tan: K2CO3, KHCO3 và KCl. (1)
+ Không tan: CaCO3.
- Cho dd mẫu thử nhóm (1) pư với HCl dư.
+ Có khí thoát ra: K2CO3, KHCO3. (2)
PT: \(K_2CO_3+2HCl\rightarrow2KCl+CO_2+H_2O\)
\(KHCO_3+HCl\rightarrow KCl+CO_2+H_2O\)
+ Không hiện tượng: KCl.
- Cho mẫu thử nhóm (2) pư với BaCl2.
+ Xuất hiện kết tủa trắng: K2CO3.
PT: \(K_2CO_3+BaCl_2\rightarrow2KCl+BaCO_{3\downarrow}\)
+ Không hiện tượng: KHCO3.
- Dán nhãn.
2. - Trích mẫu thử.
- Nhỏ vài giọt từng mẫu thử vào dd BaCl2.
+ Xuất hiện kết tủa trắng: Na2CO3.
PT: \(Na_2CO_3+BaCl_2\rightarrow2NaCl+BaCO_{3\downarrow}\)
+ Không hiện tượng: NaOH, Ca(OH)2 và HCl. (1)
- Cho mẫu thử nhóm (1) pư với Na2CO3 vừa nhận biết được.
+ Có khí thoát ra: HCl.
PT: \(Na_2CO_3+2HCl\rightarrow2NaCl+CO_2+H_2O\)
+ Không hiện tượng: NaOH, Ca(OH)2. (2)
- Sục CO2 vào mẫu thử nhóm (2).
+ Xuất hiện kết tủa trắng: Ca(OH)2.
PT: \(CO_2+Ca\left(OH\right)_2\rightarrow CaCO_{3\downarrow}+H_2O\)
+ Không hiện tượng: NaOH.
PT: \(CO_2+2NaOH\rightarrow Na_2CO_3+H_2O\)
- Dán nhãn.
dùng phương pháp hoá học phân biệt các muối bị mất nhãn ở dạng rắn sau: CACO3 , Na2SO4 ,KCL
Hãy cho biết những phản ứng hoá học nào trong bảng có thể dùng để điều chế các muối sau (Bằng cách ghi dấu x (có) và dấu o (không) vào những ô tương ứng) :
Natri clorua.
Đồng clorua.
Viết các phương trình hoá học.
Viết các phương trình hóa học của phản ứng từ (1) đến (10) .
| PHẢN ỨNG HÓA HỌC | Axit + Bazơ | Axit + Oxit bazơ | Axit + Kim loại | Axit + Muối | Muối + Muối | Kim loại + Phi kim |
| NaCl | x(l) | x(2) | 0 | x(3) | x(4) | x(5) |
| CuCl 2 | x(6) | x(7) | 0 | x(8) | x(9) | x(10) |
1/ HCl + NaOH → NaCl + H 2 O
6/ 2HCl + Cu OH 2 → CuCl 2 + 2 H 2 O
2/ 2HCl + Na 2 O → 2NaCl + H 2 O
7/ 2HCl + CuO → CuCl 2 + H 2 O
3/ 2HCl + Na 2 CO 3 → 2NaCl + H 2 O + CO 2
8/ 2HCl + CuCO 3 → CuCl 2 + H 2 O + CO 2
4/ Na 2 SO 4 + BaCl 2 → 2NaCl + BaSO 4
9/ CuSO 4 + BaCl 2 → CuCl 2 + BaSO 4
5/ 2Na + Cl 2 → NaCl
10/ Cu + Cl 2 → Cu Cl 2
Có các lọ riêng biệt đựng các dung dịch không màu : C u C l 2 , A l N O 3 3 , F e 2 S O 4 3 , Z n C l 2 , KCl. Chỉ dùng dung dịch nào dưới đây để phân biệt các lọ mất nhãn trên ?
A. N a 2 C O 3
B. B a O H 2
C. N H 3
D. NaOH
Để phân biệt các dung dịch đựng các lọ riêng biệt, không dán nhãn: M g C l 2 , A l C l 3 F e C l 2 , KCl bằng phương pháp hóa học, có thể dùng:
A. dd NaOH
B. dd NaCl
C. dd N a 2 C O 3
D. Quì tím
Cho dung dịch NaOH từ từ đến dư vào từng mẫu thử:

Chọn A.