Một hỗn hợp gồm 13 gam kẽm và 5,6 gam sắt tác dụng với dung dịch axit sunfuric loãng, dư.
Thể tích khí hiđro (đktc) được giải phóng sau phản ứng là
A. 4,48 lít. B. 2,24 lít
C. 6,72 lít. D. 67,2 lít.
Một hỗn hợp gồm 13 gam kẽm và 5,6 gam sắt tác dụng với dung dịch axit sunfuric loãng dư. Thể tích khí hiđro (đktc) được giải phóng sau phản ứng là ?
Một hỗn hợp gồm 13 gam kẽm và 5,6 gam sắt tác dụng với dung dịch axit HCl dư. Thể tích khí hidro (đktc) được giải phóng sau phản ứng là
A. 6,72 lít
B. 2,24 lít
C. 4,48 lít
D. 67,2 lít
Một hỗn hợp gồm 13 gam kẽm và 5,6 gam sắt tác dụng với dung dịch axit HCl dư. Thể tích khí hidro (đktc) được giải phóng sau phản ứng là
A. 6,72 lít.
B. 2,24 lít.
C. 4,48 lít.
D. 67,2 lít.
Một hỗn hợp gồm 13 gam kẽm và 5,6 gam sắt tác dụng với dung dịch axit HCl dư. Thể tích khí hidro (đktc) được giải phóng sau phản ứng là
A. 6,72 lit
B. 2,24 lit
C. 4,48 lit
D. 67,2 lit
Một hỗn hợp gồm 13 gam kẽm và 5,6 gam sắt tác dụng với dung dịch axit HCl dư. Thể tích khí hidro (đktc) được giải phóng sau phản ứng là
A. 6,72 lít.
B. 2,24 lít.
C. 4,48 lít.
D. 67,2 lít.
Một hỗn hợp gồm 13 gam kẽm và 5,6 gam sắt tác dụng với dung dịch axit HCl dư. Thể tích khí hidro (đktc) được giải phóng sau phản ứng là
A. 6,72 lít.
B. 2,24 lít.
C. 4,48 lít.
D. 67,2 lít.
Cho 18,6 gam hỗn hợp X gồm kẽm và sắt tác dụng với dung dịch axit sunfuric loãng, dư, thu được 6,72 lít khí H2 (đktc). Thành phần phần trăm khối lượng của kẽm có trong hỗn hợp X là
A. 96,69%
B. 69,89%
C. 50%
D. 34,94%
Đáp án B
Số mol H2 thu được là: n H 2 = 0 , 3 mol
Đặt số mol các chất trong X là Zn: a mol ; Fe: b mol.
m Zn + m Fe = m X ⇒ 65 a + 56 b = 18 , 6 ( I )
Sơ đồ phản ứng:
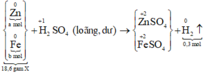
Các quá trình nhường, nhận electron:
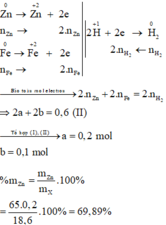
Cho 5,6 gam sắt tác dụng với dung dịch axit sunfuric loãng, thu được V lít khí Hidro (ở đktc).
a. Viết PTHH của phản ứng.
b. Tính thể tích khí hidro thu được.
c. Dẫn V lít khí Hidro ở phản ứng trên qua bình đựng 12 gam CuO. Sau phản ứng, chất nào còn dư và dư bao nhiêu gam? Tính khối lượng Cu sinh ra.
a) Fe + H2SO4 --> FeSO4 + H2
b) \(n_{Fe}=\dfrac{5,6}{56}=0,1\left(mol\right)\)
PTHH: Fe + H2SO4 --> FeSO4 + H2
0,1------------------------>0,1
=> VH2 = 0,1.22,4 = 2,24 (l)
c) \(n_{CuO}=\dfrac{12}{80}=0,15\left(mol\right)\)
PTHH: CuO + H2 --to--> Cu + H2O
Xét tỉ lệ: \(\dfrac{0,15}{1}>\dfrac{0,1}{1}\) => CuO dư, H2 hết
PTHH: CuO + H2 --to--> Cu + H2O
0,1<--0,1------->0,1
=> mCuO(dư) = (0,15 - 0,1).80 = 4 (g)
mCu = 0,1.64 = 6,4 (g)
a, PT: \(Fe+H_2SO_4\rightarrow H_2SO_4+H_2\)
b, Ta có: \(n_{Fe}=\dfrac{5,6}{56}=0,1\left(mol\right)\)
Theo PT: \(n_{H_2}=n_{Fe}=0,1\left(mol\right)\)
\(\Rightarrow V_{H_2}=0,1.22,4=2,24\left(l\right)\)
c, Ta có: \(n_{CuO}=\dfrac{12}{80}=0,15\left(mol\right)\)
PT: \(CuO+H_2\underrightarrow{t^o}Cu+H_2O\)
Xét tỉ lệ: \(\dfrac{0,15}{1}>\dfrac{0,1}{1}\), ta được CuO dư.
Theo PT: \(n_{Cu}=n_{CuO\left(pư\right)}=n_{H_2}=0,1\left(mol\right)\)
\(\Rightarrow n_{CuO\left(dư\right)}=0,05\left(mol\right)\Rightarrow m_{CuO\left(dư\right)}=0,05.80=4\left(g\right)\)
\(m_{Cu}=0,1.64=6,4\left(g\right)\)
Bạn tham khảo nhé!
Bài 1: Cho 5,6 gam sắt tác dụng với dung dịch axit sunfuric loãng, thu được V lít khí Hidro (ở đktc).
a. Viết PTHH của phản ứng.
b. Tính thể tích khí hidro thu được.
c. Dẫn V lít khí Hidro ở phản ứng trên qua bình đựng 12 gam CuO. Sau phản ứng, chất nào còn dư và dư bao nhiêu gam?
Bài 2: Đốt cháy 3,1 gam photpho trong bình chứa khí oxi tạo thành chất rắn màu trắng điphotpho pentaoxit.
a. Viết PTHH của phản ứng.
b. Tính thể tích khí oxi cần dùng ở đktc.
c. Nếu cho lượng khí Oxi ở phản ứng trên tác dụng với 19,5 gam kim loại kẽm thì chất nào còn dư sau phản ứng và dư bao nhiêu gam?
Bài 1.
\(n_{Fe}=\dfrac{5,6}{56}=0,1mol\)
\(Fe+H_2SO_4\rightarrow FeSO_4+H_2\)
0,1 0,1 0,1 0,1
\(V_{H_2}=0,1\cdot22,4=2,24l\)
\(n_{CuO}=\dfrac{12}{80}=0,15mol\)
\(CuO+H_2\rightarrow Cu+H_2O\)
0,15 0,1
\(\Rightarrow CuO\) dư và dư \(\left(0,15-0,1\right)\cdot80=4g\)
Bài 2.
\(n_P=\dfrac{3,1}{31}=0,1mol\)
\(4P+5O_2\underrightarrow{t^o}2P_2O_5\)
0,1 0,125
\(V_{O_2}=0,125\cdot22,4=2,8l\)
\(n_{Zn}=\dfrac{19,5}{65}=0,3mol\)
\(2Zn+O_2\underrightarrow{t^o}2ZnO\)
0,3 0,125 0
0,25 0,125 0,25
0,05 0 0,25
\(\Rightarrow ZnO\) dư và dư \(0,05\cdot81=4,05g\)
Bài 1.
a, \(n_{Fe}=\dfrac{5,6}{56}=0,1\left(mol\right)\)
PTHH: Fe + H2SO4 ---> FeSO4 + H2
Mol: 0,1 0,1
b, \(V_{H_2}=0,1.22,4=2,24\left(l\right)\)
c, \(n_{CuO}=\dfrac{12}{80}=0,15\left(mol\right)\)
Ta có: \(\dfrac{0,15}{1}>\dfrac{0,1}{1}\) ⇒ CuO dư, H2 hết
PTHH: CuO + H2 ---to----> Cu + H2O
Mol: 0,1 0,1
\(m_{CuOdư}=\left(0,15-0,1\right).80=4\left(g\right)\)