Một oxit A của nitơ có chứa 30,43% N về khối lượng. Tỉ khối hơi của A so với không khí là 1,586. A là
A. NO.
B. N2O
C. NO2
D. N2O3.
Tỉ lệ khối lượng của nito và oxi trong một oxit của nito là 7 : 20. Công thức của oxit là:
A. N 2 O . B. N 2 O 3 . C. N O 2 . D. N 2 O 5 .
Hãy chọn đáp số đúng.
Gọi công thức hóa học của oxit là N x O y
Tỉ số khối lượng:
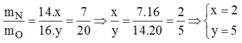
Vậy công thức hóa học của oxit Nito là: N 2 O 5 .
→ Chọn D.
Một oxit nitơ (X) chứa 30,43% N về khối lượng .Tỉ khối của X so với không khí là 1,5862.Cần bao nhiêu gam dd H N O 3 HNO3 40% tác dụng với Cu để điều chế 1 lit khí X (ở 134 o 134o C,1atm), giả sử phản ứng chỉ giải phóng duy nhất khí X? 13,4g 9,45g 12,3g kết quả khác.
\(n_X=\dfrac{P.V}{R.T}=\dfrac{1.1}{0,082.\left(273+134\right)}=0,03\left(mol\right)\\ M_X=29.1,5862=46\left(\dfrac{g}{mol}\right)\\ Đặt.CTTQ:N_kO_t\left(k,t:nguyên,dương\right)\\ Ta.có:k:t=\dfrac{30,43\%}{14}:\dfrac{69,57\%}{16}=0,022:0,043=1:2\\ \Rightarrow k=1;t=2\\ \Rightarrow CTHH.X:NO_2\\ Cu+4HNO_3\rightarrow Cu\left(NO_3\right)_2+2NO_2+2H_2O\\ n_{HNO_3}=\dfrac{4}{2}.n_{NO_2}=\dfrac{4}{2}.0,03=0,06\left(mol\right)\\ \Rightarrow m_{ddHNO_3}=\dfrac{0,06.63.100}{40}=9,45\left(g\right)\)
Tỉ lệ khối lượng của nitơ và oxi trong một oxit của nitơ là 70:40 . Công thức oxit đó là
A. NO
B. N2O
C. N2O3
D. NO2
CTHH: NxOy
Có \(\dfrac{m_N}{m_O}=\dfrac{14x}{16y}=\dfrac{70}{40}\)
=> \(\dfrac{x}{y}=\dfrac{2}{1}\)
=> CTHH: N2O
=> B
Gọi công thức hóa học của oxit là NxOyNxOy
Tỉ số khối lượng:
Vậy công thức hóa học của oxit Nito là: N2O5N2O5.
chọn D.
\(\dfrac{m_N}{m_O}=\dfrac{70}{40}=\dfrac{7}{4}\)
\(N_xO_y\)
\(\Rightarrow x:y=\dfrac{7}{14}:\dfrac{4}{16}=0,5:0,25=2:1\)
\(\Rightarrow CTHH:N_2O\)
Hãy tính
a. Khối lượng của hỗn hợp gồm 0,12 mol Fe(OH)2 và 0,15 mol Mg(OH)2.
b. Thể tích của hỗn hợp gồm 0,25 mol NO2, 0,1 mol NO và 0,05 mol N2O (đktc).
c. Khối lượng của 10,08 lít chất khí A (đktc), biết A có tỉ khối so với H2 là 23.
d. Khối lượng mol của 6,72 lít hỗn hợp khí CO2 và O2, biết tỉ lệ mol CO2:O2 là 2:1.
\(a.\)
\(m_{hh}=0.12\cdot90+0.15\cdot58=19.5\left(g\right)\)
\(b.\)
\(V_{hh}=\left(0.25+0.1+0.05\right)\cdot22.4=8.96\left(l\right)\)
\(c.\)
\(n_A=\dfrac{10.08}{22.4}=0.45\left(mol\right)\)
\(M_A=23\cdot2=46\left(\dfrac{g}{mol}\right)\)
\(m_A=0.45\cdot46=20.7\left(g\right)\)
\(d.\)
\(n_{hh}=\dfrac{6.72}{22.4}=0.3\left(mol\right)\)
Vì CO2 : O2 = 2 : 1
\(\Rightarrow n_{CO_2}=0.2\left(mol\right),n_{O_2}=0.1\left(mol\right)\)
\(m_{hh}=0.2\cdot44+0.1\cdot32=12\left(g\right)\)
\(\overline{M}=\dfrac{12}{0.3}=40\left(\dfrac{g}{mol}\right)\)
Bài 7:
a) A là một oxit của lưu huỳnh có tỉ khối hơi đối với neon là 3,2. Xác định công thức phân tử của A.
b) B là oxit của nitơ có tỉ khối hơi so với metan( CH4) là 1,875. Xác định công thức phân tử của B.
c) C là hợp chất CxHy có tỉ khối hơi so với hidro là 15, biết cacbon chiếm 80% khối lượng phân tử. Xác định công thức phân tử của A.
Hỗn hợp A gồm 2 khí NO và NO2 có tỉ khối so với hidro bằng 17.Phần trăm về khối lượng của NO2 trong hỗn hợp khí A là:
Gọi số mol NO và NO2 lần lượt là a,b (mol)
Ta có: \(\dfrac{30a+46b}{a+b}=17.2\)
=> 30a + 46b = 34a + 34b
=> 4a = 12b => a = 3b
\(\%m_{NO_2}=\dfrac{46b}{30a+46b}.100\%=\dfrac{46b}{90b+46b}.100\%=33,82\%\)
Phần trăm khối lượng của N trong một oxit của nó là 30,43%.Tỉ khối của A so với He bằng 23. Xác định CTPT của oxit đó là:
A. N2O
B. N2O4
C. N2O5
D. NO2
Đáp án D
Phân tử khối của A là 46. Gọi công thức của oxit là NxOy
Có %N/%O=14x/16y= 30,43/69,57
suy ra x/y= 1/2 → Công thức đơn giản nhất là NO2
Mà MA= 46→ A là NO2
Bài 1. a) Tính tỉ khối hơi của khí SO2 so với khí O2 N2, SO3, CO, N2O, NO2.
b) Tính tỉ khối hơi của hỗn hợp khí A gồm SO2 và O2 có tỉ lệ mol 1:1 đối với khí O2.
Bài 2. a) Tính tỉ khối hơi của hỗn hợp khí X gồm hai khí N2 và CO đối với khí metan CH4. Hỗn hợp X nặng hay nhẹ hơn không khí?
b) Tính tỉ khối hơi của hỗn hợp Y đồng khối lượng gồm khí C2H4 (etilen), N2 và khí CO so với khí H2.
c) Hỗn hợp khí X gồm: NO, NxO, CH4. Trong đó NO chiếm 30% về thể tích, NxO chiếm 30% còn lại là CH4. Trong hỗn hợp CH4 chiếm 22,377% về khối lượng. Xác định công thức hoá học của NxO. Tính tỷ khối của X so với không khí
Bài 2:
a) Vì khối lượng mol của N2 và CO đều bằng 28 và lớn hơn khối lượng mol của khí metan CH4 (28>16)
=> \(d_{\dfrac{hhX}{CH_4}}=\dfrac{28}{16}=1,75\)
Hỗn hợp X nhẹ hơn không khí (28<29)
b)
\(M_{C_2H_4}=M_{N_2}=M_{CO}=28\left(\dfrac{g}{mol}\right)\\ \rightarrow M_{hhY}=28\left(\dfrac{g}{mol}\right)\\ d_{\dfrac{Y}{H_2}}=\dfrac{28}{2}=14\)
c) \(\%V_{NO}=100\%-\left(30\%+30\%\right)=40\%\\ \rightarrow\%n_{CH_4}=40\%\\ Vì:\%m_{CH_4}=22,377\%\\ Nên:\dfrac{30\%.16}{40\%.30+30\%.16+30\%.\left(x.14+16\right)}=22,377\%\\ \Leftrightarrow x=-0,03\)
Sao lại âm ta, để xíu anh xem lại như nào nhé.
Bài 1:
\(a.\\ d_{\dfrac{SO_2}{O_2}}=\dfrac{64}{32}=2\\ d_{\dfrac{SO_2}{N_2}}=\dfrac{64}{28}=\dfrac{16}{7}\\ d_{\dfrac{SO_2}{SO_3}}=\dfrac{64}{80}=0,8\\ d_{\dfrac{SO_2}{CO}}=\dfrac{64}{28}=\dfrac{16}{7}\\ d_{\dfrac{SO_2}{N_2O}}=\dfrac{64}{44}=\dfrac{16}{11}\\ d_{\dfrac{SO_2}{NO_2}}=\dfrac{64}{46}=\dfrac{32}{23}\\ b.M_{hhA}=\dfrac{1.64+1.32}{1+1}=48\left(\dfrac{g}{mol}\right)\\ d_{\dfrac{hhA}{O_2}}=\dfrac{48}{32}=1,5\)
Một oxit nitơ có CT NOx trong đó N chiếm 30,43% về khối lượng. Công thức của oxit nitơ đó là
A. NO
B. NO2
C. N2O2
D. N2O5