Để phân biệt etan, etilen và xiclopropan có thể sử dụng cặp hoá chất nào sau đây?
A. dd KMnO4 và dd Br2
B. dd Br2 và khí H2/Ni,t0
C. Khí O2, t0 và dd Br2
D. dd KMnO4 và khí H2/Ni,t0
Trong các phản ứng sau, có bao nhiêu phản ứng sinh ra đơn chất:
(1) H2S + SO2;
(2) KClO3 (t0, MnO2 xúc tác);
(3) CH3CHO + dd AgNO3/NH3, t0
(4) NH4NO3 (t0);
(5) H2O2 + dd KMnO4/H2SO4;
(6) C6H5NH2 + Br2 (dd);
(7) C2H5OH + O2 (men giấm);
(8)CH2Br-CH2Br + Zn (t0);
(9) C3H5(OH)3 + Cu(OH)2;
A. 4
B. 6
C. 7
D. 5
Cho 10g hỗn hợp khí X gồm etilen và etan qua dung dịch Br2 25% có 160g dd Br2 phản ứng. % khối lượng của etilen trong hỗn hợp là:
A. 70%
B. 30%
C. 35,5%
D. 64,5%
Đáp án A
Hướng dẫn
nC2H4 = nBr2 = 25 . 160 100 . 160 = 0,25 mol => %mC2H4 = 0 , 25 . 28 10 .100% = 70%
Cho hình vẽ mô tả thí nghiệm điều chế khí X trong phòng thí nghiệm :
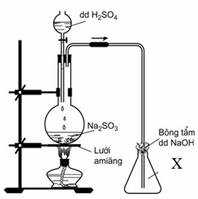
Trong điều kiện thích hợp, khí X có thể phản ứng được với mấy chất trong số các chất sau : dd KMnO4, nước Br2, dd FeCl3, khí H2S, Mg, dd NaOH dư, dd Na2SO3, dd BaCl2 ?
A. 6
B. 8.
C. 5.
D. 7
Chọn A
dd KMnO4, nước Br2,khí H2S, Mg, dd NaOH dư, dd Na2SO3
Cho hình vẽ mô tả thí nghiệm điều chế khí X trong phòng thí nghiệm :
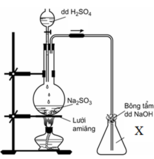
Trong điều kiện thích hợp, khí X có thể phản ứng được với mấy chất trong số các chất sau : dd KMnO 4 , nước Br 2 , dd FeCl 3 , khí H 2 S , Mg , dd NaOH dư, dd Na 2 SO 3 , dd BaCl 2 ?
A. 6.
B. 8.
C. 5.
D. 7.
Đáp án A
Từ hình vẽ mô tả thí nghiệm, ta thấy X là SO 2 :
![]()
SO 2 là một chất vừa có tính oxi hóa vừa có tính khử và là một oxit axit. Suy ra : Trong số các chất đề cho, SO 2 có thể phản ứng với 7 chất :
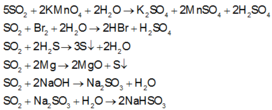
Trong các phản ứng sau, có bao nhiêu phản ứng sinh ra đơn chất:
(1) H2S + SO2;
(2) KClO3 (t0, MnO2 xúc tác);
(3) CH3CHO + dd AgNO3/NH3, t0
(4) NH4NO3 (t0);(5) Mg + dd giấm ăn;
(6) C6H5NH2 + Br2 (dd);
(7) C2H5OH + O2 (men giấm);
(8) Na + cồn 96 0 ;
(9) C3H5(OH)3 + Cu(OH)2;
![]()
![]()
![]()
![]()
đun nòn 0,11 mol hh khí T gồm CH4, C2H4, H2 (xúc tác Ni)sau 1 thời gian thu được 0,1 mol hh khí Q có tỉ khối so với H2 bằng 7,7
Cho Q lội qua dd Br2 dư thì có 4,8g Br2 tham gia pứ
Tính % thể tích H2 trong hh Q
\(m_Q=\left(7,7.2\right).0,1=1,54\left(g\right)\)
=> mT = 1,54 (g)
Gọi \(\left\{{}\begin{matrix}n_{CH_4}=a\left(mol\right)\\n_{C_2H_4}=b\left(mol\right)\\n_{H_2}=c\left(mol\right)\end{matrix}\right.\)
=> \(\left\{{}\begin{matrix}a+b+c=0,11\left(1\right)\\16a+28b+2c=1,54\left(2\right)\end{matrix}\right.\)
ngiảm = nH2(pư) = 0,11 - 0,1 = 0,01 (mol)
\(n_{Br_2}=\dfrac{4,8}{160}=0,03\left(mol\right)\)
Bảo toàn liên kết: b = 0,01 + 0,03 = 0,04 (mol) (3)
(1)(2)(3) => a = 0,02 (mol); b = 0,04 (mol); c = 0,05 (mol)
=> nH2(Q) = 0,05 - 0,01 = 0,04 (mol)
=> \(\%V_{H_2}=\dfrac{0,04}{0,1}.100\%=40\%\)
Dẫn 8,96 l hỗn hợp X gồm metan và etilen vào 200ml dd Br2. Sau pư hoàn toàn thấy thoát ra 2,24l khí
a, Tính %V mỗi khí trong hỗn hợp X
b,Tính Cm dd Br2 pư và cho biết sau khi pư kết thúc khối lượng bình Br2 tăng hay giảm bao nhiêu gam ?
a)
$V_{CH_4} = V_{khí\ thoát\ ra} = 2,24(lít)$
$\%V_{CH_4} = \dfrac{2,24}{8,96}.100\% = 25\%$
$\%V_{C_2H_4} = 100\% -25\% = 75\%$
b)
$n_{Br_2} = n_{C_2H_4} = \dfrac{8,96.75\%}{22,4} = 0,3(mol)$
$C_{M_{Br_2}} = \dfrac{0,3}{0,2} = 1,5M$
$m_{tăng} = m_{C_2H_4} = 0,3.28 = 8,4(gam)$
Cho sơ đồ phản ứng
Nhận xét nào sau đây sai ?
C r → t 0 + C l 2 , d ư X → + d d N a O H . d ư Y → + B r 2 , d d N a O H Z → + B a C l 2 T ↓
A. Trong phản ứng tạo Z, Y đóng vai trò là chất khử
B. Chất X vừa có tính oxi hóa, vừa có tính khử
C. Z có thể tác dụng với dung dịch HCl
D. T là kết tủa màu da cam
Cho 13,34 lít hỗn hợp gồm 2 khí là metan và axetilen đi qua bình đựng dd Br2 dư , thì dùng hết 250ml dd Br2 và thoát ra 5,6 lít khí
a/ Tính thành phần % thể tích các khí trong hỗn hợp
b/ Tính nồng độ mol dd Br đã dùng
c/ Tính thể tích O2 (đktc) cần dùng để đốt cháy hoàn toàn hỗn hợp khí trên.
mọi người giúp mik với mai mik kiểm tra 1 tiết rồi !!
Khí thoát ra là metan
\(\%V_{CH_4} = \dfrac{5,6}{13,44}.100\% =41,67\%\\ \%V_{C_2H_4} = 100\% - 41,67\% = 58,33\%\\ b) V_{C_2H_2} = 13,44 -5,6 = 7,84(lít)\\ n_{C_2H_2} = \dfrac{7,84}{22,4} = 0,35(mol)\\ C_2H_2 + 2Br_2 \to C_2H_2Br_4\\ n_{Br_2} = 2n_{C_2H_2} = 0,7(mol)\\ \Rightarrow C_{M_{Br_2}} = \dfrac{0,7}{0,25} = 2,8M\\ c)\)
\(CH_4 + 2O_2 \xrightarrow{t^o} CO_2 + 2H_2O\\ C_2H_4 + 3O_2 \xrightarrow{t^o} 2CO_2 + 2H_2O\\ V_{O_2} = 2V_{CH_4} + 3V_{C_2H_4} = 5,6.2 + 7,84.3 = 34,72(lít)\)