Cho phản ứng: SO2 + KMnO4 + H2O ® K2SO4 + MnSO4 + H2SO4.
Trong phương trình hóa học của phản ứng trên, khi hệ số của KMnO4 là 2 thì hệ số của SO2 là
A. 5
B. 7
C. 6
D. 4
Cho phản ứng:
SO2 + KMnO4 + H2O → K2SO4 + MnSO4 + H2SO4
Trong phương trình hóa học của phản ứng trên, khi hệ số của KMnO4 là 2 thì hệ số của SO2 là
A. 5
B. 6
C. 4
D. 7
Quan sát phương trình phản ứng ta thấy S tăng từ mức oxi hóa +4 lên mức oxi hóa +6; Mn giảm từ mức oxi hóa +7 xuống mức oxi hóa +2 → SO2 là chất khử và KMnO4 là chất oxi hóa.
5 x S + 4 → S + 6 + 2 e
2 x M n + 7 + 5 e → M n + 2
Suy ra phương trình phản ứng đã cân bằng như sau:
5SO2 + 2KMnO4 + 2H2O → K2SO4 + 2MnSO4 + 2H2SO4
Chọn đáp án A.
Cân bằng phương trình hóa học của phản ứng sau (với hệ số các chất là số nguyên tối giản) :
S O 2 + K M n O 4 + H 2 O → M n S O 4 + H 2 S O 4 + K 2 S O 4
Các hệ số của K M n O 4 v à H 2 S O 4 lần lượt là
A. 2 và 2
B. 2 và 5
C. 1 và 5
D. 1 và 3
Chọn A
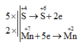
5SO2 + 2KMnO4 + 2H2O → 2MnSO4 + 2H2SO4 + K2SO4
→ Các hệ số của KMnO4 và H2SO4 lần lượt là 2 và 2
Cho phản ứng: KMnO4 + H2SO4 + KCl ® K2SO4 + MnSO4 + Cl2 + H2O
Trong phương trình hóa học của phản ứng trên, tỉ lệ số của KMnO4 và KCl là:
A. 2:5
B. 1:5
C. 2:6
D. 1:6
YTHH 05: Cân bằng nhanh theo bảo toàn nguyên tố:
1.KMnO4 thì sinh 1. MnSO4 và có 4.O chuyển hết về 4.H2O
Bảo toàn H suy ra có 4.H2SO4; bảo toàn S suy ra có 3.K2SO4; bảo toàn K suy ra có 5.KCl
Vậy KMnO4 + 4H2SO4 + 5KCl ® 3K2SO4 + MnSO4 + 2,5Cl2 + 4H2O
® tỉ lệ cần xác định là 1:5. Đáp án B.
Từ chất X (C6H5-CH2-CH=CH2), thực hiện phản ứng sau:
X + KMnO4 + H2SO4 → C6H5COOH + CO2 + MnSO4 + K2SO4 + H2O. Trong phương trình hóa học trên, khi hệ số của C6H5COOH là 5 thì hệ số của H2O là
A. 24
B. 34
C. 42
D. 48
Cho phản ứng :
R - C ≡ C - R ' + KMnO 4 + H 2 SO 4 → RCOOH + R ' COOH + K 2 SO 4 + MnSO 4 + H 2 O
Hệ số cân bằng trong phương trình hóa học của phản ứng trên lần lượt là :
A. 5; 6; 9; 5; 5; 6; 3; 5
B. 5; 6; 9; 5; 5; 6; 3; 4
C. 5; 6; 8; 5; 5; 6; 3; 4
D. 5; 6; 7; 5; 5; 6; 3; 4
Cho phương trình phản ứng:
SO2 + KMnO4 + H2O → K2SO4 + MnSO4 + H2SO4
Sau khi cân bằng với hệ số là các giá trị tối giản, hệ số của chất oxi hoá và chất khử là
A. 5 và 2.
B. 2 và 5.
C. 2 và 2.
D. 5 và 5.
Đáp án B.
5SO2 + 2KMnO4 + 2H2O → K2SO4 + 2MnSO4 + 2H2SO4
Cho phản ứng: C H 3 C H O + K M n O 4 + H 2 S O 4 → C H 3 C O O H + M n S O 4 + K 2 S O 4 + H 2 O
Hệ số cân bằng của phương trình hóa học trên là
A. 5, 2, 4, 5, 2, 1, 4.
B. 5, 2, 2, 5, 2, 1, 2.
C. 5, 2, 3, 5, 2, 1, 3
D. Tât cả đều sai.
Đáp án C
Hướng dẫn 5 C H 3 C H O + 2 K M n O 4 + 3 H 2 S O 4 → 5 C H 3 C O O H + 2 M n S O 4 + K 2 S O 4 + 3 H 2 O
Cho phản ứng:
C H 3 - C 6 H 4 - C H 2 - C H = C H 2 + K M n O 4 + H 2 S O 4 → H O O C - C 6 H 4 - C O O H + C O 2 + K 2 S O 4 + M n S O 4 + H 2 O
Tổng hệ số (nguyên, tối giản) tất cả các chất trong phương trình hóa học của phản ứng trên là:
A. 156
B. 129
C. 447
D. 17
Dẫn khí SO2 vào dung dịch KMnO4 màu tím nhận thấy dung dịch bị mất màu, vì xảy ra phản ứng hóa học sau:
SO2 + KMnO4 + H2O → K2SO4 + MnSO4 + H2SO4
Hãy cho biết vai trò của SO2 và KMnO4 trong phản ứng trên.
SO2 là chất khử, KMnO4 là chất oxi hóa.