Khi cho khí clo tác dụng với kim loại, em có nhận xét gì về mức độ hoạt động hoá học của nguyên tố clo. Cho thí dụ minh hoạ.

Những câu hỏi liên quan
Chọn các từ/cụm từ thích hợp dưới đây để hoàn thành nhận xét về tính chất hoá học của clo(mạnh/yếu,phi kim/kim loại,hidro/oxi)
Clo là một phi kim hoạt động hoá học...(1)...Clo có những tính chất hoá học của...(2)...như:tác dụng với hầu hết kim loại tạo thành muối clorua,tác dụng với...(3)...tạo thành khí hidro clorua
Clo là một phi kim hoạt động hoá học...(1)mạnh...Clo có những tính chất hoá học của...(2)phi kim...như:tác dụng với hầu hết kim loại tạo thành muối clorua,tác dụng với...(3)hidro...tạo thành khí hidro clorua
Đúng 5
Bình luận (0)
Cho các kim loại sau : kẽm ; magie ; đồng ; natri ; sắt.
Kim loại nào hoạt động hoá học yếu nhất ? Cho thí dụ minh hoạ.
Kim loại hoạt động hoá học yếu nhất là : đồng.
Thí dụ : Các kim loại Zn, Mg, Na, Fe tác dụng với dung dịch HCl. Kim loại Cu không tác dụng.
Đúng 0
Bình luận (0)
Cho các kim loại sau :kẽm ; magie ; đồng ; natri ; sắt.
Kim loại nào hoạt động hoá học mạnh nhất ? Cho thí dụ minh hoạ.
Kim loại hoạt động hoá học mạnh nhất là : natri.
Thí dụ : Chỉ Na phản ứng mạnh với nước ở nhiệt độ thường.
2Na + 2 H 2 O → 2NaOH + H 2
Đúng 0
Bình luận (0)
Người ta căn cứ vào tính chất hóa học nào để đánh giá clo là phi kim hoạt động hoá học mạnh ? Cho thí dụ minh họ
- Clo tác dụng với hầu hết các kim loại. Thí dụ : 2Fe + 3 Cl 2 → 2Fe Cl 3
- Clo tác dụng với hiđro (khi chiếu sáng hoặc đốt nóng) tạo thành hiđro elorua.
Đúng 0
Bình luận (0)
Làm thế nào để so sánh độ hoạt động hoá học mạnh hay yếu của phi kim ? Cho thí dụ minh hoạ.
Mức độ hoạt động hoá học mạnh, yếu của phi kim thường được xem xét qua khả năng phản ứng với hiđro hoặc với kim loại. Thí dụ :
H 2 + F 2 → bóng tối 2HF
H 2 + Cl 2 → t ° 2HCl
F hoạt động hóa học mạnh hơn Cl.
Đúng 0
Bình luận (0)
Các nguyên tố nhóm VII đều là những phi kim mạnh tương tự clo (trừ At): tác dụng với hầu hết kim loại tạo muối, tác dụng với hiđro tạo hợp chất khí. Viết phương trình hoá học minh hoạ với brom.
Các nguyên tố nhóm VIIA có tính chất hóa học tương tự clo.
Br2 + 2K 2KBr
3Br2 + 2Fe 2FeBr3
Br2 + H2 2HBr (k)
Đúng 0
Bình luận (0)
Bài 4. Các nguyên tố nhóm VII đều là những phi kim mạnh tương tự clo (trừ At): tác dụng với hầu hết kim loại tạo muối, tác dụng với hiđro tạo hợp chất khí. Viết phương trình hoá học minh hoạ với brom.
Lời giải:
Các nguyên tố nhóm VIIA có tính chất hóa học tương tự clo.
Br2 + 2K 2KBr
3Br2 + 2Fe 2FeBr3
Br2 + H2 2HBr (k)
Đúng 0
Bình luận (0)
Brom là một nguyên tố thuộc nhóm với Clo (VIIA) nên sẽ có tính chất hóa học tương tự với Clo.
- Tác dụng với kim loại:
+ PTHH: \(Br_2+2Na\rightarrow2NaBr\left(Natribromua\right)\)
+ PTHH: \(3Br_2+2Fe\rightarrow2FeBr_3\)( Sắt III brommua)
- Tác dung với hidro: PTHH: \(H_2+Br_2\rightarrow2HBr\) (Khí hdrobromua)
Ngoài ra brom có thể tác dung với NaI, H2O, ................ và đặc biệt: Br2 có tính oxi hóa mạnh hơn I2
Đúng 0
Bình luận (0)
Cho biết tính chất hóa học cơ bản của nguyên tố clo. Giải thích vì sao nguyên tố clo có tính chất hóa học cơ bản đó? Cho thí dụ minh họa.
Tính chất hóa học cơ bản của clo: Clo là chất oxi hóa mạnh.
- Tác dụng với kim loại : clo oxi hóa trực tiếp hầu hết các kim loại tạo muối clorua, phản ứng xảy ra ở nhiệt độ thường hoặc không cao lắm, tốc độ nhanh, tỏa nhiều nhiệt.
2Fe + 3Cl2 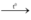 2FeCl3
2FeCl3
- Tác dụng với hiđro: Phản ứng xảy ra khi chiếu sáng bởi ánh sáng mặt trời:
H2 + Cl2 → 2HCl.
- Tác dụng với nước:
Trong phản ứng với nước, clo vừa là chất oxi hóa vừa là chất khử.
Cl2 + H2O ⇆ HCl + HClO
Sở dĩ có những tính chất hóa học cơ bản trên vì khi tham gia phản ứng, nguyên tử clo dễ nhận thêm 1 electron để thành ion Cl-. Vì vậy tính chất hóa học cơ bản của clo là tính oxi hóa mạnh.
Đúng 0
Bình luận (0)
Cho một luồng khí clo dư tác dụng với 9,2 gam kim loại sinh ra 23,4 gam muối của kim loại có hoá trị I. Hãy xác định tên của kim loại.
- Gọi kí hiệu và nguyên tử khối của kim loại là M.
Phương trình hoá học :
2M + Cl 2 → 2MCl
9,2 x 2(M + 35,5) = 2M x 23,4
653,2 = 28,4M
M = 23. Vậy kim loại M là kim loại natri (Na).
Đúng 2
Bình luận (0)
Trong những nhận xét dưới đây, nhận xét nào đúng?A. Nitơ không duy trì sự hô hấp vì nitơ là một khí độc.B. Vì có liên kết ba nên phân tử nitơ rất bền và ở nhiệt độ thường nitơ khá trơ về mặt hoá học.C. Khi tác dụng với kim loại hoạt động, nitơ thể hiện tính khử.D. Số oxi hoá của nitơ trong các hợp chất và ion AlN,
N
2
O
4
,
N
H
4
+
,...
Đọc tiếp
Trong những nhận xét dưới đây, nhận xét nào đúng?
A. Nitơ không duy trì sự hô hấp vì nitơ là một khí độc.
B. Vì có liên kết ba nên phân tử nitơ rất bền và ở nhiệt độ thường nitơ khá trơ về mặt hoá học.
C. Khi tác dụng với kim loại hoạt động, nitơ thể hiện tính khử.
D. Số oxi hoá của nitơ trong các hợp chất và ion AlN, N 2 O 4 , N H 4 + , N O 3 - , N O 2 - lần lượt là -2, +4, -3, +5, +3.











