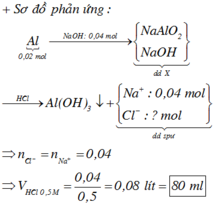
Cho 5,4 gam Al vào 100 ml dung dịch H 2 SO 4 0,5M. Tính thể tích khí H 2 sinh ra (đktc).

Những câu hỏi liên quan
Cho 5,4 gam Al vào 100 ml dung dịch H 2 SO 4 0,5M. Tính nồng độ mol của các chất trong dung dịch sau phản ứng. Cho ràng thể tích dung dịch sau phản ứng thay đổi không đáng kể.
n Al 2 SO 4 3 = 0,05/3 x 1 ≈ 0,017 mol
C M Al 2 SO 4 3 = 0,017/0,1 = 0,17M
Đúng 0
Bình luận (0)
Cho 0,54 gam Al vào 100 ml dung dịch H2SO4 0,5M, biết phản ứng xảy ra hoàn toàn.
a) Tính thể tích khí hydrogen sinh ra (đkc). Biết ở điều kiện chuẩn (1 bar, 25°C), 1 mol khí chiếm thể tích 24,79 lít.
b) Tính nồng độ mol của các chất trong dung dịch sau phản ứng, biết rằng thể tích dung dịch sau phản ứng thay đổi không đáng kể
Cho 5,4 gam Al vào 400 ml dung dịch CuSO4 0,5M. Sau phản ứng hoàn toàn, thu được m gam chất rắn. Giá trị của m là
A. 12,8.
B. 14,6
C. 13,7
D. 15,5
Bài 1:Hòa tan hoàn toàn 7,2 gam Mg trong V ml dung dịch HCl 3M.Gía trị của V là
Bài 2:Cho từ từ 3,25 gam Zn vào 120 ml dung dịch HCl 1M.Xác định thể tích khí hydrogen thoát ra (đkc)
Bài 3:Cho từ từ 5,4 gam Al vào 450ml dung dịch H2SO4 1M.Tính khối lượng muối tạo thành
Bài 3:
\(n_{Al}=\dfrac{5,4}{27}=0,2\left(mol\right);n_{H_2SO_4}=0,45.1=0,45\left(mol\right)\\ PTHH:2Al+3H_2SO_4\rightarrow Al_2\left(SO_4\right)_3+3H_2\\ Vì:\dfrac{0,2}{2}< \dfrac{0,45}{3}\Rightarrow H_2SO_4dư\\ n_{Al_2\left(SO_4\right)_3}=\dfrac{n_{Al}}{2}=\dfrac{0,2}{2}=0,1\left(mol\right)\\ m_{muối}=m_{Al_2\left(SO_4\right)_3}=342.0,1=34,2\left(g\right)\)
Đúng 1
Bình luận (0)
Bài 2:
\(n_{Zn}=\dfrac{3,25}{65}=0,05\left(mol\right);n_{HCl}=0,12.1=0,12\left(mol\right)\\ Zn+2HCl\rightarrow ZnCl_2+H_2\\ Vì:\dfrac{0,05}{1}< \dfrac{0,12}{2}\Rightarrow HCldư\\ n_{H_2}=n_{Zn}=0,05\left(mol\right)\\ V_{H_2\left(đkc\right)}=0,05.24,79=1,2395\left(l\right)\)
Đúng 1
Bình luận (0)
Bài 1:
\(n_{Mg}=\dfrac{7,2}{24}=0,3\left(mol\right)\\ PTHH:Mg+2HCl\rightarrow MgCl_2+H_2\\ n_{HCl}=2n_{Mg}=2.0,3=0,6\left(mol\right)\\ V_{ddHCl}=\dfrac{0,6}{3}=0,2\left(l\right)=200\left(ml\right)\)
Đúng 1
Bình luận (0)
Xem thêm câu trả lời
Cho 0,54 gam Al vào 40 ml dung dịch NaOH 1M, sau phản ứng thu được dung dịch X. Cho từ từ dung dịch HCl 0,5M vào dung dịch X thu được kết tủa. Để thu được kết tủa lớn nhất thì thể tích dung dịch HCl 0,5M cần dùng là A. 110 ml. B. 40 ml. C. 70 ml. D. 80 ml.
Đọc tiếp
Cho 0,54 gam Al vào 40 ml dung dịch NaOH 1M, sau phản ứng thu được dung dịch X. Cho từ từ dung dịch HCl 0,5M vào dung dịch X thu được kết tủa. Để thu được kết tủa lớn nhất thì thể tích dung dịch HCl 0,5M cần dùng là
A. 110 ml.
B. 40 ml.
C. 70 ml.
D. 80 ml.
Cho 8,3 gam hỗn hợp Al, Fe vào 300 ml dung dịch HCl 1M và
H
2
SO
4
0,5M, thu được dung dịch X và thấy thoát ra 5,6 lít
H
2
(đktc). Tính thể tích dung dịch NaOH 1M cần cho vào dung dịch X để thu được kết tủa có khối lượng lớn nhất ? A. 300 ml B. 500 ml C. 400 ml D. 600 ml
Đọc tiếp
Cho 8,3 gam hỗn hợp Al, Fe vào 300 ml dung dịch HCl 1M và H 2 SO 4 0,5M, thu được dung dịch X và thấy thoát ra 5,6 lít H 2 (đktc). Tính thể tích dung dịch NaOH 1M cần cho vào dung dịch X để thu được kết tủa có khối lượng lớn nhất ?
A. 300 ml
B. 500 ml
C. 400 ml
D. 600 ml
Đáp án D
Trong dung dịch axit, ta có :
n Cl - = n HCl = 0 , 3 mol
n SO 4 2 - = n H 2 SO 4 = 0 , 15 mol
Sơ đồ phản ứng :

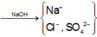
Cho NaOH vào X để thu được kết tủa lớn nhất thì dung dịch sau phản ứng chỉ còn các ion Na + , Cl - và SO 4 2 - .
Áp dụng bảo toàn điện tích trong dung dịch sau phản ứng và bảo toàn nguyên tố Na, ta có :
n NaOH = n Na + = n Cl - + 2 n SO 4 2 - = 0,6 mol
→ V dd NaOH 1 M = 0,6 lit = 600ml
Đúng 0
Bình luận (0)
Cho 0,96 gam Cu vào 100 ml dung dịch chứa đồng thời HNO3 1M thấy sinh ra một chất khí A có dA/H2 = 15 và dung dịch A.
a) Tính thể tích khí sinh ra ở đktc?
b) Tính thể tích dung dịch NaOH 0,5M tối thiểu cần dùng để kết tủa hoàn toàn Cu2+
a) \(M_A=15.2=30\left(g/mol\right)\)
=> A là NO
\(n_{Cu}=\dfrac{0,96}{64}=0,015\left(mol\right)\)
nHNO3 = 0,1.1 = 0,1 (mol)
PTHH: 3Cu + 8HNO3 --> 3Cu(NO3)2 + 2NO + 4H2O
_____0,015->0,04---------->0,015-------->0,01
=> VNO = 0,01.22,4 = 0,224(l)
b) A chứa: 0,015 mol Cu(NO3)2 và 0,06 mol HNO3
=> \(\left\{{}\begin{matrix}Cu^{2+}:0,015\\H^+:0,06\end{matrix}\right.\)
H+ + OH- --> H2O
0,06->0,06
Cu2+ + 2OH- --> Cu(OH)2
0,015->0,03
=> \(n_{OH^-}=0,09\left(mol\right)\) => nNaOH = 0,09 (mol) => \(V_{dd}=\dfrac{0,09}{0,5}=0,18\left(l\right)\)
Đúng 0
Bình luận (0)
Bài 1: Hòa tan 4,5 gam hợp kim nhôm, magie trong dung dịch H2SO4 loãng, dư, thấy có 5,04 lít khí hiđro bay ra (đktc).A) Viết phương trình hoá học. B) Tính thành phần phần trăm khối lượng của các kim loại trong hợp kim.Bài 2: Cho 5,4 gam Al vào 100 ml dung dịch H2SO4 0.5M.A) Tính thể tích khí H2 sinh ra (đktc).B) Tính nồng độ mol của các chất trong dung dịch sau phản ứng. Cho rằng thể tích dung dịch sau phản ứng thay đổi không đáng kể.
Đọc tiếp
Bài 1: Hòa tan 4,5 gam hợp kim nhôm, magie trong dung dịch H2SO4 loãng, dư, thấy có 5,04 lít khí hiđro bay ra (đktc).
A) Viết phương trình hoá học.
B) Tính thành phần phần trăm khối lượng của các kim loại trong hợp kim.
Bài 2: Cho 5,4 gam Al vào 100 ml dung dịch H2SO4 0.5M.
A) Tính thể tích khí H2 sinh ra (đktc).
B) Tính nồng độ mol của các chất trong dung dịch sau phản ứng. Cho rằng thể tích dung dịch sau phản ứng thay đổi không đáng kể.
1.nH2=5.04/22.4=0.225mol
Đặt x,y lần lượt là số mol của Al,Mg
a)2Al + 3H2SO4 --> Al2(SO4)3 + 3H2
x 3/2 x
Mg+ H2SO4 --> MgSO4 + H2
y y
b) theo đề, ta có hệ pt: 27x + 24y= 4.5
1.5x + y =0.225
giải hệ pt trên,ta có :x=0.1 ; y=0.075
thay vào pt,suy ra :
mAl=0.1*27=2.7g =>%Al=(2.7/4.5)*100=60%
=>%Mg=40%
vậy % của Al,Mg lần lượt là 60% và 40%
2.nAl=5.4/27=0.2mol
nH2SO4=0.5*0.1=0.05 mol
pt:2Al + 3H2SO4 --> Al2(SO4)3 + 3H2
0.2 0.05 0.02 0.05
a)theo pt, ta thấy Al dư
VH2=0.05*22.4=1.12 l
b)CMAl2(SO4)3= 0.02/0.1=0.2M
Bài này không khó đâu nh,tính theo pthh thôi à.
Chúc em học tốt!!!:))
Đúng 1
Bình luận (3)
Cho 200 ml dung dịch X gồm Ba(OH)2 0,5M và NaAlO2 (hay Na[Al(OH)4]) 1,5M. Thêm từ từ dung dịch H2SO4
0,5M vào dung dịch X cho đến khi kết tủa tan trở lại 1 phần, thu được kết tủa Y. Đem nung kết tủa Y này đến khối lượng
không đổi thu được 24,32 gam chất rắn Z. Thể tích dung dịch H2SO4 0,5M đã dùng là
-cho h2so4 vô X thì chắc chắn có tủa baso4 và mất 0.2 mol OH- tại axit td bazo đầu tiên(tủa Al(oh)3 tan là nhờ axit chứ ko nhờ oh- nữa nhé) => đã có 0.1 mol h2so4 td rùi -> 0.1 mol baso4=> 23.3 g baso4
-Có 24.32 g = 23.3 + m Al2O3 => 0.01 mol Al2o3 => 0.02 Al(oh)3 sau p ứng.
-Mà cho 0.3 mol NaAlO2 => tạo tủa 0.3 mol và mất 0.28 mol td axit còn 0.02 như ở trên
-n h2so4 quá trình này = (0.3 + 0.28 .3) / 2 =0.57
-nh2so4 = 0.57 + 0.1 = 0.67 => V = 1.34 l
Đúng 0
Bình luận (0)