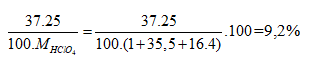Khí clo có khối lượng nguyên tử bằng 35,468 u. Khí này là hỗn hợp đồng vị bền là: Cl 35 = 34 , 969 u , Cl 37 = 66 , 996 u
Tỉ lệ khối lượng giữa hai đồng vị này trong khí clo là:
A. 2,8
B.3
C. 3,1
D. 3,2
Khí clo có khối lượng nguyên tử bằng 35,468 u. Khí này là hỗn hợp đồng vị bền là 35Cl = 34,969 u và 37Cl = 36,996 u. Tỉ lệ khối lượng giữa hai đồng vị này trong khí clo là
A. 2,8
B. 3,0
C. 3,1
D. 3,2
Khí clo là hỗn hợp của hai đồng vị bền là C 35 l = 34 ٫ 969 u hàm lượng 75 ٫ 4 % và C 37 l = 36 ٫ 966 u hàm lượng 24 ٫ 6 % . Tính khối lượng nguyên tử của nguyên tố hoá học clo.
A. 35,46u.
B. 35,97u.
C. 35,95u.
D. 35,42u.
Khí Clo là hỗn hợp của hai đồng vị bền là C 35 l = 34,969 u hàm lượng 75,4% và C 17 l = 36,966 u hàm lượng 24,6%.
Tính khối lượng nguyên tử của nguyên tố hoá học clo.
Khối lượng nguyên tử của clo :
34,969 u.75,4% + 36,966 u.24,6% = 35,46 u
Khí clo trong tự nhiên có thể coi là hỗn hợp của hai đồng vị chính là C35 có khối lượng nguyên tử là 34,969 u và C37 có khối lượng nguyên tử là 36,996 u. Cho khối lượng nguyên tử của clo trong tự nhiên là 35,453. Xác định tí lệ % số hạt C35 trong tự nhiên.
A.78,5%
B. 79,5%
C. 68,5%
D. 70,5%
Đáp án: A.
Gọi tỉ lệ số hạt của C35 trong tự nhiên là x thì:
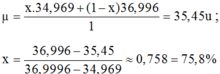
Trong tự nhiên có 35 Cl và 37 Cl. Khối lượng của 1 lít khí clo ở đktc là 3,17g.
a,Tính thành phần phần trăm về số nguyên tử từng đồng vị trong tự nhiên.
b,Tính số nguyên tử 37 Cl có trong 1 lít khí clo (đktc)
c,Tính thành phần phần trăm về khối lượng của đồng vị 35 Cl trong KClO.
( biết K=39, O=16)
Nguyên tố Clo có hai đồng vị bền là: 35Cl(75,77%) và 37Cl(24,23%)
a, Tính số nguyên tử của từng đồng vị trong 8,96l khí Clo(đktc) và nguyên tử khối trung bình của Clo
b, Tính phần trăm về khối lượng của 35Clo có trong FeCl3. Cho Fe=56
Áp dụng công thức tính nguyên tử khối trung bình:
Trong đó đồng vị A có x% số nguyên tử, đồng vị B có y% số nguyên tử.
Vậy nguyên tử khối trung bình của nguyên tố clo bằng:
Trong tự nhiên clo có 2 đồng vị bền 35 17Cl và 37 17Cl . Nguyên tử khối trung bình của nguyên tố clo là 35,485. Tính thành phần phần trăm khối lượng của 37 17Cl có trong hợp chất HClO2
Nguyên tử khối trung bình của Clo là 35,5. Clo trong tự nhiên có hai đồng vị là 35 Cl và 37 Cl. Tính phần trăm về khối lượng của 37 Cl chứa trong HClO4 (với Hidro đồng vị là 1 H, oxi đồng vị là 16 O)
\(\%^{35}Cl=x\%\Rightarrow\%^{37}Cl=\left(100-x\right)\%\)
\(\overline{M}=\dfrac{35x+37\cdot\left(100\%-x\right)}{100\%}=35.5\left(g\text{/}mol\right)\)
\(\Rightarrow x=75\%\)
\(\%^{37}Cl_{\left(HClO_4\right)}=\dfrac{25\%\cdot37}{1+35.5+16\cdot4}\cdot100\%=9.2\%\)
Phần trăm đồng vị 35Cl = x, thì % đồng vị 37Cl = 100 - x
Ta có:
, vậy x = 75%.
Phần trăm khối lượng của 37Cl trong HClO4=
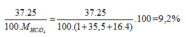
Nguyên tử khối trung bình của clo là 35,5. Clo trong tự nhiên có 2 đồng vị là 35 Cl và 37Cl. Phần trăm khối lượng của 3717Cl chứa trong HClO4 ?(với hidro là đồng vị 11H, oxi là đồng vị 168O) là.
Tham thảo :
Phần trăm đồng vị 35Cl = x, thì % đồng vị 37Cl = 100 - x
Ta có:
![]() , vậy x = 75%.
, vậy x = 75%.
Phần trăm khối lượng của 37Cl trong HClO4=