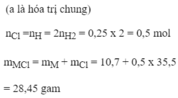Một dung dịch X có chứa 46,5 gam hỗn hợp NaCl, Mg Cl 2 , Zn Cl 2 phản ứng vừa đủ với dung dịch Ag NO 3 thu được 114,8 gam kết tủa và dung dịch Y. Tính khối lượng muối trong dung dịch Y.

Những câu hỏi liên quan
. Hòa tan 32 gam X gồm Fe, Mg, Al, Zn bằng dung dịch HCl dư thu được 2,24 lít H 2
(đktc). Mặt khác 32 gam X tác dụng với Cl 2 dư thì có 3,36 lít Cl 2 đktc ) tham gia phản ứng. Tính phần
trăm khối lượng Fe trong hỗn hợp X.
\(n_{Fe}=a\left(mol\right),n_{Mg}=b\left(mol\right),n_{Al}=c\left(mol\right),n_{Zn}=d\left(mol\right)\)
\(n_{H_2}=\dfrac{2.24}{22.4}=0.1\left(mol\right)\)
\(\)\(BTe:\)
\(2a+2b+3c+2d=0.2\left(1\right)\)
\(n_{Cl_2}=\dfrac{3.36}{22.4}=0.15\left(mol\right)\)
\(BTe:\)
\(3a+2b+3c+2c=0.15\cdot2=0.3\left(2\right)\)
\(\left(2\right)-\left(1\right):a=0.3-0.2=0.1\)
\(\%Fe=\dfrac{0.1\cdot56}{32}\cdot100\%=17.5\%\)
Đúng 0
Bình luận (0)
KHẨN CẦU MỌI NGƯỜI GIẢI NHANH GIÚP EM VỚI Ạ!!! :câu 1:Dung dịch X chứa các ion: Fe2+ (0,1 mol), Al3+ (0,2 mol), Cl- (x mol), SO42- (y mol). Cô cạn dung dịch X thu được 44,4 gam muối rắn. Tìm giá trị x và y?Câu 2 : Cho 5,1 gam hỗn hợp Al và Mg tác dụng với dung dịch HNO3 loãng dư, thu được dung dịch X và 1,12 lít khí N2 (đktc, sản phẩm khử duy nhất). Khối lượng muối thu được trong X là?Câu 3 : Trộn 200ml dung dịch gồm HCl 0,01M và H2SO4 0,02M với 300ml dung dịch KOH 0,03M. Tính pH dung dịch thu đ...
Đọc tiếp
KHẨN CẦU MỌI NGƯỜI GIẢI NHANH GIÚP EM VỚI Ạ!!! :<<<<
câu 1:Dung dịch X chứa các ion: Fe2+ (0,1 mol), Al3+ (0,2 mol), Cl- (x mol), SO42- (y mol). Cô cạn dung dịch X thu được 44,4 gam muối rắn. Tìm giá trị x và y?
Câu 2 : Cho 5,1 gam hỗn hợp Al và Mg tác dụng với dung dịch HNO3 loãng dư, thu được dung dịch X và 1,12 lít khí N2 (đktc, sản phẩm khử duy nhất). Khối lượng muối thu được trong X là?
Câu 3 : Trộn 200ml dung dịch gồm HCl 0,01M và H2SO4 0,02M với 300ml dung dịch KOH 0,03M. Tính pH dung dịch thu được?
(Cho biết Fe=56; Al=27; Cl=35,5; S=32; O=16; H=1; N=14)
Câu 1:
Theo ĐLBT ĐT, có: x + 2y = 0,1.2 + 0,2.3 (1)
Theo ĐLBT KL, có: 35,5x + 96y = 44,4 - 0,1.56 - 0,2.27 (2)
Từ (1) và (2) \(\Rightarrow\left\{{}\begin{matrix}x=0,4\left(mol\right)\\y=0,2\left(mol\right)\end{matrix}\right.\)
Câu 2:
Gọi: \(\left\{{}\begin{matrix}n_{Al}=x\left(mol\right)\\n_{Mg}=y\left(mol\right)\end{matrix}\right.\)
⇒ 27x + 24y = 5,1 (1)
Có: \(n_{N_2}=0,05\left(mol\right)\)
Theo ĐLBT e, có: 3x + 2y = 0,05.10 (2)
Từ (1) và (2) \(\Rightarrow x=y=0,1\left(mol\right)\)
BTNT Al và Mg, có: \(n_{Al\left(NO_3\right)_3}=n_{Mg\left(NO_3\right)_2}=0,1\left(mol\right)\)
⇒ m muối = 0,1.213 + 0,1.148 = 36,1 (g)
Câu 3:
Có: \(n_{H^+}=0,2.0,01+0,2.0,02.2=0,01\left(mol\right)\)
\(n_{OH^-}=0,3.0,03=0,009\left(mol\right)\)
PT: \(H^++OH^-\rightarrow H_2O\)
__0,01___0,009 (mol)
⇒ H+ dư và nH+ (dư) = 0,001 (mol)
\(\Rightarrow\left[H^+\right]=\dfrac{0,001}{0,2+0,3}=0,002\left(M\right)\)
\(\Rightarrow pH=-log0,002\approx2,7\)
Bạn tham khảo nhé!
Đúng 2
Bình luận (0)
1)Cho dung dịch chứa 34,2g bari hiđroxit vào dung dịch chứa 18,25g axit clohiđric, dung dịch sau phản ứng có (cho Ba137; O16; H1; Cl35,5)A. pH 7.B. pH 7.C. pH 7.D. pH 9.2)Cho 1,5 gam hỗn hợp (X) gồm Mg và MgO tác dụng với axit HCl dư, thu được 0,336 lít khí hiđro (đktc). Thành phần phầm trăm của mỗi chất trong (X) là: (Cho Mg24; O16; H1; Cl35,5.)A. 50% Mg và 50% MgOB. 25% Mg và 75% MgOC. 24% Mg và 76% MgOD. 30% Mg và 70% MgO3)Dãy các kim loại nào sau đây được sắp xếp đúng theo chiều hoạt độn...
Đọc tiếp
1)Cho dung dịch chứa 34,2g bari hiđroxit vào dung dịch chứa 18,25g axit clohiđric, dung dịch sau phản ứng có (cho Ba=137; O=16; H=1; Cl=35,5)
A. pH > 7.
B. pH < 7.
C. pH = 7.
D. pH > 9.
2)Cho 1,5 gam hỗn hợp (X) gồm Mg và MgO tác dụng với axit HCl dư, thu được 0,336 lít khí hiđro (đktc). Thành phần phầm trăm của mỗi chất trong (X) là: (Cho Mg=24; O=16; H=1; Cl=35,5.)
A. 50% Mg và 50% MgO
B. 25% Mg và 75% MgO
C. 24% Mg và 76% MgO
D. 30% Mg và 70% MgO
3)
Dãy các kim loại nào sau đây được sắp xếp đúng theo chiều hoạt động hóa học tăng dần?
A. Cu, Fe, Zn, Al, Mg, K.
B. Fe, Cu, K, Mg, Al, Zn.
C. K, Mg, Cu, Al, Zn, Fe.
D. Zn, K, Mg, Cu, Al, Fe.
Câu 1: Cho 7,84l(đktc) hỗn hợp khí O và Cl tác dụng vừa đủ với 0,1 mol Mg và 0,3 mol Al, thu được M gam hỗn hợp muối clorua và oxit.Tính giá trị của M
Câu 2: Tính nồng độ mol có 500ml dung dịch X chứa 5,85g NaCl và 7,1g Na2SO4
Cho m gam hỗn hợp X gồm các kim loại Al, Mg, Fe, Zn, tác dụng vừa đủ với dung dịch HCl tạo ra 1,456 lít (đktc) H2. Cũng m gam hỗn hợp X tác dụng với khí Cl dư tạo ra (m+4,97) g hỗn hợp các muối. Khối lượng Fe trong m gam X là?
Khi cho 2,00 gam hỗn hợp X gồm Mg, Al, Zn và Fe phản ứng hoàn toàn với lượng dư dung dịch HCl thì
thu được 1,12 lít khí H 2 . Nếu cho 2,00 gam hỗn hợp X như trên phản ứng hoàn toàn với lượng dư khí Cl 2 thì thu
được 5,763 gam hỗn hợp muối. Tính % khối lượng của Fe có trong hỗn hợp X.
có nH2 = 1,12/22,4 = 0,05 mol
Áp dụng ĐLBT nguyên tố với H :
có nHCl = 2nH2 = 0,05.2 =0,1 mol
Áp dụng ĐLBT khối lượng , có :
mKL + mHCl = m muối + mH2
➜ m muối = 2 + 0,1.36,5 - 0,05.2 = 5,55 gam
có mCl-thêm vào= mmuối(TN2)-mmuối(TN2)=5,763-5,55 = 0,213 gam
⇒ nCl-thêm vào = 0,213/35,5 = 0,006 mol
PTHH :
FeCl2 + Cl- → FeCl3
0,006 0,006 (mol)
⇒ nFeCl2= nCl =0,006 mol
BTNT với Fe , có nFe = nFeCl2 = 0,006 mol
⇒ %mFe = \(\frac{0,006.56}{2}\) .100% = 16,8%
Đúng 0
Bình luận (0)
Câu 1: Một dung dịch không thể chứa đồng thời các ion sau:A. NH_4^+;CO_3^-;SO_4^{2-};Na^+ B.K^+;Zn^{2+};Cl^-;Br^-C. Ag^+;Al^{3+};PO_4^{3-};CO_3^{2-} D. Ba^{2+};Mg^{2+};Cl^-;NO_3^-Câu 2: Các ion nào sau đây không cùng tồn tại trong một dung dịch ?A. Na^+;Mg^{2+};OH^-B. K^+;Fe^{2+};NO_3^-C. Ca^{2+};Na^+;Cl^-D. Al^{3+};Cu^{2+};SO_4^{2-}Câu 3: Dung dịch nào sau đây tồn tại được A. Na^+;Mg^{2+};OH^-;NO_3^-B. Ag^+;H^+;Cl^-;SO_4^{2-}C. HSO_4^-;Na^+;Ca^{2+};CO_...
Đọc tiếp
Câu 1: Một dung dịch không thể chứa đồng thời các ion sau:
A. \(NH_4^+;CO_3^-;SO_4^{2-};Na^+\)
\(B.K^+;Zn^{2+};Cl^-;Br^-\)
C. \(Ag^+;Al^{3+};PO_4^{3-};CO_3^{2-}\)
D. \(Ba^{2+};Mg^{2+};Cl^-;NO_3^-\)
Câu 2: Các ion nào sau đây không cùng tồn tại trong một dung dịch ?
A. \(Na^+;Mg^{2+};OH^-\)
B. \(K^+;Fe^{2+};NO_3^-\)
C. \(Ca^{2+};Na^+;Cl^-\)
D. \(Al^{3+};Cu^{2+};SO_4^{2-}\)
Câu 3: Dung dịch nào sau đây tồn tại được
A. \(Na^+;Mg^{2+};OH^-;NO_3^-\)
B. \(Ag^+;H^+;Cl^-;SO_4^{2-}\)
C. \(HSO_4^-;Na^+;Ca^{2+};CO_3^-\)
D. \(OH^-;Na^+;Ba^{2+};Cl^-\)
Câu 4: Ion \(CO_3^{2-}\) không phản ứng được với ion nào sau đây ?
A. \(Ca^{2+};Mg^{2+}\)
B. \(H^+;NH_4^+;Na^+;K^+\)
C. \(Ba^{2+};Cu^{2+};NH_4^+;K^+\)
D. \(NH_4^+;Na^+;K^+\)
Câu 1: Chọn C (\(2Al^{^{3+}}+3CO_3^{^{2-}}+3H_2O->2Al\left(OH\right)_3+3CO_2\), bị thuỷ phân)
Câu 2: Chọn A (\(Mg^{^{2+}}+2OH^{^-}->Mg\left(OH\right)_2\), không tan)
Câu 3: Chọn C (\(Ca^{^{2+}}+CO_3^{^{2-}}->CaCO_3\), không tan)
Câu 4: Chọn D. Các chất tạo thành đều là chất tan, tạo thành dung dịch gồm 4 ion đó.
Đúng 2
Bình luận (0)
Một hỗn hợp foomf Fe, Mg, Al có khối lượng 10,7 gam cho tan hoàn toàn trong dung dịch HCl thì thu được 5,6 lít khí (ở đktc). Khi chưng khô dung dịch thu được bao nhiêu gam muối (Cl=35,5)?
Hòa tan hoàn toàn 104,25 g hỗn hợp gồm NaCl và NaI vào nước được dung dịch A. Sục khí Cl2 dư vào dung dịch A kết thúc thí nghiệm, cô cạn dung dịch thu được 58,5g muối khan. Khối lượng NaCl có trong hỗn hợp X là