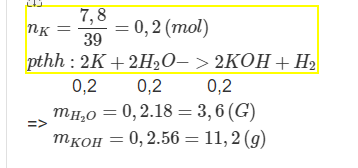tính khối lượng của H2O; NaCL, N2 để có cùng số phân tử bằng nhau

Những câu hỏi liên quan
Tính khối lượng của H2 và khối lượng NaOH tạo thành khi cho 2mol Na tác dụng với H2O,biết phương trình phản ứng
Na+H2O -> NaOH + H2
\(2Na+2H_2O\rightarrow2NaOH+H_2\)
\(\dfrac{2}{2}\) = \(\dfrac{2}{2}\) ( mol )
2 2 2 2 ( mol )
( Cả 2 chất đều không dư )
\(m_{H_2}=1.2=2g\)
\(m_{NaOH}=2.40=80g\)
Đúng 2
Bình luận (1)
\(2Na+2H_2O\rightarrow2NaOH+H_2\)
2 2 1 ( mol )
\(m_{H_2}=1.2=2g\)
\(m_{NaOH}=2.40=80g\)
Tính khối lượng của CO2 và khối lượng H2O tạo thành khi cho 3 mol O2 tác dụng với CH4,biết phương trình phản ứng
CH4+O2 -> CO2 + H2O
\(CH_4+2O_2\rightarrow\left(t^o\right)CO_2+2H_2O\)
3 1,5 3 ( mol )
\(m_{CO_2}=1,5.44=66g\)
\(m_{H_2O}=3.18=54g\)
Đúng 2
Bình luận (0)
Để đốt cháy hoàn toàn 2,50 g chất A phải dùng vừa hết 3,36 lít
O
2
(đktc). Sản phẩm cháy chỉ có
C
O
2
và
H
2
O
, trong đó khối lượng
C
O
2
hơn khối lượng
H
2
O
là 3,70 g. Tính phần trăm khối lượng của từng nguyên tố tron...
Đọc tiếp
Để đốt cháy hoàn toàn 2,50 g chất A phải dùng vừa hết 3,36 lít O 2 (đktc). Sản phẩm cháy chỉ có C O 2 và H 2 O , trong đó khối lượng C O 2 hơn khối lượng H 2 O là 3,70 g. Tính phần trăm khối lượng của từng nguyên tố trong chất A.
Khi A tác dụng với O 2 chỉ sinh ra, và H 2 O , vậy A có chứa cacbon, hiđro, có thể có hoặc không có oxi.
Theo định luật bảo toàn khối lượng :
m C O 2 + m H 2 O = m A + m O 2 = 7,30 (g) (1)
Theo đầu bài: m C O 2 + m H 2 O = 3,70(g). (2)
Từ hệ (1) và (2), tìm được m C O 2 = 5,50 g; m H 2 O = 1,80 g.
Khối lượng C trong 5,50 g
C
O
2
: 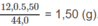
Khối lượng H trong 1,8 g
H
2
: 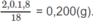
Đó cũng là khối lượng c và H trong 2,50 g chất A. Vậy chất A phải chứa O.
Khối lượng O trong 2,50 g A: 2,50 - 1,50 - 0,200 = 0,80 (g)
Phần trăm khối lượng của C: 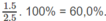
Phần trăm khối lương của H: 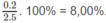
Phần trăm khối lương của O: 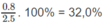
Đúng 0
Bình luận (0)
Bài 1: NaOH + HCl - NaCl + H2O 2H2 + O2 - 2H2OCho khối lượng của NaOH là 4gam. Tính thể tích khí O2 cần dùng để tạo ra lượng H2O bằng lượng H2O trong phản ứng của NaOH với HClBài 2: Cho số Avogadro6x1023 . Trong 0,69 mol KMnO4 có bao nhiêu nguyên tửBài 3: CH4 + 2Cl2 - CH2Cl2 + 2HCl ( đk: á/s, 1:2 ). Cho thể tích của CH4 là 17,92 lít, của Cl2 là 11200 cm3. Tính thể tích Ba(OH)2 được trung hòa bằng lượng HCl tạo thành, biết: Ba(OH)2 + 2HCl - BaCl2 + 2H2OBài 4: Trong...
Đọc tiếp
Bài 1: NaOH + HCl -> NaCl + H2O
2H2 + O2 -> 2H2O
Cho khối lượng của NaOH là 4gam. Tính thể tích khí O2 cần dùng để tạo ra lượng H2O bằng lượng H2O trong phản ứng của NaOH với HCl
Bài 2: Cho số Avogadro=6x1023 . Trong 0,69 mol KMnO4 có bao nhiêu nguyên tử
Bài 3: CH4 + 2Cl2 -> CH2Cl2 + 2HCl ( đk: á/s, 1:2 ). Cho thể tích của CH4 là 17,92 lít, của Cl2 là 11200 cm3. Tính thể tích Ba(OH)2 được trung hòa bằng lượng HCl tạo thành, biết:
Ba(OH)2 + 2HCl -> BaCl2 + 2H2O
Bài 4: Trong điều kiện 25oC và 0,22 atm, có 7,77 lít khí O2. Lượng khí Oxi trên có phản ứng đủ với 0,1 mol Fe theo phản ứng: 3Fe + 2O2 -> Fe3O4 không ? (Làm tròn mol khí O2 đến 2 chữ số sau dấu phẩy)
\(Tacó:n=\dfrac{A}{N}\\ Sốnguyêntử:A=0,69.6.10^{23}=4,14.10^{23}\left(nguyêntử\right)\)
Đúng 2
Bình luận (0)
Trong 0,69 mol KMnO4 có số phân tử là:
\(0,69.6.10^{23}=4,14.10^{23}\left(phân.tử\right)\)
Đúng 1
Bình luận (0)
đốt cháy hoàn toàn 23g C2H6O a) Tính khối lượng và thể tích O2 cần dùng ở đktcb) Tính khối lượng và thể tích CO2 tạo thành ở đk thườngc) Tính khối lượng H2O và số phân tử H2O , tính số nguyên tử có trong lượng nướcNẾU CÁC BẠN KHÔNG CÓ THỜI GIAN GIẢI HẾT, THÌ GIẢI GIÚP MÌNH CÂU tính số nguyên tử có trong lượng nước XIN CHÂN THÀNH CẢM ƠN!
Đọc tiếp
đốt cháy hoàn toàn 23g C2H6O
a) Tính khối lượng và thể tích O2 cần dùng ở đktc
b) Tính khối lượng và thể tích CO2 tạo thành ở đk thường
c) Tính khối lượng H2O và số phân tử H2O , tính số nguyên tử có trong lượng nước
NẾU CÁC BẠN KHÔNG CÓ THỜI GIAN GIẢI HẾT, THÌ GIẢI GIÚP MÌNH CÂU ' tính số nguyên tử có trong lượng nước ' XIN CHÂN THÀNH CẢM ƠN!
PTHH: C2H5OH+3O2→2CO2+3H20
0,5 → 1,5 1
a) V CO2(đktc)=1x 22,4=22,4 l
b)V O2(đktc)=1,5. 22,4=33,6 l
c>m H2O=1,5 .18=27 g
nt H2)=1,5.1,6.10-19=2,4.10-19
Đúng 0
Bình luận (0)
tính khối lượng tương đối của phân tử H2O theo 3 cách?
\(C1:\\ KLTĐ_{H2O}=M_{H2O}.1,66.10^{-24}\\ =18.1,66.10^{-24}=29,88.10^{-24}gam\\KLtđ_{H2O}=KLTĐ.6,02.10^{23}=17,98=18gam\\ C2:\\ Kltđ_{H2O}=M_{H2O}=2.1+16.1=18gam\\ C3:\\ KlTĐ_{H2O}\\ =2m_H+m_O=2\left(1.1,6726.10^{-24}+1.9,1.10^{-28}\right)+8.1,675.10^{-24}\\ +8.9,1.10^{-28}=30,1351.10^{-24}gam\\ \Rightarrow Kltđ_{H2O}=30,1351.10^{24}.6,02.10^{23}=18\left(gam\right)\)
Đúng 2
Bình luận (1)
\(mH_2O=MH_2O.nH_2O\)
lấy H2O đi cân
tính theo pthh có H2O
Đúng 0
Bình luận (0)
Bài 1: NaOH + HCl - NaCl + H2O 2H2 + O2 - 2H2OCho khối lượng của NaOH là 4gam. Tính thể tích khí O2 cần dùng để tạo ra lượng H2O bằng lượng H2O trong phản ứng của NaOH với HClBài 3: CH4 + 2Cl2 - CH2Cl2 + 2HCl ( đk: á/s, 1:2 ). Cho thể tích của CH4 là 17,92 lít, của Cl2 là 11200 cm3. Tính thể tích Ba(OH)2 được trung hòa bằng lượng HCl tạo thành, biết: Ba(OH)2 + 2HCl - BaCl2 + 2H2OBài 4: Trong điều kiện 25oC và 0,22 atm, có 7,77 lít khí O2. Lượng khí Oxi trên có phản...
Đọc tiếp
Bài 1: NaOH + HCl -> NaCl + H2O
2H2 + O2 -> 2H2O
Cho khối lượng của NaOH là 4gam. Tính thể tích khí O2 cần dùng để tạo ra lượng H2O bằng lượng H2O trong phản ứng của NaOH với HCl
Bài 3: CH4 + 2Cl2 -> CH2Cl2 + 2HCl ( đk: á/s, 1:2 ). Cho thể tích của CH4 là 17,92 lít, của Cl2 là 11200 cm3. Tính thể tích Ba(OH)2 được trung hòa bằng lượng HCl tạo thành, biết:
Ba(OH)2 + 2HCl -> BaCl2 + 2H2O
Bài 4: Trong điều kiện 25oC và 0,22 atm, có 7,77 lít khí O2. Lượng khí Oxi trên có phản ứng đủ với 0,1 mol Fe theo phản ứng: 3Fe + 2O2 -> Fe3O4 không ? (Làm tròn mol khí O2 đến 2 chữ số sau dấu phẩy)
Hòa tan 7,8 gam K vào H2O hoàn toàn:
a) Viết PTHH
b) Tính V khí (đktc)
c) Khối lượng H2O phản ứng
d) Khối lượng Bazơ thu được
\(n_K=\dfrac{7,8}{39}=0,2\left(mol\right)\\
pthh:2K+2H_2O->2KOH+H_2\)
0,2 0,2 0,2 0,1
=> \(V_{H_2}=0,1.22,4=2,24\left(L\right)\)
\(m_{H_2O}=0,2.18=3,6\left(g\right)\\
m_{KOH}=0,2.56=11,2\left(g\right)\)
Đúng 2
Bình luận (1)
Xem thêm câu trả lời
Tính khối lượng của: a/ 1,8.1023phân tử H2O b/ 6,1975 lit CO2 (đkc)
b: \(n=\dfrac{V}{22.4}=\dfrac{6.1975}{22.4}=0,28\left(mol\right)\)
\(\Leftrightarrow m_{CO_2}=n_{CO_2}\cdot M_{CO_2}=0.28\cdot44=12.32\left(g\right)\)
Đúng 1
Bình luận (0)
Bài 1: Tính khối lượng của 1 mol Cl2, CH4 , CO2 , K2O , Fe2O3, CuSO4, NaOH, Fe(NO3)2 , Fe(OH)2 , K NO3, Tính khối lượng của 0,1 mol CaCO3 ; 0,5 mol H2O ; 0,15 mol CuO.
\(m_{Cl_2}=1.71=71\left(g\right)\)
\(m_{CH_4}=1.16=16\left(g\right)\)
\(m_{CO_2}=1.44=44\left(g\right)\)
\(m_{K_2O}=1.94=94\left(g\right)\)
\(m_{Fe_2O_3}=1.160=160\left(g\right)\)
\(m_{CuSO_4}=1.160=160\left(g\right)\)
\(m_{NaOH}=1.40=40\left(g\right)\)
\(m_{Fe\left(NO_3\right)_2}=1.242=242\left(g\right)\)
\(m_{Fe\left(OH\right)_2}=1.90=90\left(g\right)\)
\(m_{KNO_3}=1.101=101\left(g\right)\)
\(m_{CaCO_3}=0,1.100=10\left(g\right)\)
\(m_{H_2O}=0,5.18=9\left(g\right)\)
\(m_{CuO}=0,15.80=12\left(g\right)\)
Đúng 0
Bình luận (1)