Cho sơ đồ phản ứng : Fe3O4 + HNO3 ® Fe(NO3)3 + NxOy + H2O. Sau khi cân bằng, hệ số của phân tử HNO3 là :
A. 23x – 9y
B. 23x – 8y
C. 46x – 18y
D. 13x – 9y
Cho PTPƯ Fe3O4 + HNO3 -> Fe(NO3)3 + NxOy + H2O.Sau khi cân bằng PTPƯ trên với các chất là số nguyên, tối giản thì hệ số củ HNO3 là? Làm dạng tự luận
A 13x-9y B 46x-18y C 46x-18y D 23x-9y
Giúp e vs
Fe3O4 + HNO3 ---> Fe(NO3)3 + NxOy + H2O
Fe(+8/3) -1e --> 3Fe3+
N+5 + (5x-2y) --> NxOy ( vì hóa trị Oy là -2y => hóa trị Nx là 2y/x)
Từ pt thăng bằng electron bạn thế ngược lên pt pứ: Hay đơn giản 3*(5x -2y)Fe(NO3)3 + NxOy ( vì chỉ cần tìm hệ số của N). Nhân vào hệ số của nitơ ta đc: 45x -18y + x =46x -18y ( là hệ số của HNO3)
Ta được phương trình phản ứng
(5x-2y) Fe3O4 +(46x-18y) HNO3 ->(15x-6y) Fe(NO3)3 + NxOy +(23x-9y) H2O
Vậy chọn B
Cho sơ đồ phản ứng : FeS2 + HNO3 ® Fe(NO3)3 + H2SO4 + NO + H2O
Sau khi cân bằng, tổng hệ số cân bằng của các chất trong phản ứng là:
A. 21
B. 19
C. 23
D. 25
Đáp án B.
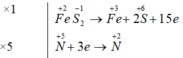
FeS2 + 8HNO3 → Fe(NO3)3 + 2H2SO4 + 5NO + 2H2O
Tổng hệ số cân bằng của các chất trong phản ứng là = 1 + 8+ 1+ 2+ 5 + 2= 19
Cho phản ứng:
FeO + HNO3 → Fe(NO3)3 + NxOy + H2O
Sau khi cân bằng, hệ số của HNO3 là
A. 13x - 9y
B. 23x - 9y
C. 23x - 8y
D. 16x - 6y
Cho sơ đồ phản ứng: F e 3 O 4 + H N O 3 → F e ( N O 3 ) 3 + N O + H 2 O . Sau khi cân bằng, tỉ lệ số phân tử bị oxi hóa và số phân tử bị khử là
A. 28 : 3.
B. 1 : 3.
C. 3 : 1.
D. 3 : 28.
Đáp án C
Số oxi hóa của các nguyên tố thay đổi:
F e + 8 / 3 3 O 4 + H N + 5 O 3 → F e + 3 ( N O 3 ) 3 + N + 2 O + H 2 O
Các quá trình nhường, nhận electron:
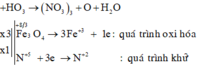
=> Tỉ lệ số phân tử bị oxi hóa : số phân tử bị khử = 3: l
Cho sơ đồ phản ứng: Fe 3 O 4 + HNO 3 → Fe ( NO 3 ) 3 + NO + H 2 O
Sau khi cân bằng, tỉ lệ số phân tử bị oxi hóa và số phân tử bị khử là
A. 28 : 3.
B. 1 : 3.
C. 3 : 1.
D. 3: 28.
Cho sơ đồ phản ứng: Fe3O4 + HNO3 → Fe(NO3)3 + NO + H2O
Sau khi cân bằng, tỉ lệ số phân tử bị oxi hóa và số phân tử bị khử là
A. 28 : 3
B. 1:3
C. 3 :1
D. 3: 28
Đáp án : C
Số phân tử bị oxi hóa là Fe3O4 và phân tử bị khử là HNO3 ( đúng bằng số NO )
3Fe3O4 + 10HNO3 -> 9Fe(NO3)3 + NO + 5H2O
=> oxi hóa : khử = 3 : 1
Cho sơ đồ phản ứng: F e 3 O 4 + H N O 3 → F e ( N O 3 ) 3 + N O + H 2 O Sau khi cân bằng, tỉ lệ giữa số phân tử bị oxi hoá và số phân tử bị khử là :
A. 3:1
B. 28:3
C. 3:28
D. 1:3
Đáp án A.
Ta có các quá trình :
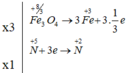
Số phân tử HNO3 đóng vai trò làm chất oxi hóa là 1
![]()
Fe3O4 là chất bị oxi hóa, HNO3 vừa là môi trường vừa là chất bị khử.
Cho sơ đồ phản ứng:
F e 3 O 4 + H N O 3 → F e N O 3 3 + N a O b + H 2 O
Sau khi cân bằng, hệ số của phân tử HNO3 là
A. 23x-9y
B. 23x-8y
C. 46x-18y
D. 13x-9y
Cho phản ứng sau: F e ( O H ) 2 + H N O 3 - > F e ( N O 3 ) 3 + N x O y + H 2 O Sau khi cân bằng, tổng hệ số tối giản của chất tham gia và chất tạo thành sau phản ứng là
A. 39x - l5y + 1
B. 20x – l6y
C. 34x + l5y
D. 39x + l5y
Đáp án A
Số oxi hóa của các nguyên tố thay đổi là:
F e + 2 ( O H ) 2 + H N + 5 O 3 - > F e + 3 ( N O 3 ) 3 + N x + 2 y / x O y + H 2 O
Các quá trình nhường, nhận electron:
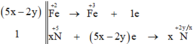
Phương trình cân bằng:
( 5 x - 2 y ) F e ( O H ) 2 + ( 16 x - 6 y ) H N O 3 → ( 5 x - 2 y ) F e ( N O 3 ) 3 + N x O y + ( 13 x - 5 y ) H 2 O
Tổng hệ số tối giản của chất tham gia và chất tạo thành sau phản ứng = (5x - 2y) + (l6x - 6y) + (5x - 2y) + 1 + (13x - 5y) = 39x – l5y + 1