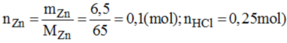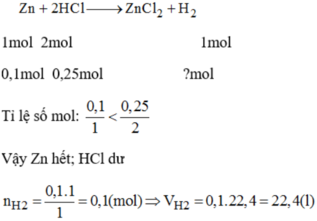Cho 6,5g kẽm vào bình dung dịch chứa 0,25mol axit clohidric. Sau phản ứng còn dư chất nào? Khối lượng là bao nhiêu gam?

Những câu hỏi liên quan
cho 6,5g kẽm vào bình dd chứa 0,25mol HCl
a,tính thể tích khí H (ĐKTC)
b,sau phản ứng chất naò còn dư khối lượng là bao nhiêu
a) \(n_{Zn}=\dfrac{6,5}{65}=0,1\left(mol\right)\)
PTHH: Zn + 2HCl --> ZnCl2 + H2
Xét tỉ lệ: \(\dfrac{0,1}{1}< \dfrac{0,25}{2}\) => Zn hết, HCl dư
PTHH: Zn + 2HCl --> ZnCl2 + H2
0,1--->0,2------------>0,1
=> VH2 = 0,1.22,4 = 2,24 (l)
b) mHCl(dư) = (0,25 - 0,2).36,5 = 1,825 (g)
Đúng 9
Bình luận (0)
cho 6,5 kẽm vào bình dung dịch chứa 0,25 mol axit clohidric .
a/ tính thể tích khí hidro thu được ở đktc
b/ sau phản ứng còn dư chất nào ? khối lượng là bao nhiêu gam
zn+2Hcl→zncl2+h2
a) nZn=6.5/65=0.1(mol)
ta có nZn/1=0.1/1<nHcl/2=0.25/2=0.125
→zn hết ,hcl dư
theo pt:nH2=nZn=0.1 (mol)
Vh2=0.1*22.4=2.24
b) sau pư zn hết ,Hcl dư
theo pt nHcl=2nZn=0.1*2=0.2( mol )
sô mol Hcl dư là:
0.25-0.2=0.05(mol)
mHcl dư là:0.05*36.5=1.825
xong ![]()
Đúng 1
Bình luận (0)
Cho 6.5 gam kẽm vào bình dung dịch chứa 60 gam dung dịch axit clohidric 7.3 %. a) Tính thể tích khí hidro thu đc dktc
b)sau p/ứ còn dư chất nào ? khối lượng dư là bao nhiêu gam ?
Zn + 2HCl \(\rightarrow\) ZnCl2 + H2
nZn = \(\dfrac{6,5}{65}=0,1mol\)
nHCl = \(\dfrac{60.7,3\%}{36,5}=0,12mol\)
Lập tỉ lệ: nZn : nHCl = \(\dfrac{0,1}{1}:\dfrac{0,12}{2}=0,1:0,06\)
=> Zn dư
nZn dư = 0,1 - 0,06 = 0,04 mol
=> mZn dư = 0,04 . 65 = 2,6g
Đúng 1
Bình luận (0)
\(n_{Zn}=\dfrac{6.5}{65}=0.1\left(mol\right)\)
\(n_{HCl}=\dfrac{60\cdot7.3}{100\cdot36.5}=0.12\left(mol\right)\)
\(Zn+2HCl\rightarrow ZnCl_2+H_2\)
\(1...........2\)
\(0.1.........0.12\)
\(LTL:\dfrac{0.1}{1}>\dfrac{0.12}{2}\Rightarrow Zndư\)
\(n_{H_2}=\dfrac{0.12}{2}=0.06\left(mol\right)\)
\(V_{H_2}=0.06\cdot22.4=1.344\left(l\right)\)
\(m_{Zn\left(dư\right)}=\left(0.1-0.06\right)\cdot65=2.6\left(g\right)\)
Đúng 0
Bình luận (0)
Cho 6,5 g kẽm vào bình dung dịch chứa 0,25 mol axit clohiđric.
a/ Tính thể tích khí hiđro thu được ở đktc?
b. Sau phản ứng còn dư chất nào ? khối lượng là bao nhiêu gam?
PTHH: \(Zn+2HCl\rightarrow ZnCl_2+H_2\uparrow\)
Ta có: \(\left\{{}\begin{matrix}n_{Zn}=\dfrac{6,5}{65}=0,1\left(mol\right)\\n_{HCl}=0,25\left(mol\right)\end{matrix}\right.\)
Xét tỉ lệ: \(\dfrac{0,1}{1}< \dfrac{0,25}{2}\) \(\Rightarrow\) HCl còn dư, Kẽm p/ứ hết
\(\Rightarrow\left\{{}\begin{matrix}n_{H_2}=0,1\left(mol\right)\\n_{HCl\left(dư\right)}=0,05\left(mol\right)\end{matrix}\right.\) \(\Rightarrow\left\{{}\begin{matrix}V_{H_2}=22,4\cdot0,1=2,24\left(l\right)\\m_{HCl\left(dư\right)}=0,05\cdot36,5=1,825\left(g\right)\end{matrix}\right.\)
Đúng 3
Bình luận (0)
Cho 6,5 gam Zn vào bình đựng dung dịch chứa 0,25mol axit clohidric HCl
a) Tính thể tích khí Hidro thu được ở đktc
b) Sau phản ứng, chất nào còn dư? Khối lượng là bao nhiêu gam?
P/s : Các bạn giúp mình với, gần thi rồi !!! Cảm ơn các bạn rất nhiều
nZn=0,1 mol
nHCl=0,25 mol
Zn +2HCl=>ZnCl2+H2
Pứ 0,1 mol>=0,2 mol. =>0,1 mol
Dư 0,05 mol
VH2=2,24lit
HCl còn dư:0,05 mol
=>mHCl dư=1,825g
Đúng 0
Bình luận (0)
Cho 13 gam kẽm vào bình chứa dung dịch axit clohidric (HCl) thu được kẽm clorua (ZnCl2) và khí hidro
a) Lập phương trình hóa học
b) Nếu lượng HCl là 21,9 gam thì Zn, HCl chất nào còn dư? Dư bao nhiêu mol?
c) Tính khối lượng ZnCl2 tạo thành, thể tích khí hidro bay ra (ở đktc)
\(a,Zn+2HCl\to ZnCl_2+H_2\\ b,n_{Zn}=\dfrac{13}{65}=0,2(mol);n_{HCl}=\dfrac{21,9}{36,5}=0,6(mol)\)
Vì \(\dfrac{n_{Zn}}{1}<\dfrac{n_{HCl}}{2}\) nên \(HCl\) dư
\(n_{HCl(dư)}=0,6-0,2.2=0,2(mol)\\ c,n_{ZnCl_2}=n_{H_2}=n_{Zn}=0,2(mol)\\ \Rightarrow m_{ZnCl_2}=0,2.136=27,2(g)\\ V_{H_2}=0,2.22,4=4,48(l)\)
Đúng 1
Bình luận (0)
dẫn 10,08l khí h2 vào một ống có chứa 48g fe2o3 và núng nóng tới nhiệt độ thích hợp. a) chất nào còn dư sau phản ứng? dư bao nhiêu gam? b) điều chế lượng hidro trên cần dùng bao nhiêu gam kẽm tác dụng với dung dịch axit clohidric
a)\(n_{H_2}=\dfrac{10,08}{22,4}=0,45\left(m\right)\)
\(n_{Fe_2O_3}=\dfrac{48}{160}=0,3\left(m\right)\)
\(PTHH:Fe_2O_3+3H_2\underrightarrow{ }2Fe+3H_2O\)
ta có tỉ lệ:\(\dfrac{0,45}{3}< \dfrac{0,3}{1}->H_2dư\)
H2 còn lại sau phản ứng
\(n_{H_2\left(dư\right)}=0,3-0,15=0,15\left(m\right)\)
\(m_{H_2\left(dư\right)}=0,15.2=0,3\left(g\right)\)
b)\(PTHH:Zn+2HCl\underrightarrow{ }ZnCl_2+H_2\)
tỉ lệ :1 2 1 1
số mol :0,15 0,3 0,15 0,15
\(m_{Zn}=0,15.65=9,75\left(g\right)\)
Đúng 1
Bình luận (0)
Cho 6,5g kẽm vào bình dung dịch chứa 0,25mol axit clohidric. Tính thể tích khí hidro thu được ở đktc.
cho 3,25 gam kẽm tác dụng với dung dịch loãng chứa 43,8 gam axit clohidric HCL A chất nào còn dư sau phản ứng dư bao nhiêu gam B tính thể tích hidro thu được ở (đktc)
Đọc tiếp
cho 3,25 gam kẽm tác dụng với dung dịch loãng chứa 43,8 gam axit clohidric HCL A chất nào còn dư sau phản ứng dư bao nhiêu gam B tính thể tích hidro thu được ở (đktc)
Pt: \(Zn+2HCl\rightarrow ZnCl_2+H_2\)
\(n_{Zn}=\dfrac{3,25}{65}=0,05mol\)
\(n_{HCl}=\dfrac{43,8}{36,5}=1,2mol\)
Lập tỉ lệ:
nZn : nHCl = \(\dfrac{0,05}{1}:\dfrac{1,2}{2}=0,05:0,6\)
=> HCl dư
nHCl dư = 1,2 - 0,05 = 1,15 mol
mHCl dư = 1,15 . 36,5 = 41,975g
b) Theo pt: nH2 = nZn = 0,05 mol
=> VH2 = 0,05.22,4=1,12lit
đề có sai chỗ 43,8 g HCl ko, số hơi to
Đúng 1
Bình luận (0)
\(a) n_{Zn} = \dfrac{3,25}{65} = 0,05(mol)\ ; n_{HCl} = \dfrac{43,8}{36,5} = 1,2(mol)\\ Zn + 2HCl \to ZnCl_2 + H_2\\ n_{HCl} = 1,2 > 2n_{Zn} = 0,1 \to HCl\ dư\\ n_{HCl\ pư} = 2n_{Zn} = 0,1(mol)\\ \Rightarrow m_{HCl\ dư} = 43,8 - 0,1.36,5 = 40,15(gam)\\ c) n_{H_2} = n_{Zn} = 0,05(mol) \Rightarrow V_{H_2} = 0,05.22,4 = 1,12(lít)\)
Đúng 0
Bình luận (0)