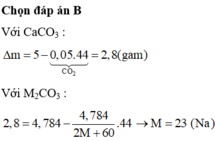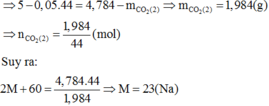Hai cốc đựng dung dịch HCl đặt trên hai đĩa cân X, Y cân ở trạng thái cân bằng. Cho 5 gam CaCO3 vào cốc X và 4,784 gam M2CO3 (M là kim loại kiềm) vào cốc Y. Sau khi hai muối đã tan hoàn toàn, cân trở lại vị trí thăng bằng. Kim loại M là:
A. K
B. Cs
C. Li
D. Na