Thể tích dung dịch Ca(OH)2 0,01M tối thiểu để hấp thụ hết 0,02mol khí CO2 là
A. 1,0 lít
B. 1,5 lít
C. 2,0 lít
D. 2,5 lít
a, \(C_2H_4+Br_2\rightarrow C_2H_4Br_2\)
\(C_2H_2+2Br_2\rightarrow C_2H_2Br_4\)
b, \(n_{C_2H_4}+n_{C_2H_2}=\dfrac{0,56}{22,4}=0,025\left(mol\right)\left(1\right)\)
Theo PT: \(n_{Br_2}=n_{C_2H_4}+2n_{C_2H_2}=\dfrac{2,8}{160}=0,0175\left(mol\right)\left(2\right)\)
Từ (1) và (2) \(\Rightarrow\left\{{}\begin{matrix}n_{C_2H_4}=0,0325\left(mol\right)\\n_{C_2H_2}=-0,0075\end{matrix}\right.\)
Đến đây thì ra số mol âm, bạn xem lại đề nhé.
Cho V lít khí CO2 (đktc) hấp thụ hoàn toàn vào 3 lít dung dịch Ca(OH)2 0,01M thu được 1,5 gam kết tủa. Giá trị của V là
A. 0,336.
B. 2,016.
C. 0,336 hoặc 2,016.
D. 0,336 hoặc 1,008.
Cho V lít khí CO2 (đktc) hấp thụ hết vào 500ml dung dịch Ca(OH)2 0,02M thì thu được 0,5 gam kết tủa. Giá trị tối thiểu của V là
A. 0,336
B. 0,112
C. 0,224
D. 0,448
Đáp án B
Ta có: nCa(OH)2= 0,5.0,02= 0,01 mol;
nCaCO3= 0,5/100= 0,005 mol
Ta có: nCa(OH)2 > nCaCO3 và đề hỏi giá trị tối thiểu của V nên khi đó Ca(OH)2 dư
CO2 + Ca(OH)2 → CaCO3 ↓ + H2O
Theo PT: nCO2= nCaCO3= 0,005 mol
→ VCO2= 0,005.22,4= 0,112 lít
Thể tích dd NaOH 2M tối thiểu để hấp thụ hết 5,6 lít khí CO2 (đktc) là
A. 500 ml
B. 175 ml
C. 125 ml.
D. 250 ml.
Tối thiểu => ti lệ 1:1 => V = 0,25:2 = 125 ml => Đap an C
Thể tích dung dịch NaOH 2M tối thiểu đề hấp thụ hết 5,6 lít khí SO2 (đktc) là
A. 125ml.
B. 215ml.
C. 500ml.
D. 250ml.
Đáp án A
Số mol SO2 là: n SO 2 = 0 , 25 mol
Lượng NaOH tối thiểu để hấp thụ khí SO2 chính là lượng NaOH phản ứng với SO2 để tạo muối axit:

Thể tích dd KOH 0,5M tối thiểu để hấp thụ hết 1,4 lít khí H2S(đkc) là A. 250ml B. 500ml C. 125ml D. 175ml
\(n_{H_2S}=\dfrac{1,4}{22,4}=0,0625\left(mol\right)\)
PTHH: KOH + H2S ---> KHS + H2O
0,0625 0,0625
\(\rightarrow V_{ddKOH}=\dfrac{0,0625}{0,5}=0,125\left(l\right)=125\left(ml\right)\)
Chọn C
Hấp thụ hết V lít khí CO 2 vào dung dịch chứa 0,42 mol Ca ( OH ) 2 , thu được a gam kết tủa. Tách lấy kết tủa, sau đó thêm tiếp 0,6V lít khí CO 2 nữa, thu thêm 0,2a gam kết tủa. Thể tích các khí đo ở đktc. Giá trị của V là:
A. 7,84 lít
B. 5,60 lít
C. 6,72 lít
D. 8,40 lít
Đáp án C
Theo giả thiết, suy ra : Khi cho V lít CO 2 vào dung dịch chứa 0,42 mol Ca ( OH ) 2 thì chưa có hiện tượng hòa tan kết tủa. Sau khi lọc bỏ kết tủa thêm tiếp 0,6V lít CO 2 vào thì đã có hiện tượng hòa tan một phần kết tủa (nếu không có hiện tượng hòa tan kết tủa thì lượng kết tủa thu được phải là 0,6a gam).
Xét toàn bộ quá trình phản ứng, ta có :
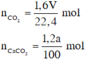
Kết quả thí nghiệm được biểu diễn bằng đồ thị sau :
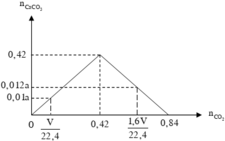
Từ đồ thị, suy ra :
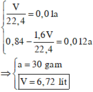
Cho V lít khí CO2 (đktc) hấp thụ hoàn toàn vào 4 lít dung dịch Ba(OH)2 0,01M thu được 2,955 gam kết tủa. Giá trị của V là
A. 0,336.
B. 0,672.
C. 0,336 hoặc 1,456.
D. 0,672 hoặc 2,912
Hấp thụ hết V lít CO2 (đktc) vào dung dịch chứa 500 ml dung dịch Ca(OH)2 0,01M, thu được 2 gam kết tủa. Tính giá trị của V.
Sửa đề : 500 ml dung dịch Ca(OH)2 0,1M . Nếu là 0,01M thì đề sai
\(n_{Ca\left(OH\right)_2}=0,5.0,1=0,05\left(mol\right)\)
\(n_{CaCO_3}=\dfrac{2}{100}=0,02\left(mol\right)\)
Bảo toàn nguyên tố Ca : \(n_{Ca\left(OH\right)_2}=n_{CaCO_3}+n_{Ca\left(HCO_3\right)_2}\)
=> \(n_{Ca\left(HCO_3\right)_2}=0,05-0,02=0,03\left(mol\right)\)
Bảo toàn nguyên tố C :
=> \(n_{CO_2}=n_{CaCO_3}+2n_{Ca\left(HCO_3\right)_2}=0,02+0,03.2=0,08\left(mol\right)\)
=> \(V_{CO_2}=0,08.22,4=1,792\left(l\right)\)