Khi cho thanh kẽm vào dung dịch FeSO4 thì khối lượng dung dịch sau phản ứng so với ban đầu sẽ
A. giảm
B. không đổi
C. tăng
D. ban đầu tăng sau đó giảm xuống
Nhúng một thanh kẽm vào dung dịch chứa 8,5 gam AgNO3. Sau phản ứng thấy khối lượng thanh kẽm tăng lên 8% so với khối lượng ban đầu. Xác định khối lượng thanh kẽm ban đầu?
PT: \(Zn+2AgNO_3\rightarrow Zn\left(NO_3\right)_2+2Ag\)
Ta có: \(n_{AgNO_3}=\dfrac{8,5}{170}=0,05\left(mol\right)\)
Theo PT: \(n_{Zn\left(pư\right)}=\dfrac{1}{2}n_{AgNO_3}=0,025\left(mol\right)\)
\(n_{Ag}=n_{AgNO_3}=0,05\left(mol\right)\)
Có: m tăng = mAg - mZn (pư) = 0,05.108 - 0,025.65 = 3,775 (g)
Mà: m tăng = 8%mZn ban đầu
⇒ m Zn ban đầu = 47,1875 (g)
Cho 6g kẽm hạt vào một cốc đựng dung dịch H2SO4 4M (dư) ở nhiệt độ thường.
Nếu giữ nguyên các điều kiện khác, chỉ biến đổi một trong các điều kiện sau đây thì tốc độ phản ứng biến đổi như thế nào (tăng lên, giảm xuống hay không đổi)?
a) Thay 6g kẽm hạt bằng 6g kẽm bột.
b) Thay dung dịch H2SO4 4M bằng dung dịch H2SO4 2M.
c) Thực hiện phản ứng ở nhiệt độ phản ứng là 50oC.
d) Dùng thể tích dung dịch H2SO4 4M lên gấp đôi ban đầu.
a) Tốc độ phản ứng tăng lên (tăng diện tích bề mặt).
b) Tốc độ phản ứng giảm xuống (giảm nồng độ chất phản ứng).
c) Tốc độ phản ứng tăng.
d) Tốc độ phản ứng không thay đổi.
Nhúng thanh Zn vào dung dịch muối X, sau khi kết thúc phản ứng thu được dung dịch có khối lượng giảm so với dung dịch ban đầu. X là
A. Ni(NO3)2
B. AgNO3
C. Fe(NO3)3
D. Cu(NO3)2
Ngâm một lá Zn trong 100ml dung dịch AgNO3 0,1M, sau đó lấy thanh Zn ra rồi cho tiếp dung dịch HCl vào dung dịch vừa thu được thì không thấy hiện tượng gì. Hỏi khối lượng lá Zn tăng hay giảm bao nhiêu gam so với ban đầu:
A. Tăng 0,755g.
B. Giảm 0,567g.
C. Tăng 2,16g.
D. Tăng 1,08g.
Đáp án A
Vì khi cho HCl vào dung dịch vừa thu được không thấy hiện tượng gì nên trong dung dịch không còn Ag+
![]()
Do đó Ag+ đã phản ứng hết với Zn.
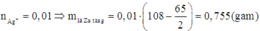
Nhúng thanh Zn vào dung dịch muối X, sau khi kết thúc phản ứng thu được dung dịch có khối lượng giảm so với dung dịch ban đầu. Muối X là muối nào sau đây?
A. Ni(NO3)2.
B. AgNO3.
C. Fe(NO3)3.
D. Cu(NO3)2.
Giả sử có 1 mol Zn phản ứng:
A. Zn + Ni(NO3)2 → Zn(NO3)2 + Ni ⇒ mZn(NO3)2 > mNi(NO3)2 ⇒ mdung dịch tăng
B. Zn + 2AgNO3 → Zn(NO3)2 + 2Ag ⇒ mZn(NO3)2 < mAgNO3 ⇒ mdung dịch giảm
C. 3Zn + 2Fe(NO3)3 → 3Zn(NO3)2 + 2Fe ⇒ mZn(NO3)2 > mFe(NO3)3 ⇒ mdung dịch tăng
D. Zn + Cu(NO3)2 → Zn(NO3)2 + Cu ⇒ mZn(NO3)2 > mCu(NO3)2 ⇒ mdung dịch tăng
Chọn đáp án B
Nhúng thanh Zn vào dung dịch muối X, sau khi kết thúc phản ứng thu được dung dịch có khối lượng giảm so với dung dịch ban đầu. Muối X là muối nào sau đây?
A. Ni(NO3)2.
B. AgNO3.
C. Fe(NO3)3.
D. Cu(NO3)2.
Chọn đáp án B
Giả sử có 1 mol Zn phản ứng:
A. Zn + Ni(NO3)2 → Zn(NO3)2 + Ni ⇒ mZn(NO3)2 > mNi(NO3)2 ⇒ mdung dịch tăng
B. Zn + 2AgNO3 → Zn(NO3)2 + 2Ag ⇒ mZn(NO3)2 < mAgNO3 ⇒ mdung dịch giảm
C. 3Zn + 2Fe(NO3)3 → 3Zn(NO3)2 + 2Fe ⇒ mZn(NO3)2 > mFe(NO3)3 ⇒ mdung dịch tăng
D. Zn + Cu(NO3)2 → Zn(NO3)2 + Cu ⇒ mZn(NO3)2 > mCu(NO3)2 ⇒ mdung dịch tăng
⇒ chọn C.
Nhúng thanh Zn vào dung dịch muối X, sau khi kết thúc phản ứng thu được dung dịch có khối lượng giảm so với dung dịch ban đầu. Muối X là muối nào sau đây?
A. Ni(NO3)2.
B. AgNO3.
C. Fe(NO3)3.
D. Cu(NO3)2.
Chọn đáp án B
Giả sử có 1 mol Zn phản ứng:
A. Zn + Ni(NO3)2 → Zn(NO3)2 + Ni ⇒ mZn(NO3)2 > mNi(NO3)2 ⇒ mdung dịch tăng
B. Zn + 2AgNO3 → Zn(NO3)2 + 2Ag ⇒ mZn(NO3)2 < mAgNO3 ⇒ mdung dịch giảm
C. 3Zn + 2Fe(NO3)3 → 3Zn(NO3)2 + 2Fe ⇒ mZn(NO3)2 > mFe(NO3)3 ⇒ mdung dịch tăng
D. Zn + Cu(NO3)2 → Zn(NO3)2 + Cu ⇒ mZn(NO3)2 > mCu(NO3)2 ⇒ mdung dịch tăng
Nhúng thanh Fe vào dung dịch CuSO4. Sau một thời gian, khối lượng dung dịch giảm 0,8 gam so với khối lượng dung dịch ban đầu. Khối lượng Fe đã phản ứng là
A. 6,4 gam.
B. 11,2 gam.
C. 5,6 gam.
D. 8,4 gam.
Fe + Cu2+ → Fe2+ + Cu
PT 1 1 mol → m dung dịch giảm = 64 – 56 = 8 gam
ĐB 0,1 ← 0,8 gam
mFe = 5,6 gam
Đáp án C
Nhúng thanh Fe vào dung dịch CuSO4. Sau một thời gian, khối lượng dung dịch giảm 0,8 gam so với khối lượng dung dịch ban đầu. Khối lượng Fe đã phản ứng là
A. 6,4 gam
B. 11,2 gam
C. 5,6 gam
D. 8,4 gam