Cho thanh kim loại A (hóa trị 2) vào dung dịch C u N O 3 2 thì sau phản ứng khối lượng thanh giảm 0,2%. Cũng thanh kim loại trên nếu cho vào dung dịch P b N O 3 2 thì khối lượng lại tăng 28,4%. Xác định kim loại A.
A. Zn
B. Fe
C. Cu
D. Mg
Cho 12,8 gam kim loại A hóa trị II phản ứng hoàn toàn với khí Cl2 thu muối B. Hòa tan B vào nước thu được 400ml dung dịch C. Nhúng thanh sắt nặng 11,2 gam vào dung dịch C, sau một thời gian thấy kim loại A bám vào thanh sắt và khối lượng thanh sắt là 12,0 gam, nồng độ FeCl2 trong dung dịch là 0,25M. Xác định kim loại A và nồng độ mol của kim loại B trong dung dịch C.
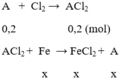
số mol FeCl2 là n = 0,25 . 0,4 = 0,1 (mol)
gọi x là số mol Fe phản ứng
khối lượng kim loại tăng là Δm = mA - mFe = Ax – 56x = 0,8
x = 0,1 → A.0,1 – 56.0,1 = 0,8 → A = 64. A là Cu
số mol Cu là nCu = 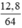 = 0,2 (mol)
= 0,2 (mol)
số mol CuCl2 → n(CuCl2) = nCu = 0,2 (mol)
nồng độ mol/l CuCl2 là C(M(CuCl2)) = 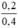 = 0,5M
= 0,5M
Cho 12,8 gam kim loại A hóa trị II phản ứng hoàn toàn với khí Cl2 thu muối B. Hòa tan B vào nước thu được 400ml dung dịch C. Nhúng thanh sắt nặng 11,2 gam vào dung dịch C, sau một thời gian thấy kim loại A bám vào thanh sắt và khối lượng thanh sắt là 12,0 gam, nồng độ FeCl2 trong dung dịch là 0,25M. Xác định kim loại A và nồng độ mol của kim loại B trong dung dịch C.
Nhúng 1 thanh kim loại M hóa trị II vào 1 lít dung dịch AgNO3 0,5M. Kết thúc thí nghiệm thấy khối lượng thanh kim loại tăng 19,2g và nồng độ dung dịch AgNO3 còn 0,3M.
a) Xác định kim loại M?
b) Cho thanh kim loại M nặng 20g vào 200ml dung dịch CuSO4 0,5M sau phản ứng khối lượng thanh kim loại là 20,8g. Tính CM các muối có trong dung dịch sau phản ứng giả sử toàn bộ Cu sinh ra đều bám vào thanh kim loại M và thể tích dung dịch coi như không đổi.
a)
$n_{AgNO_3\ pư} = 1.(0,5 - 0,3) = 0,2(mol)$
M + 2AgNO3 → M(NO3)2 + 2Ag
0,1.......0,2............................0,2.......(mol)
Suy ra : $0,2.108 - 0,1M = 19,2 \Rightarrow M = 24(Mg)$
Vậy M là kim loại Magie
b)
Mg + CuSO4 → MgSO4 + Cu
a............a...............a..........a............(mol)
Suy ra : $20 -24a + 64a = 20,8 \Rightarrow a = 0,02(mol)$
Vậy :
$C_{M_{MgSO_4}} = \dfrac{0,02}{0,2} = 0,1M$
$C_{M_{CuSO_4\ dư}} = \dfrac{0,2.0,5 - 0,02}{0,2} = 0,4M$
nhúng thanh kim loại R( hóa trị II) vào dung dịch CuSO4 sau một thời gian lấy thanh kim loại ra thấy khối lượng thanh kim loại giảm 0,05%.Mặt khác nếu lấy thanh kim loại nhúng vào dung dịch Pb(NO3)2 sau một thời gian lấy ra khối lượng thanh kim loại tăng 7,1%.Biết số mol của Cu(NO3)2 và Pb(NO3)2 tham gia phản ứng ở trên là như nhau.Xác định kim loại R
Giả sử thanh kim loại ban đầu nặng m (g)
Gọi số mol Cu(NO3)2, Pb(NO3)2 pư là a (mol)
TN1:
PTHH: R + Cu(NO3)2 --> R(NO3)2 + Cu
a<-------a------------------>a
=> mgiảm = a.MR - 64a (g)
Và \(m_{giảm}=\dfrac{0,05m}{100}=0,0005m\left(g\right)\)
=> \(a.M_R-64a=0,0005m\) (1)
TN2:
PTHH: R + Pb(NO3)2 --> R(NO3)2 + Pb
a<-------a------------------->a
=> mtăng = 207a - a.MR (g)
Và \(m_{tăng}=\dfrac{7,1.m}{100}=0,071m\left(g\right)\)
=> \(207a-a.M_R=0,071m\) (2)
(1)(2) => \(\dfrac{M_R-64}{207-M_R}=\dfrac{0,0005}{0,071}\)
=> MR = 65 (g/mol)
=> R là Zn
Câu 1 Nhúng một thanh nhôm nặng 45 gam vào 400 ml dung dịch CuSO4 0,5 M sau một thời gian lấy thanh nhôm ra cân nặng 46,38 g . khối lượng Cu thoát ra là
Câu 2;Ngâm một vật bằng Cu có khối lượng 15 gam trong 340 gam dung dịch AgNO3 6% sau một thời gian lấy vật ra thấy khối lượng AgNO3 trong dung dịch giảm 25% khối lượng của vật sau phản ứng là
Câu 3;Nhúng một thanh kim loại hóa trị II vào dung dịch CuSO4 dư sau phản ứng khối lượng thanh kim loại giảm 0,24 gam cũng tan kim loại đó nếu nhúng vào dung dịch AgNO3 dư thì khi phản ứng xong khối lượng thanh kim loại tăng 0,52 gam kim loại hóa trị II là
Câu 4;Nhúng thanh kẽm vào dung dịch chứa 8,32 gam CdSO4 sau khử hoàn toàn ion CD2+ khối lượng thanh kẽm tăng 2,35% với ban đầu Hỏi khối lượng thanh kẽm ban đầu là
Bài 1
2Al+3CuSO4→Al2(SO4)3+3Cu
a-------------------------------------1,5a
Đặt a là số mol của Al pư
Độ tăng của thanh Al sau khi lấy thanh ra khỏi dd:
46,38−45=1,38(g)
⇒96a−27a=69a=1,38
⇒a=0,02⇒a=0,02
⇒mCu=1,92(g)
Câu 1:
2Al + 3Cu2+ --> 2Al3+ + 3Cu
x............1,5x.........................1,5x
m sau – m trước = 64 . 1,5x – 27x = 46,38 – 45
=> x = 0,02 => m Cu phản ứng = 1,5 . 0,02 . 64 = 1,92g
Câu 2:
mAgNO3 = 340 . 6% = 20,4g => nAgNO3 = 0,12mol
Khối lượng AgNO3 giảm 25% chính là lượng AgNO3 phản ứng
=> nAgNO3 phản ứng = 0,12 . 25% = 0,03
Cu + 2AgNO3 ---> Cu(NO3)2 + 2Ag
0,015..........0,03.....................................0,03
m vật = 15 + (0,03.108 - 0,015.64) = 17,28 (g)
Nhúng 1 thanh kim loại M hóa trị II vào 200ml dung dịch CuSO4 0,4M, sau khi phản ứng xong khối lượng thanh kim loại tăng 0,4g và nồng độ CuSO4 còn là 0,15M.
a) xác định kim loại M?
b) Cho 4,48g bột kim loại M vào 250ml dung dịch AgNO3 0,2M; Cu(NO3)2 0,4M. Khuấy đều cho phản ứng hoàn toàn thu m gam chất rắn A và dung dịch B. Tính:
- m?
- CM các chất có trong dung dịch B (coi thể tích dung dịch không đổi)
a)
$n_{CuSO_4\ pư} = 0,2.0,4 - 0,2.0,15 = 0,05(mol)$
$M + CuSO_4 \to MSO_4 + Cu$
Theo PTHH :
$n_{M} = n_{Cu} = n_{CuSO_4} = 0,05(mol)$
Suy ra :
$(64 - M).0,05= 0,4 \Rightarrow M = 56(Fe)$
Vậy M là Fe
b) $n_{Fe} = 0,08(mol) ; n_{AgNO_3} = 0,05(mol) ; n_{Cu(NO_3)_2} = 0,1(mol)$
Fe + 2AgNO3 → Fe(NO3)2 + 2Ag
0,025...0,05...........0,025........0,05........(mol)
Fe + Cu(NO3)2 → Fe(NO3)2 + Cu
0,055...0,055...........0,055.......0,055...........(mol)
Suy ra :
$m = 0,05.108 + 0,055.64 = 8,92(gam)$
$C_{M_{Fe(NO_3)_2}} = \dfrac{0,08}{0,25} = 0,32M$
$C_{M_{Cu(NO_3)_2\ dư}} = \dfrac{0,1 - 0,055}{0,25} =0,18M$
Nhúng thanh kim loại R hóa trị II vào dung dịch CuSO4. Sau một thời gian lấy thanh kim loại ra thấy khối lượng giảm 0,05%. Mặt khác nhúng thanh kim loại này vào dung dịch Pb(NO3)2, sau một thời gian thấy khối lượng thanh tăng 7,1%. Biết rằng số mol R tham gia hai phản ứng là như nhau. R là?
1. Hòa tan hoàn toàn 6 gam kim loại hóa trị II vào m gam H2O thu được (m+5.7) gam dung dịch A. Xác định kim loại X.
2. Hòa tan hoàn toàn 1 kim loại X hóa trị II bằng dung dịch HCl 14.6% vừa đủ thu được 1 dung dịch muối có nồng độ phần trăm là 24.15 % . Xác định tên kim loại.
1/ PT : X + 2H2O -> X[OH]2 + H2
mol : \(\frac{6}{M_X}\) -> \(\frac{6}{M_X}\)
=> mH2 = \(\frac{12}{M_X}\) => mdd = m+6 - \(\frac{12}{M_X}\)
Ta có: m+5,7 = m+6 - \(\frac{12}{M_X}\)
<=> \(\frac{12}{M_X}\)= 0,3 => MX = 40 => X là Canxi [Ca]
2/ Dặt nHCl= a [a> 0] => mddHCl= 36,5a : 14,6 x 100= 250a
PT : X + 2HCL => XCl2 + H2
mol : a/2 a -> a/2 a/2
mH2 = a/2 x 2 = a ; mX = a/2 . MX
m XCl2= a/2 x [MX +71]
mdd XCL2= a/2 .MX + 250a - a = a/2 .MX +249a
Ta có :\(\frac{\frac{a}{2}\times M_X+\frac{71}{2}a}{M_X\times a:2+249a}\times100\%=24,15\%\)
<=> \(\frac{M_X+71}{M_X+498}=24,15\%\Leftrightarrow M_X=65\)=> X là kẽm [Zn]
Hai thanh kim loại X cùng chất, đều có khối lượng là a gam. Thanh thứ nhất nhúng vào l00ml dung dịch AgNO3; thanh thứ 2 nhúng vào 1,5 lít dung dịch Cu(NO3)2. Sau 1 thời gian lấy 2 thanh kim loại ta thấy thanh thứ nhất tăng khối lượng, thanh thứ hai giảm khối lượng nhưng tổng khối lượng 2 thanh vẫn là 2a gam, đồng thời trong dung dịch thấy nồng độ mol của muối kim loại X trong dung dịch Cu(NO3)2 gấp 10 lần trong dung dịch AgNO3. Kim loại X là gì? (biết X có hóa trị II).
A. Cd
B. Fe
C. Zn
D. Pb
Đáp án C
Tổng khối lượng 2 thanh kim loại sau phản ứng vẫn là 2a gam
=> mthanh 1 tăng = mthanh 2 tăng
Đặt số mol kim loại phản ứng với AgNO3 và Cu(NO3)2 lần lượt là x, y
=> 108 . 2 x - M X . x = M X . y - 64 y ( 1 )
Nồng độ mol của muối kim loại X trong dung dịch Cu(NO3)2 gấp 10 lần trong dung dịch AgNO3.
⇒ y 1 , 5 = 10 . x 0 , 1 ⇒ y = 150 x thay vào (1) được:
108 . 2 x - M X . x = M X . 150 x - 64 . 150 x ⇒ M X = 65 => X là Zn.