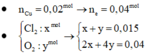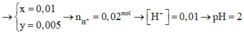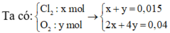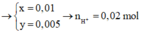Khi điện phân dung dịch NaCl thu được 250g dung dịch NaOH 12%. Tính thể tích khí C l 2 (ở đktc) thu được (Na=23, O=16, H=1).

Những câu hỏi liên quan
Cho 10g CaCO3 tác dụng với dung dịch HCL dư. a,Tính thể tích khí CO2 thu được ở đktc. b,Dẫn khí CO2 thu được vào lọ đựng 25g dung dịch NaOH 40%. Tính khối lượng muối cacbonnat thu được. (biết Ca=40, C=12, O=16, H=1, Na=23, Cl=35,5)
a) CaCO3+2HCl=>CaCl2+H2O+CO2
n CaCO3=10/100 = 0,1 mol
theo phương trình : n CO2 = n CaCO3 = 0,1 mol
=> V CO2 = 0,1*22,4 = 2,24 lít
b) CO2+2NaOH => Na2CO3+H2O
có thể xảy ra phản ứng :
Na2CO3+CO2+H2O=>2NaHCO3
m NaOH = 25*0,4 = 10 gam
=> n NaOH = 10/40 = 0,25 mol
mà nếu theo phương trình đầu tiên của câu b:
n CO2 = 1/2 n NaOH = 1/2*0,25 = 0,125 mol
mà thực tế n CO2 có 0,1 mol
=> n CO2 hết, n NaOH dư
=> chỉ tạo ra 1 muối là Na2CO3
n Na2CO3 = n CO2 = 0,1 mol
=> m Na2CO3 = 0,1*106=10,6 gam
Đúng 1
Bình luận (0)
Cho 14 gam sắt tác dụng với dung dịch HCl, sau phản ứng thu được khí hidro và FeCl2 .
a) Viết PTHH.
b) Tính khối lượng HCl cần dùng.
c)Tính thể tích khí thu được(đktc)
(Cho biết nguyên tử khối: H=1, O=16, C=12, Na =23, Fe=56, Cl=35,5, S =32, Al=27, Zn= 65)
Mình cần gấp ạ^^
nFe = \(\dfrac{14}{56}\) = 0,25 (mol)
a) Fe + 2HCl → FeCl2 + H2
b) Theo phương trình phản ứng, ta có
nFe = 2nHCl = 2.0,25 = 0,5 (mol)
=> mHCl = 0,5.36,5= 18,25 (mol)
c) Theo phương trình phản ứng, ta có:
nFe = nH2 = 0,25 (mol)
=> VH2= 0,25.22,4 = 5,6 (lít)
Đúng 0
Bình luận (0)
Hấp thụ hoàn toàn 4,48 lít khí SO2 (ở đktc) vào dung dịch chứa 16 gam NaOH thu được dung dịch X. Khối lượng muối tan thu được trong dung dịch X là (Cho H = 1, O = 16, Na = 23, S = 32) ?
nSO2=0.2mol
nNaOH=0.4mol
k=nNaOH/nSO2=0.4/0.2=2
k=2, => pứ tạo 1 muối trung hòa.
PT:
SO2+2NaOH-->Na2SO3+H2O
0.2----0.4------->0.2
mNa2SO3=126.0.2=25.2g.
Đúng 0
Bình luận (0)
Điện phân 2 lít dung dịch hỗn hợp gồm NaCl và
CuSO
4
đến khi
H
2
O
bị điện phân ở hai điện cực thì dừng lại, tại catot thu được 1,28 gam kim loại và tại anot thu 0,336 lít khí (đktc). Coi thể tích dung dịch không đổi thì pH của dung dịch thu được là : A. 3 B. 2 C. 12 D. 13.
Đọc tiếp
Điện phân 2 lít dung dịch hỗn hợp gồm NaCl và CuSO 4 đến khi H 2 O bị điện phân ở hai điện cực thì dừng lại, tại catot thu được 1,28 gam kim loại và tại anot thu 0,336 lít khí (đktc). Coi thể tích dung dịch không đổi thì pH của dung dịch thu được là :
A. 3
B. 2
C. 12
D. 13.
Dẫn V lít khí CO2 qua dung dịch NaOH, phản ứng xảy ra vừa đủ. Sau phản ứng chỉ thu được muối natri hidrocacbonat với khối lượng là 33,6g. Tìm thể tích khí CO2 (dktc) đã dùng. (Na = 23; H = 1; C = 12; O = 16).
nNaHCO3 = 0,4 (mol)
BTNT C, có: nCO2 = nNaHCO3 = 0,4 (mol)
⇒ VCO2 = 0,4.22,4 = 8,96 (l)
Đúng 1
Bình luận (0)
Tính thể tích khí (đktc) thu được khi điện phân hết 0,1 mol NaCl trong dung dịch với điện cực trơ, màng ngăn xốp
A. 0,024 lít
B. 1,120 lít
C. 2,240 lít
D. 4,48 lít
Điện phân 2 lít dung dịch hỗn hợp gồm NaCl và CuSO4 đến khi H2O bị điện phân ở hai cực thì dừng lại, tại catốt thu 1,28 gam kim loại và anôt thu 0,336 lít khí (ở đktc)
Xem thể tích dung dich không đổi thì pH của dung dịch thu được là
A. 2,3
B. 2
C. 12
D. 3
Đáp án đúng là B
tham khảo bài làm tại đây nhé ^^ https://wapbug.tk/threads/%C4%90i%E1%BB%87n-ph%C3%A2n-2-l%C3%ADt-dung-d%E1%BB%8Bch-h%E1%BB%97n-h%E1%BB%A3p-g%E1%BB%93m-nacl-v%C3%A0-cuso4-%C4%91%E1%BA%BFn-khi-h2o-b%E1%BB%8B-%C4%91i%E1%BB%87n-ph%C3%A2n-%E1%BB%9F-hai-c%E1%BB%B1c-th%C3%AC-d%E1%BB%ABng-l%E1%BA%A1i.18/
Đúng 0
Bình luận (0)
Điện phân 2 lít dung dịch chứa hỗn hợp gồm NaCl và CuSO4 với điện cực trơ, có màng ngăn đến khi H2O bắt đầu điện phân ở cả hai cực thì dừng lại. Ở catot thu được 1,28 gam kim loại, đồng thời ở anot thu được 0,336 lít khí (đktc). Coi thể tích dung dịch không đổi, pH của dung dịch sau điện phân có giá trị là A. 12. B. 2. C. 13. D. 1.
Đọc tiếp
Điện phân 2 lít dung dịch chứa hỗn hợp gồm NaCl và CuSO4 với điện cực trơ, có màng ngăn đến khi H2O bắt đầu điện phân ở cả hai cực thì dừng lại. Ở catot thu được 1,28 gam kim loại, đồng thời ở anot thu được 0,336 lít khí (đktc). Coi thể tích dung dịch không đổi, pH của dung dịch sau điện phân có giá trị là
A. 12.
B. 2.
C. 13.
D. 1.
Điện phân 2 lít dung dịch chứa hỗn hợp gồm NaCl và CuSO4 với điện cực trơ, có màng ngăn đến khi H2O bắt đầu điện phân ở cả hai cực thì dừng lại. Ở catot thu được 1,28 gam kim loại, đồng thời ở anot thu được 0,336 lít khí (đktc). Coi thể tích dung dịch không đổi, pH của dung dịch sau điện phân có giá trị là
A. 12
B. 2
C. 13
D. 1