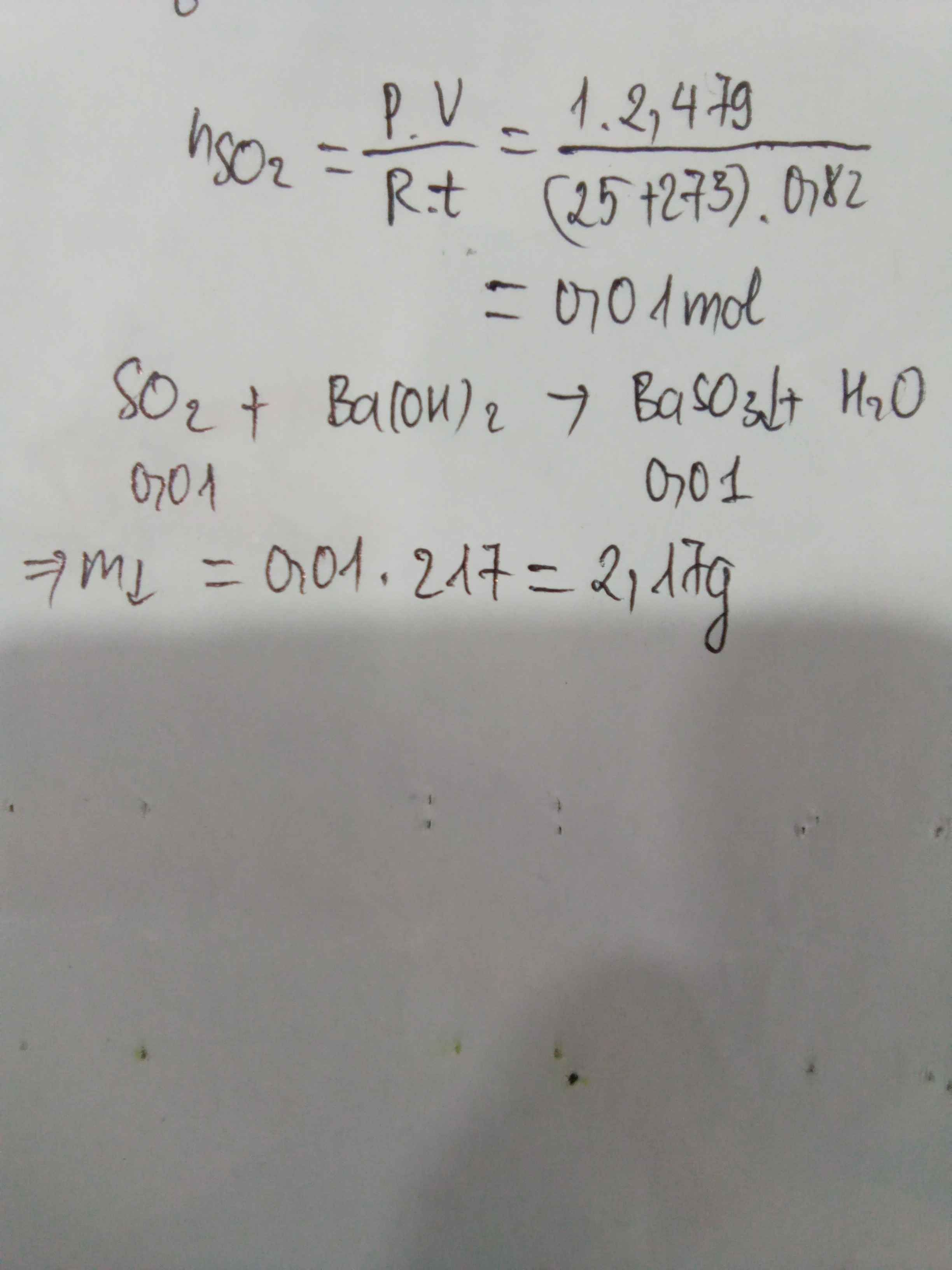Cho 2,479 lít SO2 (đkc :25OC, 1 Bar) tác dụng với dung dịch Ba(OH)2 dư (Ba=137,S=32,O=16). Hãy tính khối lượng chất kết tủa thu được ?

Những câu hỏi liên quan
cho 2,479 lít SO2 ( đkc : 25 độ C , 1 Bar ) tác dụng với dd Ba(OH)2 dư . Hãy tính khối lượng chất kết tủa thu được ?
Cho 1 lượng vừa đủ khí SO2 tác dụng với 200ml dung dịch Ba(oh)2 2M thu được kết tủa và nước A) Tính khối lượng chất kết tủa thu được B) Tính thể tích khí SO2 phản ứng ở điều kiện chuẩn (H:1 S:32 Ba:137 O:16) Làm ơn giúp mình nhé! Cảm ơn rất nhiều
n Ba(OH)2 = 2.0,2=0,4 mol
\(Ba\left(OH\right)_2+SO_2->BaSO_3+H_2O\)
0,4 ................0,4...........0,4
m BaSO3 = 0,4. ( 138+32+16.3)=87,2 g
v SO2 = 0,4.22,4=8,96 lít
Đúng 0
Bình luận (1)
Biết 2,479 lít khí CO2 (ở 25 °C, 1 bar) tác dụng vừa hết với 200ml dung dịch Ba(OH)2, sản phẩm là BaCO3 và H2O
a) Viết phương trình hóa học.
b) tính nồng độ mol của dung dịch Ba(OH)2 đã dùng.
c) tính khối lượng chất kết tủa thu được.
Cho 6,72 lít khí SO2 (đktc) tác dụng với dung dịch Ba(OH)2 dư. Tính khối lượng kết tủa thu được
\(n_{SO_2}=\dfrac{6,72}{22,4}=0,3\left(mol\right)\)
PTHH: Ba(OH)2 + SO2 --> BaSO3 + H2O
0,3----->0,3
=> mBaSO3 = 0,3.217 = 65,1 (g)
Đúng 4
Bình luận (0)
`n_(SO_2) = (6.72)/(22.4) = 0,3 mol`.
Ta có: `Ba(OH)_2 + SO_2 -> BaSO_3 + H_20`
`=> n_(BaSO_3) = 0,3 xx 1 : 1 = 0,3`.
`=> m_(BaSO_3) = 0,3 xx 217 = 65,1 g`.
Đúng 0
Bình luận (0)
Cho 4,48 lít SO2 tác dụng với 200ml dung dịch Ba(OH)2 sản phẩm thu được là BaSO3 và H2O. Tính khối lượng chất kết tủa thu được
\(n_{SO_2}=\dfrac{4,48}{22,4}=0,2\left(mol\right)\)
\(SO_2+Ba\left(OH\right)_2\rightarrow BaSO_3\downarrow+H_2O\)
0,2------------------>0,2
\(m_{kt}=m_{BaSO_3}=0,2.217=43,4\left(g\right)\)
Đúng 1
Bình luận (0)
Cho 6,1975 lít khí SO2(đktc) tác dụng vừa đủvới ddBa(OH)22M
a) Viết PTHH
b) Tính khối lượng muối tạo thành
c) Tính thểtích dung dịch Ba(OH)2cần dùng ?
(Biết Ba = 137 , H = 1 , S = 32 , O = 16 )
a) \(n_{SO_2}=\dfrac{6,1975}{24,79}=0,25\left(mol\right)\)
PTHH: SO2 + Ba(OH)2 → BaSO3 + H2O
Mol: 0,25 0,25 0,25
b) \(m_{BaSO_3}=0,25.217=54,25\left(g\right)\)
c) \(V_{ddBa\left(OH\right)_2}=\dfrac{0,25}{22}=\dfrac{1}{88}\left(l\right)\)
Đúng 0
Bình luận (2)
Biết 24,79 lít khí CO2 (Carbon dioxide) ở 25oC, 1 bar tác dụng vừa hết với 200 ml dd Ba(OH)2 (Barium hydroxide) sản phẩm là BaCO3 và H2O
a. Tính nồng độ mol của dd Ba(OH)2 đã dùng
b. Tính khối lượng chất kết tủa BaCO3 (Barium carbonate) thu được.
trung hoà vừa đủ 500ml dung dịch BA(OH)2 1M(d=1,1g/ml) với 500gam dung dịch H2SO4 15%.Sau khi phản ứng kết thúc thấy tạo ra chất kết tủa màu trắng
Hãy:
a)Viết PTHH xảy ra
b)Tính khối lượng H2SO4 đã dùng
c)Tính khối lượng chất kết tủa thu được
d)Chất nào còn dư,tính nồng độ chất dư trong dung dịch sau phản ứng
(cho Ba=137, H=1, O=16, S=32)
500ml=0.5l
nBaOH2 =0.5 x1=0.5 mol
MH2SO4=500.15%=75g
nH2SO4= xấp xỉ 0.8mol
H2SO4 dư tính theo BaOH2
pthh: Ba(OH)2 + H2SO4 => BaSO4+H2O
Theo pthh nBaSO4= nBa(OH)2=0.5mol
=>m kết tủa= 0.5x233=116.5g
theo pthh nH2SO4 phản ứng=nBaOH2= 0.5 mol
=> nH2SO4 Dư=0.8-0.5=0.3 mol
=>
m dư=0.3x98=29.4g
mH2SO4 đã dùng là m phản ứng? nếu thế thì m đã dung là 75-29.4=45.6
còn nếu m đã dùng là m chất tan thi là 75g như trên =))
Đúng 0
Bình luận (1)
Cho 1,12 lít khí CO2 (đktc) tác dụng với dung dịch Ba(OH)2 dư. Khối lượng chất kết tủa thu được là: