I. Trắc nghiệm
Nồng độ mol của dung dịch có chứa 50 gam CaBr 2 trong 400ml dung dịch là:
A. 0,625M
B. 0,15M
C. 0,45M
D. 1,25M
Câu 29: _TH_ Trong 500 ml dung dịch Na0H có chứa 2 gam chất tan. Nồng độ mol của dung dịch là:
A. 1M B. 0,2 M C. 0,1 M D. 0,15M
Câu 30: _VD_ Dung dịch Na0H 4M (D=1,43g/ml) có C% là:
A. 11 B. 12 C. 11,19 D. 11,89
29: Cụ thể: n(NaOH) =0,05mol
=>C =n/v = 0,05/0,5=0,1M
30, ta có C=10*D*C%/M
M là kluong mol
Từ đó tìm dc C%=11,19%
Câu 29:
nNaOH= 2/40=0,05(mol)
CMddNaOH=0,05/0,5=0,1(M)
Câu 30:
C%ddNaOH(4M)= (CMddNaOH.M(NaOH) )/10D= (4.40)/(10.1,43)= 11,19%
=> Chọn C
Trộn 100ml dung dịch HCl 0,8M với 400ml dung dịch Ca(OH)2 0,15M được dung dịch D.
a. Tính nồng độ mol/lít của ion OH- có trong dung dịch D
b. Tính thể tích dung dịch H2SO4 1M đủ để trung hòa dung dịch D
a)
nHCl=nH+=0,8.0,1=0,08 mol
nOH-=2.nCa(OH)2=2.0,15.0,1=0,12 mol
Khi trộn HCl với Ca(OH)2 xảy ra phản ứng trung hòa:
H+ + OH- ------H2O
0,08-----0,12
=>OH- dư
nOH- dư=0,12-0,08=0,04 mol
Vdung dịch sau pư=0,1+0,4=0,5 (l)
=> [OH- ]=0,04/0,5=0,8M
b) Dd D chứa 0,04 mol OH- dư (câu a)
Gọi thể tích H2SO4 Cần tìm là V (l)
=>nH+=2nH2SO4=2.1.v=2V (mol)
Khi cho H2SO4 vào D thì tiếp tục xảy ra pư trung hòa
H+ + OH- -------> H2O
2V -----0,04
vì phản ứng vừa đủ (đề cho)
=> mol H+=mol OH-
<=>2V=0,04<=>V=0,02 l
Dung dịch X chứa NaHCO3 0,15M và Ba(HCO3)2 0,45M. Dung dịch Y chứa Ca(OH)2 0,5M. Trộn dung dịch X và dung dịch Y với thể tích bằng nhau, thu được 400 ml dung dịch Z và m gam kết tủa. Giả sử tổng thể tích dung dịch không đổi khi pha trộn. Giá trị của m là
A. 19,00
B. 29,70
C. 39,40
D. 27,73
a/ Trong 250 gam dung dịch đồng (II) sunfat có chứa 0,3 mol đồng (II) sunfat. Tính C% của dung dịch đồng (II) sunfat trên.
b/ Tính CM của 400ml dung dịch có chứa 63,5g sắt (II) clorua?
a)
m CuSO4 = 0,3.160 = 48(gam)
C% CuSO4 = 48/250 .100% = 19,2%
b)
n FeCl2 = 63,5.127 = 0,5(mol)
CM FeCl2 = 0,5/0,4 = 1,25M
a, Ta có : nCuSO4 = 0,3 mol
=> mCuSO4 = n.M = 48g
\(\Rightarrow C\%=\dfrac{m}{m_{dd}}.100\%=19,2\%\)
b, Ta có : mFeCl2 = 63,5g
=> nFeCl2 = m/M = 0,5mol
=> \(C_M=\dfrac{n}{V}=1,25M\)
Trong 400ml dung dịch có chứa 32g CuSO4. Nồng độ MOL của dung dịch đó là
n=32/(64+32+16.4)=0,2mol
đổi 400ml=0,4L
CM=0,2/0,4=0,5M
Trong 400ml dung dịch có chứa 19,6g H2SO4. Nồng độ MOL của dung dịch đó là
Ta có: \(n_{H_2SO_4}=\dfrac{19,6}{98}=0,2\left(mol\right)\) \(\Rightarrow C_{M_{H_2SO_4}}=\dfrac{0,2}{0,4}=0,5\left(M\right)\)
Cho một hỗn hợp gồm 0,56 gam Fe và 0,64 gam Cu vào 100 ml dung dịch AgNO3 0,45M. Khi kết thúc phản ứng thu được dung dịch. A. Nồng độ mol/lit của dung dịch Fe(NO3)2 trong A là:
A. 0,04
B. 0,05
C. 0,055
D. 0,045
Chọn đáp án B.
![]()
n A g N O 3 = 0 , 045 m o l
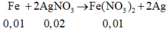
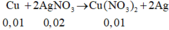

⇒ C M F e N O 3 2 = 0 , 005 0 , 1 = 0 , 05 M
Cho một hỗn hợp gồm 0,56 gam Fe và 0,64 gam Cu vào 100 ml dung dịch AgNO3 0,45M. Khi kết thúc phản ứng thu được dung dịch. A. Nồng độ mol/lit của dung dịch Fe(NO3)2 trong A là:
A. 0,04
B. 0,05
C. 0,055
D. 0,045.
trong 0.5l dung dịch axit có chứa 3.75 gam hcl. Nồng độ mol của dung dịch là A 2 B 5 C3 D 4
\(n_{HCl}=\dfrac{3,75}{36,5}\approx0,1\left(mol\right)\\ \Rightarrow C_{MddHCl}=\dfrac{0,1}{0,5}=0,2M\)
... bài này bn vừa đăng hỏi rồi á :v, trong khoảng thời gian 2 lần đăng đã có người giải cho bn rồi mà :) ?