Cho 15,6g 1 KL kiềm và 1 KL thỗ trong 1 chu kì tác dụng vs HCl dư thu 11,2 lít (đktc) . Xác định 2 KL trên

Những câu hỏi liên quan
Cho 0,3 gam hỗn hợp KL X và Y ở 2 chu kì kế tiếp nhau của nhóm IA tác dụng với H2O dư thu được 0,224 lit H2(đktc). Xác định tên 2 KL kiềm.
Gọi 2 kim loại kiềm của nhóm IA là M
n h2 = 0,224: 22,4=0,01 mol
M + 2H2O -> 2MOH + H2
n M = 0,3/ M M = n H2 = 0,01
=> M M = 30 đvc
mà M là 2 kim loại kiềm thuộc chu kì liên tiếp
=> M gồm Li và Na
Đúng 1
Bình luận (0)
xin lỗi mk làm nhầm
gọi 2 kl kiềm của nhóm IA là R
n H2 = 0,224:22,4=0,01 mol
n R = 0,3/ M R mol
2R + 2H2O -> 2ROH +H2
=> nR = n H2 .2
=> 0,3/M R = 0,02
=> M R =15 đvc
ko có gt nào tm
Đúng 0
Bình luận (0)
Cho 1,38 gam KL kiềm tác dụng với H2O dư thu được 0,672 lit H2 (đktc). Xác định tên KL
Gọi kim loại kiềm là R
PTHH: 2R + 2xH2O ---> 2R(OH)x + xH2
Ta có: \(n_{H_2}=\dfrac{0,672}{22,4}=0,03\left(mol\right)\)
Theo PT: \(n_R=\dfrac{2}{x}.n_{H_2}=\dfrac{2}{x}.0,03=\dfrac{0,06}{x}\left(mol\right)\)
=> \(M_R=\dfrac{1,38}{\dfrac{0,06}{x}}=\dfrac{1,38x}{0,06}=23x\left(g\right)\)
Biện luận:
| x | 1 | 2 | 3 |
| M | 23 | 46 | 69 |
| Na | loại | loại |
Vậy kim loại kiềm là natri (Na)
Đúng 1
Bình luận (0)
Gọi kim loại kiềm cần tìm là M. (kim loại kiềm có hóa trị l)
\(n_{H_2}=\dfrac{0,672}{22,4}=0,03mol\)
\(2M+H_2O\rightarrow M_2O+H_2\)
0,06 0,03
\(\Rightarrow n_M=\dfrac{1,38}{\overline{M_M}}=0,06\) \(\Rightarrow\overline{M_M}=23\left(Na\right)\)
Vậy kim loại M cần tìm là Natri(Na).
Đúng 1
Bình luận (3)
Cho 10 gam KL kiềm thổ tác dụng với H2O dư thu được 5,6 lit H2 (đktc). Xác định tên KL
\(n_{H_2}=\dfrac{5,6}{22,4}=0,25\left(mol\right)\)
PTHH: 2X + 2nH2O → 2XOHn + nH2
Mol: \(\dfrac{0,5}{n}\) 0,25
\(\Rightarrow M_X=\dfrac{10}{\dfrac{0,5}{n}}=20n\left(g/mol\right)\)
Vì X là kim loại nên có hóa trị l,ll,lll
| n | l | ll | lll |
| Mx | 20 | 40 | 60 |
| Kết luận | loại | thỏa mãn | loại |
⇒ X là canxi (Ca)
Đúng 1
Bình luận (0)
Cho 3,1 g hỗn hợp gồm hai kim loại kiềm ở hai chu kì kế tiếp nhau trong bảng tuần hoàn tác dụng hết với nước thu được 1,12 lít H2 ở đktc và dung dịch kiềm. Xác định tên 2 KL đó và tính thành phần phần trăm khối lượng mỗi kim loại
Gọi công thức chung cho hai kim loại kiềm là M
Số mol H2: nH2 = 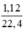 = 0,05(mol)
= 0,05(mol)
PTHH: 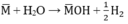
Theo pt: nM = 2. nH2 = 2. 0,05 = 0,1(mol)
⇒ M = 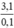 = 31 → Na, K
= 31 → Na, K
Gọi x, y lần lượt là số mol của Na và K trong hỗn hợp
Theo bài ra ta có hệ phương trình:
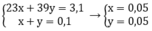
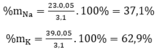
Đúng 1
Bình luận (0)
Cho 8,8 gam một hỗn hợp gồm 2 kim loại ở 2 chu kì liên tiếp thuộc nhóm IIA tác dụng với dd HCl dư cho 6,72 lít khí hiđro ở đktc. Xác định tên 2 kim loại và % khối lượng mỗi kl trong hh ban đầu.
Đọc tiếp
Cho 8,8 gam một hỗn hợp gồm 2 kim loại ở 2 chu kì liên tiếp thuộc nhóm IIA tác dụng với dd HCl dư cho 6,72 lít khí hiđro ở đktc. Xác định tên 2 kim loại và % khối lượng mỗi kl trong hh ban đầu.
Gọi công thức chung của 2 kim loại là R
\(HCIII\text{R + 2HCl -> RCl2 + H2}I->RCI2+H2\)
Ta có : \(nH2=0,3mol->M\text{ R}=8,8\)/\(0,3=29,3\)
Ta có : \(\text{24 < 29,3 < 40 nên 2 kim loại là Mg và Ca}\)
Gọi số mol Mg và Ca lần lượt là x , y
\(\text{-> x+y=0,3; 24x+40y=8,8}\)
Giải được \(\text{x = 0,2 ; y = 0,1 }\)
\(\text{-> mMg=24.0,2=4,8 gam -> %Mg=54,5% -> %Ca=45,5%}\)
Đúng 1
Bình luận (0)
Cho 3,87g hỗn hợp Mg và Al tác dụng vs lượng dư dd HCl, sau p/ứ thu đc 4,368 lít khí H2 (đktc). Xác định % kl từg kim loại trog ngợp ban đầu Giúp mình vs ạk
\(n_{H_2}=\dfrac{4,368}{22,4}=0,195\left(mol\right)\)
PTHH: Mg + 2HCl → MgCl2 + H2
Mol: x x
PTHH: 2Al + 6HCl → 2AlCl3 + 3H2
Mol: y 1,5y
Ta có: \(\left\{{}\begin{matrix}24x+27y=3,87\\x+1,5y=0,195\end{matrix}\right.\Leftrightarrow\left\{{}\begin{matrix}x=0,06\\y=0,09\end{matrix}\right.\)
\(\Rightarrow\%m_{Mg}=\dfrac{0,06.24.100\%}{3,87}=37,21\%\)
\(\%m_{Al}=100-37,21=62,79\%\)
Đúng 1
Bình luận (0)
Cho 3,2g hỗn hợp 2 kim loại kiềm thuộc 2 chu kì liên tiếp tác dụng với dd HCl dư thu được 1,12 lít khí H2 ( đkc). Vậy 2 KL kiềm là
A. Li và Na
B. K và Rb
C. Rb và Cs
D. Na và K
Cho 11,04 gam KL kiềm tác dụng với H2O dư thu được 0,48 gam H2. Xác định tên KL
Gọi kim loại kiềm là R.
PTHH: 2R + 2xH2O ---> 2R(OH)x + xH2
Ta có: \(n_{H_2}=\dfrac{0,48}{2}=0,24\left(mol\right)\)
Theo PT: \(n_R=\dfrac{2}{x}.n_{H_2}=\dfrac{2}{x}.0,24=\dfrac{0,48}{x}\left(mol\right)\)
=> \(M_R=\dfrac{11,04}{\dfrac{0,48}{x}}=\dfrac{11,04x}{0,48}=23x\left(g\right)\)
Biện luận:
| x | 1 | 2 | 3 |
| M | 23 | 46 | 69 |
| Na | loại | loại |
Vậy kim loại kiềm là natri (Na)
Đúng 1
Bình luận (1)
1/ Hòa tan 3,6g một kl hóa trị II vào 146g dd HCl thu được 3,36 lít khí (đkc)
a) R là kl nào?
b) Tính nồng độ C% của muối trong dd?
2/ Cho 1,4g hh gồm 2 kl ở 2 chu kì liên tiếp thuộc nhóm IA vào nước (dư) thu dc dd kiềm có m tăng 1,36g so vs m nước ban đầu. 2 kl đó là ?
3/Nguyên tố A nhóm VIA. Trong oxit cao nhất, tỉ lệ m giữa A và õi là 2/3. Tìm A?
1/a) X: KL hoá trị II
X+ 2HCl ----> XCl2 + H2
0.15 0.3 0.15
n H2= 3.36/22.4=0.15 mol
M X= 3.6/0.15=24 g/mol
=> X là Mg
b) Mg + 2HCl ----> MgCl2 + H2
0.15 0.3 0.15 0.15
m MgCl2= 0.15 x 95= 14.25g
Định luật bảo toàn khối lượng
mdd MgCl2= 3.6 + 146 - (0.15x2)=149.3g
C%=( 14.25x 100)/ 149.3= 9.5%
Đúng 0
Bình luận (0)



















