Trong tự nhiên Clo có hai đồng vị bền 3717Cl chiếm 24,23% tổng số nguyên tử, còn lại 3517Cl. Tính thành phần phần trăm theo khối lượng của 3717Cl trong HClO4

Những câu hỏi liên quan
Trong tự nhiên clo có hai đồng vị bền: 37Cl chiếm 24,23% tổng số nguyên tử, còn lại là 35Cl
Xác định thành phần phần trăm theo khối lượng của mỗi đồng vị , trong HClO4
Nguyên tố clo có hai đồng vị bền với tỉ lệ phần trăm số nguyên tử tương ứng là: 1735Cl chiếm 75,77% và 3717Cl chiếm 24,23%. Trong phân tử CaCl2, % khối lượng của 3517Cl là (biết nguyên tử khối trung bình của canxi là 40)A. ≈ 23,89. B. ≈ 47,79. C. ≈ 16,15. D. ≈ 75,77.
Đọc tiếp
Nguyên tố clo có hai đồng vị bền với tỉ lệ phần trăm số nguyên tử tương ứng là: 1735Cl chiếm 75,77% và 3717Cl chiếm 24,23%. Trong phân tử CaCl2, % khối lượng của 3517Cl là (biết nguyên tử khối trung bình của canxi là 40)
A. ≈ 23,89. B. ≈ 47,79. C. ≈ 16,15. D. ≈ 75,77.
1 mol CaCl₂ có 2 mol Cl, ³⁵₁₇Cl chiếm 75,77% trong 2 mol tổng Cl ứng với 1,5154 mol, còn lại là 0,4846 mol ³⁷₁₇Cl
=> %m³⁵₁₇Cl = 1,5154 × 35 ÷ (40 + 1,5154 × 35 + 0,4846 × 37) ≈ 47,79%
Đúng 3
Bình luận (1)
Trong tự nhiên Clo có hai đồng vị bền:
C
27
37
l
chiếm 24,23% tổng số nguyên tử, còn lại là
C
17
37
l
. Phần trăm theo khối lượng của
C
17
37
l
trong HClO4 là: A. 8,43% B. 8,9...
Đọc tiếp
Trong tự nhiên Clo có hai đồng vị bền: C 27 37 l chiếm 24,23% tổng số nguyên tử, còn lại là C 17 37 l . Phần trăm theo khối lượng của C 17 37 l trong HClO4 là:
A. 8,43%
B. 8,92%
C. 8,79%
D. 8,56%
Đáp án : B
Xét 1 mol HClO4 có 1 mol Cl
=> có 0,2423 mol C 37 l
% m C 17 37 l ( H C l O 4 ) = 8 , 92 %
Đúng 0
Bình luận (0)
Trong tự nhiên Clo có hai đồng vị bền:
C
17
37
l
chiếm 24,23% tổng số nguyên tử, còn lại là
C
17
35
l
. Thành phần % theo khối lượng của
C
17
37
l
trong HClO4 là:
Đọc tiếp
Trong tự nhiên Clo có hai đồng vị bền: C 17 37 l chiếm 24,23% tổng số nguyên tử, còn lại là C 17 35 l . Thành phần % theo khối lượng của C 17 37 l trong HClO4 là:
Trong tự nhiên Clo có hai đồng vị bền 17Cl37 chiếm 24,23% tổng số nguyên tử ,còn lại là 17Cl35. Thành phần % theo khối lượng của 17Cl37 trong HClO4 là : A. 8,92% B. 8,43% C. 8,56% D. 8,79%
Đọc tiếp
Trong tự nhiên Clo có hai đồng vị bền 17Cl37 chiếm 24,23% tổng số nguyên tử ,còn lại là 17Cl35. Thành phần % theo khối lượng của 17Cl37 trong HClO4 là :
A. 8,92%
B. 8,43%
C. 8,56%
D. 8,79%
Trong tự nhiên clo có hai đồng vị bền: 37Cl chiếm 24,23% tổng số nguyên tử, còn lại là 35Cl (Cl có số hiệu nguyên tử là 17). Thành phần % theo khối lượng của 37Cl trong HClO4 là (Cho: H 1, O 16): A. 8,92% B. 8,43% C. 8,56% D. 8,79%
Đọc tiếp
Trong tự nhiên clo có hai đồng vị bền: 37Cl chiếm 24,23% tổng số nguyên tử, còn lại là 35Cl (Cl có số hiệu nguyên tử là 17).
Thành phần % theo khối lượng của 37Cl trong HClO4 là (Cho: H = 1, O = 16):
A. 8,92%
B. 8,43%
C. 8,56%
D. 8,79%
Đáp án A
• %35Cl = 100% - 24,23% = 75,77%
→ MCl = 37 x 0,2423 + 35 x 0,7577 = 35,4846.
→ Thành phần % của 37Cl trong HClO4 là
![]()
Đúng 0
Bình luận (0)
Trong tự nhiên clo có hai đồng vị bền là
C
17
35
l
chiếm 75,77% tổng số nguyên tử, còn lại là
C
17
35
l
. Thành phần phần trăm theo khối lượng của
C
17
35
l
trong HClO4 là: A. 8,92 B. 8,79. C. 8,56 D. 8,43.
Đọc tiếp
Trong tự nhiên clo có hai đồng vị bền là C 17 35 l chiếm 75,77% tổng số nguyên tử, còn lại là C 17 35 l . Thành phần phần trăm theo khối lượng của C 17 35 l trong HClO4 là:
A. 8,92
B. 8,79.
C. 8,56
D. 8,43.
Chọn A
Ta có
M
C
l
¯
=
24
,
23
.
37
+
75
,
77
.
37
100
=
35
,
5
Trong 1 mol HClO
3
thì
C
17
37
l
có 0,2423 mol nên %= 8,92%
Đúng 0
Bình luận (0)
Trong tự nhiên chlorine có 2 đồng vị bền : ³⁷Cl chiếm 24,23% tổng số nguyên tử ,còn lại là ³⁵Cl . Thành phần % theo khối lượng của ³⁵Cl trong HClO4
Nguyên tử khối trung bình của clo là 35,5. Clo trong tự nhiên có 2 đồng vị là 35 Cl và 37Cl. Phần trăm khối lượng của 3717Cl chứa trong HClO4 ?(với hidro là đồng vị 11H, oxi là đồng vị 168O) là.
Tham thảo :
Phần trăm đồng vị 35Cl = x, thì % đồng vị 37Cl = 100 - x
Ta có:
![]() , vậy x = 75%.
, vậy x = 75%.
Phần trăm khối lượng của 37Cl trong HClO4= 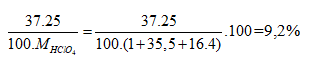
Đúng 0
Bình luận (0)
Clo có hai đồng vị 3717Cl và 3517Cl. Nguyên tử khối trung bình của Clo là 35,48. Phần trăm đồng vị 37Cl là A. 65% B. 76% C. 35% D. 24%
Đọc tiếp
Clo có hai đồng vị 3717Cl và 3517Cl. Nguyên tử khối trung bình của Clo là 35,48. Phần trăm đồng vị 37Cl là
A. 65%
B. 76%
C. 35%
D. 24%
Đáp án D
Gọi phần trăm đồng vị của 37Cl là x thì phân trăm đồng vị 35Cl là 100- x
Ta có:
M Cl = 35 , 48 = ( 37 x + 35 ( 100 - x ) ) / 100
=> x=24
Đúng 0
Bình luận (0)
















